
Themen • Kurzbeiträge • Streiflichter
Die „Sauerstoffkatastrophe“
2. Forschen nach den Ursachen des „great oxygenation event“
1. Extreme Krise als Auslöser genialer „Neuerfindungen“ des Lebens?
von Boris Schmidtgall
Studium Integrale Journal
28. Jahrgang / Heft 2 - September 2021
Seite 95 - 103
Zusammenfassung: Der ungewöhnlich hohe Sauerstoffanteil der Erdatmosphäre im Vergleich zu anderen Planeten wird gegenwärtig durch eine unumkehrbare Anreicherung der Atmosphäre mit Sauerstoff erklärt – die sogenannte „Sauerstoffkatastrophe“. Die Forschung nach möglichen natürlichen Ursachen für dieses vermutete Ereignis in der frühen Naturgeschichte erfährt viel Aufmerksamkeit unter Naturforschern. Allerdings bieten bisher angeführte Erklärungen wie geologische Sauerstoff-Quellen oder die Evolution der Photosynthese kaum Antworten auf Kernfragen zu dieser Besonderheit unseres Planeten.
• • • • • • • • •
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.

Einleitung
Der Ausspruch „never change a running system“ bringt die im Bereich der Technik oft gemachte Erfahrung zum Ausdruck, dass es anspruchsvoll ist, ein komplexes funktionales Gefüge umzubauen. Bei Automobilen kann eine Preiserhöhung oder das Verbot eines bestimmten Treibstoffs eine Herausforderung darstellen, die den Umbau veranlasst. Dabei sind allerdings technische Einschränkungen zu berücksichtigen und in manchen Fällen kann die Inkompatibilität von Bauteilen und Funktionsweisen eine Umbaumaßnahme verunmöglichen. Eine Umrüstung vom Benzinantrieb auf einen Erdgasantrieb ist problemlos machbar. Dagegen würden wegen enormen Aufwands und hoher Kosten nur wenige erwägen, einen Dieselmotor entsprechend umzubauen und die Umrüstung eines Verbrennermotors zu einer Brennstoffzelle oder einem elektrisch betriebenen Motor würde wohl niemand vornehmen. Abgesehen von ihren Unterschieden gilt für alle Umrüstungen: Bei laufendem Motor sind sie unmöglich – anders als z. B. die Neumontage eines Rückspiegels oder eines Autoradios.
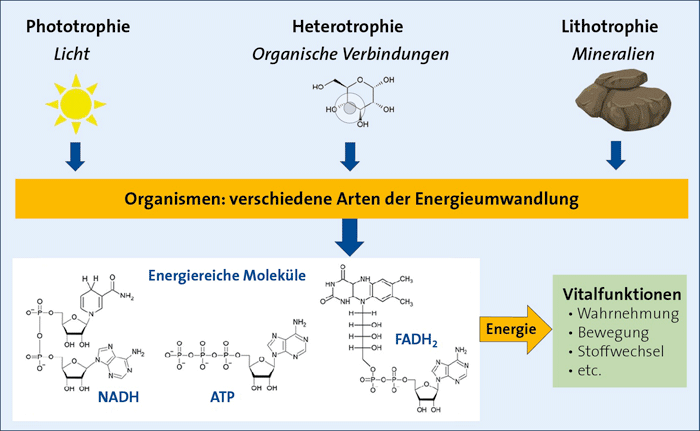
Abb. 1: Die drei Arten der Energiehaushalte in Organismen. Phototrophe Organismen nutzen Lichtenergie, heterotrophe die Energie organischer Moleküle und lithotrophe gewinnen sie aus Mineralien. In allen Organismen wird die Energie in Form von energiereichen organischen Molekülen (u. a. ATP, NADH, FADH2) zwischengespeichert.
In Analogie zu technischen Systemen sind auch Lebewesen auf Energieversorgung angewiesen, wobei auch hier die Verwertung verschiedener Energieträger möglich ist. Organismen, die Licht als Energiequelle nutzen, werden als „phototroph“ bezeichnet, solche, die sie aus Mineralien beziehen, als „lithotroph“, während „heterotrophe“ Organismen auf organische Verbindungen angewiesen sind. Die zentrale Gemeinsamkeit der unterschiedlichen Energiehaushalte ist die Zwischenspeicherung der Energie in organischen Verbindungen wie ATP, NAD(P)H oder FADH2 (Abb. 1).
Wie bei technischen Geräten gibt es auch bei Organismen die Nutzung von Energie ohne „Verbrennung“ (Phototrophie) und mit Verbrennung (Lithotrophie und Heterotrophie). Unter „Verbrennung“ versteht man in diesem Kontext einen exergonen* Elektronenübertragungsvorgang (Redoxreaktion), der die nutzbare Energie für die Bildung der energiereichen organischen Verbindungen liefert. Entscheidend für die Beschaffenheit des gesamten Energiehaushalts ist die Natur der Elektronenquelle und des Elektronenakzeptors. Während der Elektronenakzeptor bei heterotrophen Organismen immer der Sauerstoff ist, nutzen einige lithotrophe Organismen dazu auch andere chemische Verbindungen wie z. B. Sulfat. Heterotrophe Organismen sind demnach auf Sauerstoff angewiesen, während es einige lithotrophe Organismen gibt, die ohne Sauerstoff auskommen.
Im Unterschied zu technischen Systemen kann der Energiestoffwechsel von Organismen zu keiner Zeit gänzlich heruntergefahren werden, da dessen vollständiges „Ausschalten“ den Tod bedeuten würde. Eine Umrüstung des Energiestoffwechsels von einem „Treibstoff“ auf einen anderen wäre demnach für alle Lebewesen ein äußerst anspruchsvoller Vorgang. Gemäß Befürwortern der Evolutionslehre soll es die größte Herausforderung dieser Art in der frühen Phase der Evolution vor ca. 2,4 Milliarden Jahren gegeben haben: die Umstellung von der anoxischen* Atmosphäre zu einer mit Sauerstoff angereicherten – die sogenannte große „Sauerstoffkatastrophe“ („great oxygenation event“, GOE).
Wie in der vorigen Ausgabe von Studium Integrale Journal ausgeführt, wird die Hypothese des GOE durch eine Reihe von Indizien aus der Geologie und Paläobiologie belegt, die jedoch nicht zwingend das besagte Szenario nahelegen (Schmidtgall 2021). Für ein tragfähiges Modell müssten zudem auch plausible Ursachen eines solchen Vorgangs benannt werden können.
Es muss erklärt werden, durch welche natürlichen Vorgänge molekularer Sauerstoff auf der frühen Erde entstanden sein könnte.
Kompakt
Die Tatsache, dass unsere Atmosphäre ca. 21% Sauerstoff (O2) enthält, ist bisher einmalig unter allen uns bekannten Planeten. Hierfür wird seit Langem nach schlüssigen Erklärungen auf der Grundlage natürlicher Vorgänge gesucht. Dabei werden für die erstmalige Anreicherung der frühen Erdatmosphäre (sog. „great oxygenation event“, GOE) mit O2 entweder geologische Quellen oder biologische Ursachen angenommen.
Geologische Ursachen für das postulierte Szenario des GOE werden von einer großen Mehrheit der Wissenschaftler nicht befürwortet. Die photolytische* Spaltung von Kohlendioxid (CO2) bzw. Wasser durch UV-Strahlung würde zu einer sehr schnellen Anreicherung der Erdatmosphäre mit Sauerstoff führen und im Fall von Ausgasungen unterirdischer Sauerstoffvorräte wären sehr große Schwankungen der Sauerstoff-Konzentration zu erwarten, die für alle Organismen tödlich gewesen wären, sofern es bis dahin eine anoxische* Lebenswelt gab.
Auch die Erklärung der Anreicherung der Atmosphäre durch die Entwicklung O2-erzeugender Organismen erweist sich als nicht schlüssig. Hypothesen zur Evolution der oxygenen* Photosynthese gehen meistens von zwei verschiedenen Szenarien aus: 1. Das Modell des selektiven Verlusts, 2. Das Fusions-Modell. Es zeigt sich, dass beide Modelle keine guten Erklärungen für den schrittweisen Aufbau einer oxygenen Photosynthese darstellen. Es mangelt vor allem an stützenden Beobachtungen aus der Natur. Bei den Hypothesen handelt es sich ausschließlich um rein theoretische Überlegungen. Plausible Mechanismen für die Umrüstung von einer anoxygenen Photosynthese zu einer oxygenen fehlen dagegen.
Viel plausibler ist dagegen die Annahme, dass die verschiedenen Typen der Nutzung von Lichtenergie und die besondere Zusammensetzung der Erdatmosphäre weitere beeindruckende Zeugnisse für das ganzheitliche Werk des Schöpfers sind.
Hypothesen für die Herkunft von O2 in der Erdatmosphäre
Obwohl das Element Sauerstoff im Universum recht häufig vorkommt, ist Sauerstoff in der molekularen Form (O2) sehr selten. Daher ist es erstaunlich, dass die Erdatmosphäre zu 21% aus diesem Gas besteht. Zur Erklärung dieser Anomalie werden geochemische und biologische Vorgänge als mögliche Ursachen angeführt.
Geochemische Vorgänge
Photolyse* von Wasser oder CO2. Der Annahme einer nahezu sauerstofffreien Atmosphäre vor ca. 2,4 Milliarden Jahren zufolge dürfte es in dieser Zeit keine Ozonschicht und damit keinen wirksamen Schutz vor hartem UV-Licht gegeben haben. Hartes UV-Licht im Wellenlängenbereich von ca. 90-110 nm besitzt genügend Energie, um selbst die chemischen Bindungen stabiler Moleküle wie CO2 oder Wasser zu spalten. Es konnte experimentell nachgewiesen werden, dass CO2 unter der Einwirkung von hartem UV-Licht in Kohlenstoff und molekularen Sauerstoff gespalten wird (Lu et al. 2014). Dieser Vorgang läuft in zwei Schritten nach den folgenden Reaktionsgleichungen ab (hv = Energie des UV-Lichts; M: beliebiges Molekül, das freiwerdende Energie abfängt):
CO2 + hv → CO + O
O + O + M → O2 + M
In ähnlicher Weise verläuft auch die photolytische Spaltung von Wasser, wobei ebenfalls O2 entsteht. Bestätigt wurde dieser Sachverhalt auch durch die Korrelation der Mengen von molekularem Sauerstoff und Wasser auf Kometen (Yao & Giapis 2017). Chang et al. (2021) schätzen, dass dieser Prozess aufgrund des häufigen Vorkommens von Wasser auf der Erde eine bedeutende Quelle für Sauerstoff in der frühen Atmosphäre war. Für die Rate der photolytischen Spaltung des Wassers geben sie den Wert mit JH2O(O) = 5,2 • 10-5 s-1 an. Berechnet man ausgehend von dieser Zahl mit einigen vereinfachenden Annahmen die Menge an gebildeten Sauerstoff-Molekülen in der Erdatmosphäre, ergibt sich pro Jahr eine gebildete Masse von 3,8 • 1016 t an Sauerstoff-Molekülen (s. Kasten 1). Das entspricht ungefähr der siebenfachen Masse der heutigen Erdatmosphäre. Auch wenn diese Rechnung nur der Abschätzung einer Größenordnung dient, verdeutlicht sie, dass die Annahme der Wasserspaltung durch UV-Licht als Quelle für Sauerstoff eine sehr schnelle Anreicherung der Atmosphäre mit O2 impliziert. Dies steht jedoch in deutlichem Widerspruch zu der weit verbreiteten Annahme, dass der Sauerstoff in der Atmosphäre vor dem GOE im Verlauf von ca. 1 Milliarde Jahren nur ein Spurengas war (das 10-5-fache der heutigen Konzentration nach Knoll & Nowak 2017 und Lyons et al. 2014).
Freisetzung von Sauerstoff aus tiefen Schichten. Als weitere nicht-biologische Quelle für Sauerstoff in der frühen Erdgeschichte gilt die Anreicherung tiefer Schichten mit Sauerstoff durch die Disproportionierungsreaktion von Eisen(II)oxid (FeO) (Frost et al. 2004, Andrault et al. 2018):
6FeO → 2Fe0 + 2Fe2O3
Während das metallische Eisen (Fe0) weiter in Richtung des Erdkerns sinkt, verbleibt das Fe2O3 in einer Tiefe von ca. 660 km. Auf diese Weise liegt das Element Sauerstoff im Verhältnis zum Eisen in einem Überschuss vor. Andrault et al. nehmen an, dass während des Archaikums* keine Absenkung der oberen Gesteinsschichten gegeben war, sodass der überschüssige Sauerstoff in tieferen Schichten nach Ausbildung des stark Fe0-haltigen Erdkerns gefangen war. Diesen Sauerstoff-Überschuss berechneten Andrault et al. mengenmäßig zu dem 500 bis 1000-Fachen der gegenwärtigen Menge in der Erdatmosphäre. Erst nach einer Abkühlung der Erdoberfläche und der einsetzenden Gesteinskonvektion* soll es zu einem allmählichen Entweichen des Sauerstoffs als O2 über Vulkanausbrüche gekommen sein. Auf diese Weise soll die zuvor anoxische Atmosphäre mit Sauerstoff angereichert worden sein. Andrault et al. berechneten die Rate der Entweichung des Sauerstoffs zu 1,5 • 1013 mol/Jahr, woraus nach ihrer Rechnung für die Zeitspanne der Oxygenierung der Atmosphäre bis zum heutigen Sauerstoffgehalt 2,6 Millionen Jahre resultierten.
Ein allmähliches, gleichmäßiges Entweichen des Sauerstoffs aus den unteren Schichten über eine so lange Zeitspanne erscheint jedoch alles andere als plausibel. Vielmehr würde es bei solchen Prozessen wiederholt zu katastrophisch schnellen Zunahmen der O2-Konzentration in der Atmosphäre kommen. Das erwähnen auch die Autoren der besagten Arbeit: „Von Oszillationen und Schwankungen des atmosphärischen Partialdrucks des Sauerstoffs einige 100 Millionen Jahre um den Übergang vom Archaikum zum Proterozoikum* herum ist bereits berichtet worden.“ Dabei führen sie aber keinerlei quantitative Details zu solchen Schwankungen an, die für eine hypothetische Biosphäre, welche bis dahin kaum mit Sauerstoff in Kontakt gekommen sein soll, vernichtend gewesen wären.
Biologische Ursachen
Viele Forscher sind gegenwärtig der Auffassung, dass die nicht-biologischen Sauerstoff-Quellen höchstens für geringfügige, schubartige Zunahmen der Sauerstoff-Konzentration in der Atmosphäre ursächlich gewesen sein können (Anbar et al. 2007). Als eigentliche Ursache des GOE wird die Entstehung eines neuartigen bakteriellen Stoffwechsels gesehen: Es wird angenommen, dass vor ca. 2,7–2,5 Milliarden Jahren bestimmte Cyanobakterien evolviert sind, deren Photosyntheseaktivität mit der Bildung von Sauerstoff einherging (oxygene Photosynthese). Um Hypothesen zum Ursprung der oxygenen Photosynthese zu beurteilen, sollen zunächst einige Aspekte zu diesem biochemischen Vorgang zur Sprache kommen. Dabei werden ausschließlich Chlorophyll-basierte Photosysteme (PS) diskutiert, da Rhodopsin-basierte PS gegenwärtig bezüglich der Diskussion um den GOE keine Rolle spielen (Fischer et al. 2016).
1 | Rechnerische Schätzung der entstehenden Sauerstoff-Menge durch Photolyse von H2O
Das Wasservolumen V in der Atmosphäre wird auf ca. V (H2O) = 1,3 • 1016 l geschätzt. Das entspricht einer Stoffmenge von n (H2O) = 7,22 • 1017 mol Wasser. Um die pro Sekunde gebildete Stoffmenge n (O2) an photolytisch gebildetem O2 zu erhalten, muss also die Stoffmenge n (H2O) mit der Rate der photolytischen Spaltung des Wassers JH2O(O) multipliziert werden:
n (O2) = n (H2O) • JH2O(O)
= 3,75 • 1013 mol/s
Umgerechnet auf ein Jahr ergibt dies 1,18 • 1021 mol O2. Die Umrechnung in Masseneinheiten ergibt 3,8 • 1016 t O2 pro Jahr.
Oxygene Photosynthese
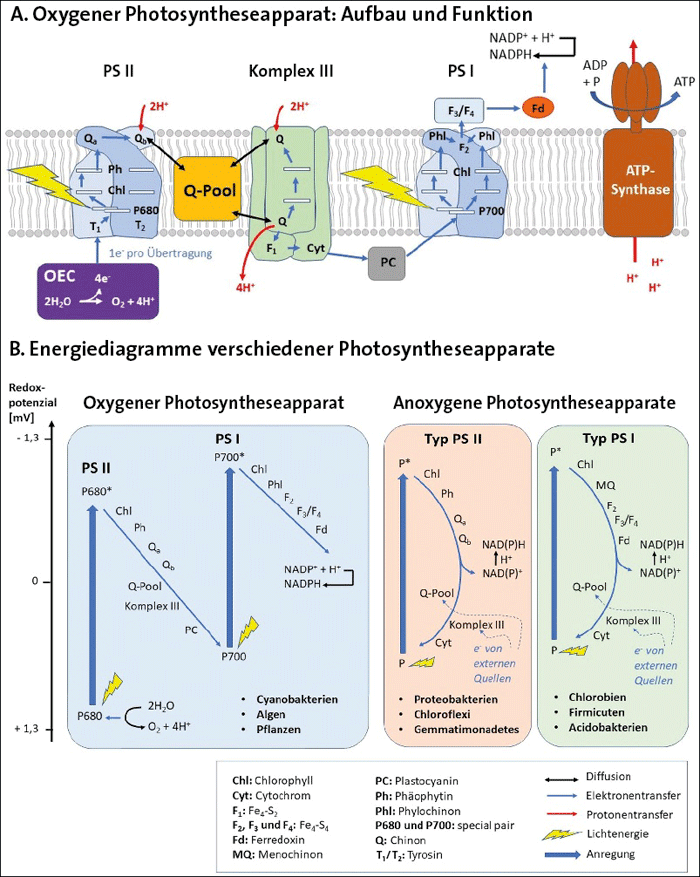
Abb. 2: A. Der oxygene Photosyntheseapparat ist aus fünf Protein-Komponenten aufgebaut: Den zwei Photosystemen (PS I und PS II), dem OEC (Oxygen Evolving Complex), dem Komplex III und der ATP-Synthase (weitere Erläuterungen siehe Kasten 2).
B. Vergleich der Energieflüsse in den verschiedenen Photosyntheseapparaten. Einzig der oxygene Photosyntheseapparat verfügt über ein PS mit niedrigem elektrochemischen Potenzial. Die PS anoxygener Photosyntheseapparate hingegen sind ausnahmslos Hochpotenzial-Systeme. Die PS einiger Organismen (Proteobakterien, Chloroflexi und Gemmatimonadetes) ähneln dem PS II der oxygenen Photosynthese, andere hingegen dem PS I (Chlorobi, Firmicuten, Acidobakterien). Der gesamte Elektronenfluss der anoxygenen Photosynthese ist im Unterschied zur oxygenen Variante zyklisch. (Nach Fischer et al. 2016)
Die Photosynthese stellt die Grundlage für Leben auf der Erde dar. Dieser Vorgang ermöglicht die Nutzung der ca. 100.000 TW (Terawatt) Strahlungsleistung der Sonne, die auf die Erde gelangen, indem etwa 1350 TW in Form von chemisch gespeicherter Energie zur Verfügung gestellt werden können – fast das Hundertfache dessen, was die Menschheit verbraucht. Von den molekularen Einrichtungen, die diese Energie einfangen, ist bis heute eine Reihe von verschiedenen Typen beschrieben worden, die sowohl Unterschiede als auch auffallende Gemeinsamkeiten haben (Fischer et al. 2016; Nelson & Junge 2015; Hohmann-Mariott & Blankenship 2011). Die oxygene Photosynthese wird von Algen, Pflanzen und Cyanobakterien genutzt und stellt hinsichtlich des molekularen Aufbaus und ihrer Funktionsweise die anspruchsvollste Variante der Verwertung von Lichtenergie dar (Abb. 2A).
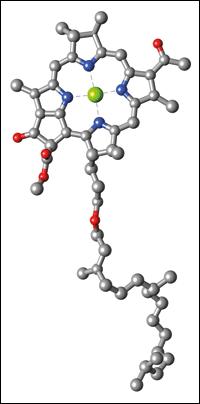
Abb. 3: Kugel-Stab-Modell eines Bakteriochlorophyll-Moleküls (mit Verankerung). Kohlenstoff-Atome sind grau dargestellt, Sauerstoff-Atome rot, Stickstoff-Atome blau und das Magnesium-Ion grün. Wasserstoff-Atome sind der Übersichtlichkeit halber nicht abgebildet.
Bei der oxygenen Photosynthese wird Lichtenergie genutzt, um aus Kohlendioxid Biomasse (Kohlenhydrate) aufzubauen, wobei molekularer Sauerstoff als Nebenprodukt anfällt. Die Bruttoreaktion dieses Vorgangs ist:
CO2 + H2O → (CH2O) + O2
Wie aus der Gleichung hervorgeht, wird hierbei Wasser zu Sauerstoff oxidiert und Kohlendioxid zu Kohlenhydraten reduziert – zwei ausgesprochen endergone* Vorgänge. Die für diese anspruchsvollen chemischen Transformationen zuständigen biomolekularen Vorrichtungen sind in der Natur einzigartig und in ihrer Funktionsweise außerordentlich effizient. Sie sind aus vier membranintegrierten, großen Proteinkomplexen und einer Vielzahl an verschiedenen Cofaktoren aufgebaut. Durch ihr exaktes Zusammenspiel werden Elektronen vom Wassermolekül zum Reduktionsäquivalent NADP+ übertragen, bei gleichzeitiger Ausbildung eines Protonengradienten, der zur Synthese von ATP durch die ATP-Synthase genutzt wird. Die gebildeten energiereichen Moleküle NADPH und ATP werden später zur Umwandlung von CO2 in Kohlenhydrate in der Dunkelreaktion verwendet, auf die hier nicht weiter eingegangen werden soll. Die zentralen Funktionseinheiten der oxygenen Photosyntheseapparate sind die als Photosysteme (PS) bezeichneten Proteinkomplexe PS I und PS II. In den Reaktionszentren dieser spiralförmig geformten Komplexe befinden sich zwei Chlorophyllmoleküle, an denen sich die energetische Anregung von Elektronen durch Photonen ereignet (Abb. 3). Für diese zwei Chlorophyllmoleküle hat sich die Bezeichnung „special pair“ etabliert.
Die hohe Effizienz der Photosynthese wird vor allem durch die Art und Anordnung der molekularen Bausteine der PS sichergestellt. Eines der am häufigsten vorkommenden Moleküle in den PS I und II ist das Chlorophyll, welches mit einem Wert von über 105 M-1cm-1 einen der höchsten Extinktionskoeffizienten* unter kleinen Molekülen besitzt (Stryer et al. 2007). In beiden Photosystemen liegen weit mehr als 80 Chlorophylle vor, die allesamt am „light harvesting“ (LH), dem „Ernten“ von Lichtenergie beteiligt sind. Die dichte, ringförmige Anordnung der LH-Komplexe um das Reaktionszentrum herum ermöglicht eine überaus effektive, kohärente Energieübertragung zum „special pair“ über verschiedene Arten des Energietransfers (Vibration, elektrodynamische Kopplung). Diese Vorrichtung kann als eine Art molekularer Energietrichter beschrieben werden, der die Energie am Reaktionszentrum stark verdichtet (Abb 4). Hinzu kommen mehrere Vorrichtungen, die für eine sehr hohe Effizienz des Energietransfers bei der PS sorgen (nähere Details s. Kasten „Weiterführendes zur Photosynthese“).
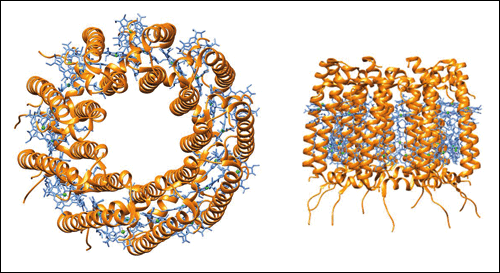
Abb. 4: Durch Röntgenstrukturanalyse erstelltes Modell des LH-2 Komplexes aus phototrophen Bakterien (Frontalansicht und seitliche Ansicht). Chlorophyll-Moleküle sind in Blau dargestellt, Mg2+ in Grün.
Für diese überaus anspruchsvolle Funktion kommen nur sehr komplex aufgebaute Biomakromoleküle in Frage. Nelson & Junge beschreiben die Biosynthese des PS I mit folgenden Worten: „Der Aufbau der PS I umfasst einen sehr komplizierten Biogenese- und Montageprozess, bei dem alle PS I-Komponenten zusammengebracht werden, um die effizienteste photochemische Maschine der Natur zu erzeugen.“
Darüber hinaus ist die Effizienz der Photosynthese empfindlich von der Struktur der beteiligten Photosysteme abhängig. Bei der Beschreibung von Aufbau und Funktion von Photosyntheseapparaten wird sehr oft eine Sprache verwendet, die eine Zielorientierung beschreibt (Teleologie): „Offenbar dienen die Proteine als Gerüst, das die Pigmente in der richtigen Geometrie hält um einen schnellen Energietransfer zu ermöglichen und die Löschung des angeregten Zustands zu verhindern“ (Nelson & Junge 2015).
Es wird deutlich, dass für die Funktionstüchtigkeit der oxygenen Photosynthese ein erstaunlich hohes Maß an struktureller Präzision und Feinabstimmung der Proteine, kombiniert mit dem Vorliegen der richtigen funktionellen Komponenten (Mg2+, Chlorophylle, Mn-Ionen im OEC), gegeben sein muss. Darüber hinaus muss eine sehr breite Spanne des Redoxpotenzials abgedeckt werden – vom Wasser/Sauerstoff (+0,8 V) zum Ferredoxin Fe3+/Fe2+(-0,43 V). Und schließlich müssen die Transmembranproteine derart angeordnet sein, dass das Erzeugen des Protonengradienten möglich ist. Dabei ist zu berücksichtigen, dass eine weniger komplexe Version des oxygenen Photosynthese-Gesamtsystems als sie bei den Cyanobakterien vorliegt, bisher in der Natur nicht vorgefunden worden ist.
Die genannten Sachverhalte müssen alle beim Aufstellen von Hypothesen zur Evolution der oxygenen Photosynthese berücksichtigt werden. Zudem gibt es in der Natur Photosyntheseapparate, die ohne Freisetzung von Sauerstoff funktionieren (anoxygene Photosynthese) und sowohl Ähnlichkeiten als auch Unterschiede zur oxygenen Photosynthese aufweisen. Daher liegt es nahe, beide Typen von Systemen zu vergleichen und die Plausibilität verschiedener Hypothesen im Hinblick auf den Ursprung der Photosynthese zu prüfen.
2 | Weiterführendes zur Photosynthese
Aufbau und Funktion
In der Photosynthese erfolgt insgesamt die Übertragung von Elektronen von Wassermolekülen zu organischen Molekülen, die als Cofaktoren bezeichnet werden. Auf diese Weise werden die Elektronen von einem niedrigeren Energieniveau auf ein höheres gehoben, so dass Lichtenergie in Form von chemischem Potenzial gespeichert wird. Der hierbei resultierende Elektronenfluss wird zudem genutzt, um einen Protonengradienten aufzubauen, der die ATP-Synthase antreibt – die zweite Form der Zwischenspeicherung von Energie.
Der Elektronenfluss beginnt im Photosystem II (PS II), wo zwei Mg2+-Cytochrom-Einheiten (P680), für die sich der Begriff „special pair“ etabliert hat, durch Absorption eines Photons in einen energetisch angeregten Zustand versetzt werden. Anschließend wird ein Elektron vom „special pair“ über einige Zwischenstationen auf ein Chinon übertragen, sodass eine Ladungstrennung resultiert und das special pair nun positiv geladen ist (P680+). Diese positive Ladung wird neutralisiert, indem ein Elektron aus dem Mangan-Komplex entzogen wird, der das Elektron durch Oxidation von Wasser bezieht (oxygen evolving complex, OEC). Läuft dieser Vorgang ein zweites Mal ab, resultiert ein vollständig reduziertes Chinolmolekül. Im PS II läuft also insgesamt eine Elektronenübertragung von Wassermolekülen auf Chinone ab – ein endergoner Vorgang. Das resultierte Chinol diffundiert entlang der Membran und gelangt in den Komplex III (in Cyanobakterien: Cytochrom b6f-Komplex, in Pflanzen Cytochrom-bc1). Hier findet eine stufenweise Oxidation des Chinols zum Chinon statt, wobei die Elektronen wiederum über einige Zwischenstationen auf ein Plastochinon übertragen werden, das später als Elektronenquelle für das Photosystem I (PS I) fungiert. Somit ist der Komplex III eine Art Brücke für den Elektronenfluss von PS II auf PS I.
Im PS I läuft ein ähnlicher Vorgang ab wie im PS II, wobei das elektrochemische Potenzial des gesamten Prozesses deutlich höher liegt. Zunächst wird auch hier ein „special pair“ (P700) durch ein Photon auf einen angeregten Zustand gebracht und es folgt ein Elektronentransfer über eine Reihe an Zwischenstationen zu einem Ferredoxin (Eisen-Schwefel-Protein). Das nach der Ladungstrennung resultierte P700+ wird durch das Plastocyanin reduziert, sodass es erneut für eine Anregung durch Photonen zur Verfügung steht. Insgesamt wird also ein Elektron von einem Plastocyanin auf ein Ferredoxin übertragen – ebenfalls ein endergoner Vorgang. Vom Ferredoxin gelangen die Elektronen dann zum NADP+, wobei für eine vollständige Reduktion des NADP+ zu NADPH zwei Elektronentransfers über den PS I erfolgen müssen.
Zur Effizienz der Photosynthese
Die Quantenausbeute* der photochemischen Prozesse am „special pair“ liegt bei ca. 100% für PS I und 90% für PS II und ist damit für einen photochemischen Vorgang außerordentlich hoch (Croce & van Amerongen 2020). Das liegt daran, dass die Anregung des „special pair“ nur 20 bis 300 Picosekunden (1 ps = 10-12 s) dauert, während die Lebensdauer des angeregten Zustandes im Bereich von Nanosekunden (1 ns = 10-9 s) liegt (Croce & van Amerongen 2020). Aufgrund dieses Verhältnisses ist die Wahrscheinlichkeit einer Übertragung des angeregten Elektrons auf benachbarte Elektronenakzeptoren sehr viel höher als der Rückfall in den Grundzustand. Wichtig hierfür ist, dass das Magnesium-Ion (Mg2+) als komplexiertes Metallion in den Chlorophyllen der Photosysteme vorliegt (Kaim & Schwederski 2005). Dadurch wird ein Übergang in weniger energiereiche Zustände kinetisch gehemmt. Zudem gibt es Vorrichtungen, die einen Rücktransfer des Elektrons zum positiv geladenen „special pair“ nach erfolgter Ladungstrennung verhindern. Schon vor einiger Zeit gelang es Rudolph A. Marcus herauszufinden, dass der Rücktransfer des Elektrons thermodynamisch so überaus günstig ist, dass er im so genannten „invertierten Bereich“ liegt und damit sehr langsam, weil kinetisch gehemmt ist. Für diesen intuitiv schwer nachvollziehbaren Sachverhalt erhielt Marcus 1992 den Nobelpreis für Chemie. Hinzu kommt, dass der dem „special pair“ benachbarte Elektronenakzeptor nur etwa 1 nm entfernt ist, sodass der Elektronentransfer via quantenmechanischem Tunnelvorgang in nur ca. 11 Picosekunden (10-12 s) erfolgt (Stryer et al. 2007). Wäre der Abstand des Elektronenakzeptors zum „special pair“ nur wenige Angström größer, würde die Elektronenübertragung sehr unwahrscheinlich. Insgesamt führen etwa 99% der Photonenabsorptionen im PS I zu einer Ladungstrennung (Nelson & Junge 2015).
Anoxygene Photosynthese
Während die oxygene Photosynthese bei Pflanzen, Algen und Cyanobakterien vorkommt, gibt es auf Chlorophyll basierende anoxygene Photosynthese nur bei Bakterien. Photosysteme (PS), die bei Archaebakterien vorkommen, basieren auf Rhodopsin und sind für den GOE irrelevant, da Rhodopsin-basierte oxygene PS nicht bekannt sind (DasSarma & Schwietermann 2021). Bisher sind bei insgesamt sieben von 30 beschriebenen Bakterienstämmen auf Chlorophyll basierende PS nachgewiesen worden (Zeng et al. 2014): Acidobakterien, Chlorobien, Chloroflexi, Cyanobakterien, Firmicutes, Gemmatimonadetes und Proteobakterien, wobei nur die Cyanobakterien oxygene Photosynthese betreiben. Organismen, die anoxygene Photosynthese betreiben, verwenden andere Elektronenquellen als Wasser – dazu zählen anorganische Verbindungen wie Fe2+, H2, S, HS-, S2O32-, NO2-, AsO33- oder auch organische Moleküle (Fischer et al. 2016). Die Elektronentransportsysteme dieser Organismen weisen in allen Fällen nur ein einziges PS auf, das entweder dem PS I oder dem PS II der oxygenen Photosyntheseapparate ähnelt (Abb. 2B). Ein weiterer wesentlicher Unterschied ist das Fehlen des OEC (oxygen evolving complex) bei Organismen mit anoxygener Photosynthese, da sie keine Wasseroxidation durchführen. In vielen Varianten solcher Systeme verläuft der Elektronentransfer zyklisch: Nach der Anregung des „special pair“ durchläuft ein Elektron mehrere Stationen und gelangt am Ende wiederum zum „special pair“, wobei ein Protonengradient generiert wird, der die ATP-Synthase antreibt. Prinzipiell könnte ein Elektron unendlich oft durch diesen Kreislauf geschickt werden. Da jedoch auch für andere Vorgänge wie z. B. die CO2-Assimilation Elektronen abgeführt werden, müssen weitere Elektronen aus den oben genannten äußeren Quellen aufgenommen werden (Abb. 2B).
Glossar
anoxisch: frei von Sauerstoff. Archaikum: Äon (Zeitalter) auf der geologischen Zeitskala von vor 4000 Millionen radiometrischen Jahren bis vor 2500 Millionen Jahren. ATP: Adenosin-Triphosphat. endergon: Vorgang (z. B. chemische Reaktion), bei dem das chemische Potenzial (Maß für Energieinhalt) des Systems erhöht wird. Energetisch handelt es sich also um einen Bergauf-Vorgang. Solche Vorgänge laufen nicht spontan ab. exergon: Vorgang (z. B. chemische Reaktion), bei dem das chemische Potenzial (Maß für Energieinhalt) des Systems herabgesetzt wird. Energetisch handelt es sich also um einen Bergab-Vorgang. Solche Vorgänge laufen spontan ab. Extinktionskeoffizient: Maß für die Fähigkeit eines Moleküls, Licht zu absorbieren. FADH2: Flavin-Adenin-Dinukleotid-Dihydrid. Gesteinskonvektion: Wärmebewegung von Gestein/Magma, mit der die Plattentektonik zusammenhängt. lateraler Gentransfer: Übertragung genetischer Information über ringförmige DNA, die relativ schnell zwischen Bakterien über rüsselförmige Ausstülpungen (Pili) ausgetauscht werden kann. NADH: Nicotinamidadenindinucleotid-Hydrid. kinetisch gehemmt: chemische Vorgänge laufen bei freiwerdender Energie ab. Allerdings können bestimmte Faktoren die Reaktion erheblich verlangsamen, auch wenn sie nichts mit der Energiebilanz zu tun haben. In solchen spricht man von „kinetischer Hemmung“. Oxidation: Entzug von Elektronen. oxygen (Adj.): Sauerstoff generierend. Photolyse: Spaltung chemischer Bindungen von Molekülen durch Lichtenergie. phototroph: Licht als Energiequelle nutzend. Proterozoikum: Zeitalter auf der geologischen Zeitskala von vor 2500 Millionen radiometrischen Jahren bis vor ca. 540 Millionen radiometrischen Jahren. Quantenausbeute: auch als „Quanteneffizienz“ bezeichnet. Verhältnis zwischen absorbierten Photonen und Elektronen, die vom „special pair“ auf ein benachbartes Chlorophyll übertragen werden. Redoxpotenzial: Maß für die Tendenz eines Moleküls, Elektronen aufzunehmen bzw. abzugeben. vertikaler Gentransfer: Weitergabe genetischer Information durch Fortpflanzung (bei Bakterien: Zellteilung)
Hypothesen zur Evolution der oxygenen Photosynthese
Seit über 80 Jahren wird von vielen Forschern angenommen, dass die oxygene Photosynthese als komplexere Variante moderner ist als die anoxygene. Bereits in den 1930er-Jahren wurde allein aufgrund der Tatsache, dass in der oxygenen Photosynthese vier Photonen für eine vollständige Reaktion verwendet werden – während es in der anoxygenen nur zwei sind – der Schluss gezogen, dass die letztere primitiver sei (Blum 1937). Später wurde diese Auffassung von anderen bestätigt und um zusätzliche Argumente erweitert (Olson 1970). Dazu gehören vor allem die insgesamt größere Komplexität des Aufbaus der oxygenen Photosyntheseapparate und die anspruchsvollen Vorgänge im Zusammenhang mit der Oxidation des Wassers. Cardona (2019) kommentiert die frühen Annahmen aus einer aktuellen Sicht dagegen eher kritisch: „Es sollte beachtet werden, dass diese Idee populär wurde, bevor wir ein vertieftes Verständnis der Photosynthese hatten und lange bevor wir Zugang zu Strukturen von Reaktionszentren hatten, um sie [die Hypothese] zu prüfen.“
Im Hinblick auf eine „Umrüstung“ von einer anoxygenen Photosynthese zur oxygenen durch rein natürliche Vorgänge stellen sich unmittelbar die folgenden Fragen: Wie wurden beide Reaktionszentren in eine Elektronentransportkette integriert und zugleich der Elektronentransfer gekoppelt? Wie kam es zur Bildung des OEC? Wie wurde zugleich mit der Einführung des OEC das elektrochemische Potenzial aller Komponenten des PS II herabgesetzt, damit die Elektronenübertragung vom OEC auf das „special pair“ möglich wird?
Mit der immensen Zunahme an Kenntnissen im Bereich der Molekularbiologie und Genetik ist das Bild jedoch in keiner Weise klarer geworden, sondern deutlich komplizierter: Die Zahl an Hypothesen zur Evolution der oxygenen Photosynthese ist mit der Zeit rapide gewachsen. Dabei treten hauptsächlich zwei konkurrierende Erklärungsmuster auf: 1. Das Modell des selektiven Verlusts; 2. Das Fusions-Modell.
Das erste Modell besagt, dass zunächst Bakterien eine urtümliche Form von PS erworben haben, die hinsichtlich ihrer molekularen Ausstattung eine Art Mischform zwischen PS I und PS II darstellte (Hohmann-Marriot & Blankenship 2011). Anschließend kam es zu einer Genduplikation und es entstanden in einem Organismus zwei unterschiedliche PS. Durch nachträglichen, selektiven Verlust entstanden anoxygene PS, die entweder dem PS I ähnelten oder dem PS II. Im Unterschied zu allen anderen Bakterien behielten die Cyanobakterien beide Photosysteme bei und entwickelten die oxygene Photosynthese. Es wird also davon ausgegangen, dass sich am Anfang ein Organismus mit einem komplexen Photosyntheseapparat entwickelte und zum gemeinsamen Vorfahr aller phototrophen Organismen wurde. Die Vererbung der PS erfolgt in diesem Modell nur über den vertikalen Gentransfer*.
Gemäß dem Fusions-Modell soll es zunächst zur Entstehung eines einzelnen primitiven Photosystems gekommen sein, von dem ausgehend sich die zwei verschiedenen PS I und PS II entwickelten. Anschließend soll es durch lateralen Gentransfer* in umfangreichem Ausmaß zur Integration des PS II in einen Organismus mit bereits vorhandenem PS I gekommen sein. Als Nachweis für eine durch lateralen Gentransfer erfolgte Übertragung eines Photosystems zwischen zwei sehr verschiedenen Bakterienstämmen werden auffällige Ähnlichkeiten der für die Photosysteme codierenden Gencluster zwischen Rubriviax gelatinosus IL 144 (Proteobakterium) und dem zu dem Gemmatimonadeten gehörenden Bakterium AP 64 angeführt (Zeng et al. 2014).
Kritik
Um die erste Hypothese (selektiver Verlust) zu plausibilisieren, müsste zunächst schlüssig aufgezeigt werden, wie sich der komplexe Vorfahr entwickelt haben soll. Besonders schwierig ist es dabei zu erklären, warum und wie sich ein Photosyntheseapparat mit zwei Photosystemen gebildet haben soll, wenn nicht gleichzeitig auch ein OEC mit funktionierender Wasseroxidation und die Kopplung des Elektronenflusses von PS II zu PS I gegeben war. Der Sprung von einer anoxygenen Photosynthese zu einer oxygenen ist viel zu groß, als dass er in wenigen Schritten durch Mutation und Selektion möglich wäre. Es muss also zwingend einen anoxygenen Photosyntheseapparat mit zwei PS als Vorläufer der oxygenen Photosynthese gegeben haben. Die Annahme einer solchen Zwischenstufe ist aber in keiner Weise schlüssig, da solche Systeme nicht bekannt sind und auch nicht plausibel aufgezeigt werden kann, weshalb ein anoxygener Photosyntheseapparat mit zwei Photosystemen entstehen sollte (Cardona 2019). Der bloße Verweis auf eine Genduplikation hilft nicht weiter, da damit nicht gezeigt ist, welchen Selektionsvorteil das Vorliegen zweier Photosysteme für eine anoxygene Photosynthese bietet. Abgesehen davon sind Entstehungen zweier PS durch Genduplikation in einem Organismus nie dokumentiert worden.
Die verbreitete Auffassung, dass die Photosysteme I und II homolog seien, stellt ein Beispiel für ein unbegründetes Festhalten an evolutionstheoretischen Dogmen dar.
Ein weiteres immenses Problem ist der große Unterschied der Proteinsequenzen von PS I und PS II (nur etwa 10% Übereinstimmung gemäß Fischer et al. 2016). Auch wenn die beiden Proteinkomplexe hinsichtlich ihrer räumlichen Anordnung ähnlich sind, ist die Annahme einer Entstehung von PS I und PS II durch Genduplikation angesichts ihres enormen Sequenzunterschieds nicht überzeugend. Es ist vor diesem Hintergrund erstaunlich, dass diese Proteinkomplexe von vielen Wissenschaftlern dennoch für homolog gehalten werden. Zitate wie das folgende sind in der Literatur keine Seltenheit und bezeugen ein Festhalten an evolutionstheoretischen Dogmen, das mit den Befunden in einem offenkundigen Konflikt steht (Sousa et al. 2013): „Obwohl auf Sequenzebene fast keine Ähnlichkeit zwischen RCI [PS I]und RCII [PS II] feststellbar ist, sind die Anordnungen ihrer Struktur und Kofaktoren zweifellos homolog und weisen eindeutig auf eine gemeinsame Abstammung hin“ (Hervorhebung hinzugefügt).
Im Fusionsmodell wird eine stetig wachsende Komplexität der Photosynthese ausgehend von einem einfacheren Vorläufer angenommen, wie in Evolutionstheorien üblich. Doch auch hier ist es notwendig, genau zu erklären, wie eine plausible „primitive“ Ausgangsversion der Photosynthese ausgesehen haben könnte. Da es jedoch in der Natur keine „primitiven“ Photosyntheseapparate gibt, könnten höchstens hypothetische Modelle einfacher Vorläufer entworfen werden – im Hinblick auf die Komplexität und die ausgefeilten internen Abstimmungen von Photosyntheseapparaten erscheint dieses Unterfangen aussichtslos.
Die Beschaffenheit der Photosyntheseapparate und ihre Verteilung in den Domänen des Lebens sind ein weiteres eindrückliches Zeugnis für das Werk des Schöpfers.
Ein weiteres Kernproblem der Fusionshypothese ist die Unzulänglichkeit des lateralen Gentransfers für die Übertragung derart großer genetischer Module wie derjenigen der Photosynthese. Wie bereits zuvor erwähnt, sind Photosysteme außerordentlich anspruchsvoll gebaute Proteinmaschinen, die durch eine Vielzahl von Genen codiert sind. Daher ist es nicht überraschend, dass eine Beobachtung einer solchen Übertragung eines ganzen genetischen Moduls bisher nie gemacht worden ist. Der angeblich gesicherte Transfer eines kompletten Photosynthese-Genmoduls wurde nicht tatsächlich beobachtet, sondern aus dem Vergleich der entsprechenden Gencluster des Proteobakteriums Rubriviax gelatinosus IL 144 und dem Gemmatimonatenden AP 64 gefolgert (Zeng et al. 2014). Aber auch wenn es sich tatsächlich um einen früher erfolgten Transfer handeln sollte, wäre das ein Beispiel für die Übertragung des genetischen Moduls eines PS zu einem Organismus, der vorher gar kein PS besaß. Hinweise für denkbare Übertragungen genetischer Elemente von PS zu bereits phototrophen Organismen sind dagegen unbekannt. Genau das wäre aber für die Entwicklung eines oxygenen Photosyntheseapparats mit zwei PS nötig. Außerdem gibt es bisher keine Veröffentlichungen, die plausibel aufzeigen, durch welche konkreten Schritte es zu einer Integration eines nachträglich eingeführten PS II inklusive eines OEC hätte kommen können. Auch sieht es bisher nicht danach aus, dass die notwendige Kopplung des Elektronenflusses von PS II über den Komplex III zum PS I durch schrittweise Mutation und Selektion erklärt werden könnte.
Eine generell kritische Sicht auf beide Modelle vertritt Tanai Cardona (2019): „Ehrlich gesagt stimmen Beobachtungen aus der Natur nicht mit den Erwartungen aus den gegenwärtigen Modellen für die Evolution der Photosynthese überein.“ Er schlägt als „einzigen Weg aus dem Paradox“ vor, dass die „Erfindung“ der Oxidation von Wasser der Auslöser der Evolution der zwei verschiedenen Photosysteme (PS I und PS II) gewesen sein könnte, ohne jedoch auch nur ansatzweise einen plausiblen Mechanismus anzuführen.
Darüber hinaus ist die Entstehung von Photosystemen in einer sauerstofffreien Atmosphäre grundsätzlich unplausibel, da es ein bleibendes Rätsel ist, wie sich hochempfindliche Lichtsammelkomplexe in Abwesenheit einer Ozonschicht hätten entwickeln können. Durch hartes UV-Licht werden Chlorophylle sofort zerstört, während sie in von Licht abgeschirmten Gebieten unbrauchbar sind.
Photosynthese als Schöpfungsindiz
Die hochgradige Effizienz der Photosynthese beruht auf einem überaus präzisen und komplexen Aufbau der Photosyntheseapparate. Jedes Teil ist für die jeweilige Art der Photosynthese notwendig. Geringe Abweichungen um wenige Angström von der räumlichen Anordnung der Komponenten des Lichtsammelkomplexes würden das ganze System funktionsuntüchtig machen, da die unverzichtbaren Quantentunnel-Prozesse nur auf sehr kurzen Distanzen funktionieren. Es ist zudem auffällig, dass die Verteilung der Phototrophie in den Stämmen der Lebewesen in keiner Weise monophyletisch ist (Fischer et al. 2016; Martin et al. 2018). Das heißt: Eine Rückführung auf einen gemeinsamen Vorfahren aller phototrophen Organismen ist nicht möglich. Vielmehr sieht es so aus, als ob diese Eigenschaft in der Organismenwelt gezielt verteilt worden wäre. Sowohl die Beschaffenheit der Photosyntheseapparate als auch ihre Verteilung unter den Lebewesen sprechen klar für Schöpfung als Ursache ihrer Entstehung.
Fazit
Insgesamt sieht es nicht danach aus, dass die Herkunft des molekularen Sauerstoffs in der Erdatmosphäre im Sinne eines GOE durch rein natürliche Ursachen schlüssig erklärt werden könnte. Viel eher sind aus der Beschaffenheit phototropher Organismen und ihrer Verteilung in den Domänen des Lebens und der besonderen Zusammensetzung der Erdatmosphäre deutliche Anzeichen von Schöpfung zu erkennen.
Abgesehen von dem Fehlen plausibler Ursachen für eine „Sauerstoffkatastrophe“ müsste auch erklärt werden, wie eine sauerstofffreie Lebenswelt auf die vermutete Anreicherung mit O2 reagiert haben könnte – es ist allgemein bekannt, dass Sauerstoff nicht nur chemisch sehr reaktiv ist, sondern auch zur Bildung schädlicher Nebenprodukte neigt. Diese Fragestellung soll in der nächsten Folge zum Thema „Sauerstoffkatastrophe“ erörtert werden.
A whiff of oxygen before the great oxidation event? Science 317, 1903–1906.
Large oxygen excess in the primitive mantle could be the source of the Great Oxygenation Event. Geochem. Persp. Lett. 6, doi:10.7185/ geochemlet.1801.
Stryer Biochemie. Spektrum Akademischer Verlag, München, 6. Auflage.
On the evolution of photosynthesis. Am. Nat. 71, 350–362.
Thinking twice about the evolution of photosynthesis. Open Biol. 9: 180246.
Three body photodissociation of the water molecule and its implications for prebiotic oxygen production. Nat. Commun. 12, https://doi.org/10.1038/s41467-021-22824-7.
Light harvesting in oxygenic photosynthesis: structural biology meets spectroscopy. Science 369, doi:10.1126/science.aay2058.
Early evolution of purple retinal pigments on earth and implications for exoplanet biosignatures. Int. J. Astrobiol. 20, 241–250.
Evolution of oxygenic photosynthesis. Annu. Rev. Earth Planet. Sci. 44, 647–683.
Experimental evidence for the existence of iron-rich metal in the earth’s lower mantle. Nature 428, 409–412.
Evolution of Photosynthesis. Annu. Rev. Plant Biol. 62, 515–548.
Bioanorganische Chemie – zur Funktion chemischer Elemente in Lebensprozessen. Teubner Verlag, Wiesbaden, 4. Auflage.
The timetable of evolution. Sci. Adv. 3, e1603076.
Evidence for direct molecular oxygen production in CO2 photodissociation. Science, 346, 61-64.
The rise of oxygen in Earth’s early ocean and atmosphere. Nature 506, 307–315.Martin WF, Bryant DA & Beatty JT (2018) A physiological perspective on the origin and evolution of photosynthesis. FEMS Microbiol. Rev. 42, 205–231.
Structure and energy transfer in photosystems of oxygenic synthesis. Annu. Rev. Biochem. 84, 659–683.
Die „Sauerstoffkatastrophe“. Stud. Integr. J. 28, 13–19.
Chlorophyll biosynthesis gene evolution indicates photosystem gene duplication, not photosystem merger, at the origin of oxygenic photosynthesis. Genome Biol. Evol. 5, 200–216.
Dynamic molecular oxygen production in cometary comae. Nat. Commun. 8, 15298.
Functional type 2 photosynthetic reaction centers found in the rare bacterial phylum Gemmatimonadetes. PNAS 111, 7795–7800.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 11/23/21
Webmaster