Themen • Kurzbeiträge • Streiflichter
Cystein: eine besondere Aminosäure – auch im Hinblick auf Ursprungsfragen
von Boris Schmidtgall
Studium Integrale Journal
28. Jahrgang / Heft 1 - April 2021
Seite 48 - 52
Zusammenfassung: Cystein ist neben Methionin die zweite schwefelhaltige, proteinogene* Aminosäure. In vielen Organismen erfolgt die Einführung des unverzichtbaren Elements Schwefel in andere Biomoleküle über das Cystein. Es erscheint undenkbar, dass Organismen ohne Cystein überhaupt lebensfähig sein könnten. Powner et al. haben kürzlich versucht, durch chemische Experimente die präbiotische* Entstehung des Cysteins und kleiner Peptide zu plausibilisieren. Handelt es sich um eine belastbare Hypothese zur Entstehung der Biochemie des Schwefels?
• • • • • • • •
Einführung

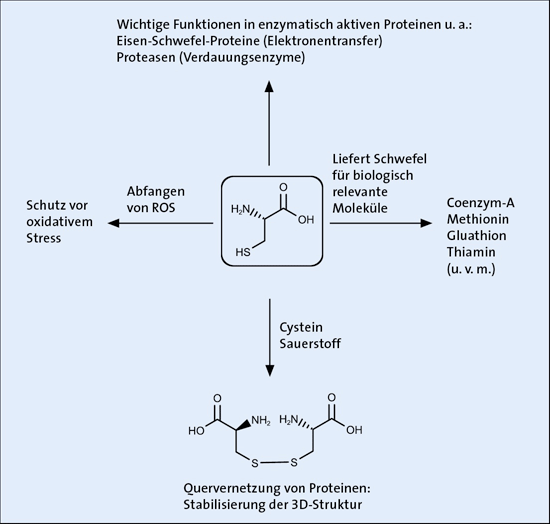
Abb. 1: Schematische Übersicht zu den Funktionen der Aminosäure Cystein in Organismen. Bei ROS (reactive oxygen species) handelt es sich um verschiedene Abbauprodukte des Sauerstoffs (Sauerstoffradikale), die sehr reaktiv sind und daher das Gewebe schädigen, wenn sie nicht abgefangen werden.
Leben ist uns nur in einer hochgradig komplexen Form bekannt. Hinweise auf einfachere Lebensformen als Bakterien gibt es bisher nicht. Von den vielen molekularen Komponenten, die von Anfang an für Leben erforderlich sind, gehören die 20 kanonischen* Aminosäuren zu den wichtigsten. Aus diesen kleinen organischen Molekülen sind die Proteine aufgebaut, die einen wichtigen Bestandteil des Gewebes vieler höherer Lebewesen darstellen. Darüber hinaus katalysieren* als Enzyme bezeichnete Proteine den Stoffwechsel aller Organismen.
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.
Eine besondere Rolle kommt hierbei der Aminosäure Cystein zu, deren Seitengruppe als Thiol-Gruppe bezeichnet wird (Abb. 1). Diese molekulare Einheit ermöglicht verschiedene chemische Reaktionen (Elektronenübertragungsreaktionen, Säure-Base-Reaktionen, nukleophile Substitutionen), weswegen Cystein ein wichtiger Bestandteil vieler enzymatisch aktiver Proteine ist (u. a. Eisen-Schwefel-Proteine und Proteasen). Zudem besitzt Cystein die einzigartige Eigenschaft, mit seinesgleichen über die Seitengruppe Bindungen zu knüpfen. Diese Verknüpfungen werden als Disulfidbrücken bezeichnet und stellen bei vielen Proteinen eine wichtige Komponente der Stabilisierung der dreidimensionalen Struktur dar (ohne diese funktionieren Proteine nicht). Darüber hinaus liefert das Cystein in vielen Organismen das Element Schwefel für den Aufbau vieler biologisch relevanter Moleküle wie Coenzym-A, Methionin, Glutathion und Thiamin (Romero et al. 2014; Jurgenson et al. 2009). Außerdem fungieren Cystein-haltige Proteine als Antioxidantien*, indem sie reaktive Sauerstoff-Verbindungen (ROS, reactive oxygen species) neutralisieren, wodurch Gewebeschäden verhindert werden (Stadtman & Levine 2003).
Das Cystein erfüllt also zugleich mehrere unverzichtbare Funktionen in der Biokatalyse (Enzyme und Cofaktoren), dem Aufbau von Proteinen und der Synthese anderer Biomoleküle. Ohne Cystein wären sehr viele Proteine funktionsunfähig oder instabil. In Pflanzen, Bakterien und einigen Protozoen wird Cystein ausgehend von Serin, einer anderen Aminosäure, synthetisiert, während die Cystein-Synthese in Säugetieren und Pilzen ausgehend vom Methionin beginnt (Romero et al. 2014; Birke et al. 2012). Bei diesen Synthesen sind jedoch stets Enzyme beteiligt, die wiederum selbst Cystein enthalten - ein weiteres Henne-Ei Problem bezüglich des Ursprungs von Lebewesen (Fujishima et al. 2018). Die angeführten Sachverhalte legen nahe, dass das Cystein von Anfang an ein Teil des molekularen Baukastens der Lebewesen war.
Naturalistische Hypothesen zum Ursprung des Cysteins
Im Gegensatz dazu wurde im Rahmen von naturalistischen Hypothesen zum Lebensursprung lange Zeit angenommen, dass zunächst ein reduzierter Satz von Aminosäuren zur Verfügung stand. Cystein soll demnach nicht durch chemische Vorgänge bereits vor der Existenz erster Lebewesen entstanden sein, sondern erst später im Laufe der Evolution von Organismen. Begründet wurde dies zum einen damit, dass Cystein relativ leicht verschiedene chemische Reaktionen eingeht (s. o.) – damit wäre es in einem noch wenig geordneten chemischen System, wie die präbiotische Welt es gewesen sein soll, nicht beständig. Zum anderen wurde bisher keine plausible Erklärung dafür gefunden, wie Cystein durch ungesteuerte Prozesse synthetisiert worden sein könnte. Bisherige chemische Versuche, die ein denkbares Szenario der Entstehung dieses Moleküls über eine Strecker-Synthese1 nachstellen sollten, resultierten in komplexen Gemischen (Foden et al. 2020, Abb. 2). Auch bei Ursuppen-Simulationsexperimenten nach Miller konnte Cystein höchstens in Spuren im Reaktionsgemisch nachgewiesen werden (Zaia et al. 2008).
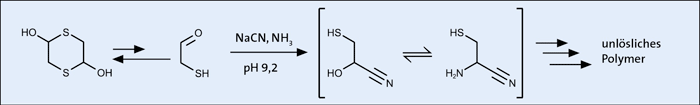
Abb. 2: Gescheiterter Versuch der Cystein-Synthese über die Strecker-Synthese (NaCN: Natriumcyanid; NH3: Ammoniak)
Allerdings ist die Annahme des späteren Hinzukommens von Cystein durch dessen Biosynthese im Verlauf der Evolution ebenfalls kaum denkbar, da in diesem Falle der genetische Code neu programmiert werden müsste – ein äußerst aufwändiger Vorgang für den bisher nichts spricht. Im Fall von Cystein als neu hinzugefügter Aminosäure wären außerdem die damit einhergehenden strukturellen Änderungen der Proteine besonders gravierend, da Cystein als einzige Aminosäure die dreidimensionale Struktur von Proteinen durch Knüpfen von Disulfidbrücken unterstützt bzw. stabilisiert (s. o.).
Cystein und Methionin sind systemrelevante Aminosäuren. Sie durften niemals fehlen noch konnten sie irgendwann neu hinzukommen.
Erschwerend kommt hinzu, dass ohne Cystein auch das Methionin fehlen würde, da Methionin in vielen Organismen biosynthetisch ausgehend von Cystein erzeugt wird. Dies ist ein weiteres gravierendes Problem, da Methionin bei der Proteinbiosynthese stets am Anfang der Aminosäuresequenz steht und damit das Startsignal für die Synthese von Proteinen darstellt. Es müsste folglich erklärt werden, wie der Start der Proteinsynthese vor dem Vorhandensein von Methionin reguliert wurde und wie eine Neudefinierung des Startsignals durch ungerichtete chemische Vorgänge ablaufen konnte. Insgesamt wird also deutlich, dass sowohl Cystein als auch Methionin in allen Organismen systemrelevante Aminosäuren sind. Sowohl ihr Fehlen bei den ersten Organismen als auch ein späteres Hinzukommen durch evolutive Vorgänge erscheinen unmöglich.
Glossar
Abiogenetisch, Abiogenese: Entstehung ohne Beteiligung von Lebewesen. Antioxidantien: Chemische Verbindungen, die leicht mit Sauerstoff oder dessen Abbauprodukten reagieren und daher deren potenziell schädliche Reaktionen im Organismus verhindern. demineralisiert: von Salzen (Mineralien) befreit. Enantiomere: Moleküle, die sich zueinander wie Bild und Spiegelbild verhalten. Homochiralität: In der Natur vorkommende molekulare Bausteine weisen eine streng einheitliche Geometrie auf (z. B. nur L-Aminosäuren oder nur D-Zucker). Dabei ist unter Voraussetzung rein chemischer Entstehungsvorgänge die Wahrscheinlichkeit, dass diese Moleküle in der spiegelbildlichen Form auftreten (d. h. D- und L-Aminosäuren oder D- und L-Zucker), gleich groß. kanonisch: zu einem bestimmten Satz gehörig. In Bezug auf die Aminosäuren bedeutet diese Bezeichnung, dass sie zum Satz der 20 Aminosäuren gehören, die in Organismen vorkommen. katalysieren: eine chemische Reaktion beschleunigen. präbiotisch: vor der Existenz von Organismen. proteinogen: Aminosäuren, aus denen Proteine zusammengebaut sind, werden als „proteinogene“ Aminosäuren bezeichnet. racemisch: Ein 1:1-Gemisch aus zwei Enantiomeren* wird als Racemat oder racemisches Gemisch bezeichnet. stereoselektiv: Eine chemische Reaktion wird als „stereoselektiv“ bezeichnet, wenn bei Vorhandensein mehrerer geometrisch verschiedener möglicher Reaktionsprodukte eines in bedeutendem Überschuss vorliegt.
Motivation und Syntheseplanung der Forschungsgruppe Foden et al.
Diese Problemstellung motivierte die Forschungsgruppe um Matthew W. Powner (Foden et al. 2020) an der Universität London dazu, eine neue präbiotische* Synthese von Cystein-haltigen Peptiden auszuprobieren. Auf diese Weise beabsichtigten sie, die Hypothese zu untermauern, dass Cystein sehr wohl im Zuge präbiotischer Vorgänge entstanden sein könnte. Dabei orientierten sie sich an der Biosynthese von Cystein, wie sie gegenwärtig in einigen Lebewesen (z. B. Pflanzen, Bakterien) abläuft. Hierbei handelt es sich allerdings um einen anspruchsvollen chemischen Vorgang, der über mehrere Schritte unter Beteiligung zweier komplexer Enzyme verläuft (Serin-Acetyltransferase und O-Acetylserin Sulfhydrase, s. Abb. 3). Wie derzeit üblich, gehen Foden et al. von der nicht weiter begründeten Annahme aus, dass komplexe Enzyme das Resultat bisher unbekannter evolutiver Prozesse sind: „[…] doch moderne Enzyme sind das Produkt einer Milliarden Jahre langen Evolution.“2 Demnach können solche Enzyme nicht in einer präbiotischen Welt existiert haben, sodass die ersten Bausteine der Lebewesen ohne ihre Beteiligung entstanden sein müssten.
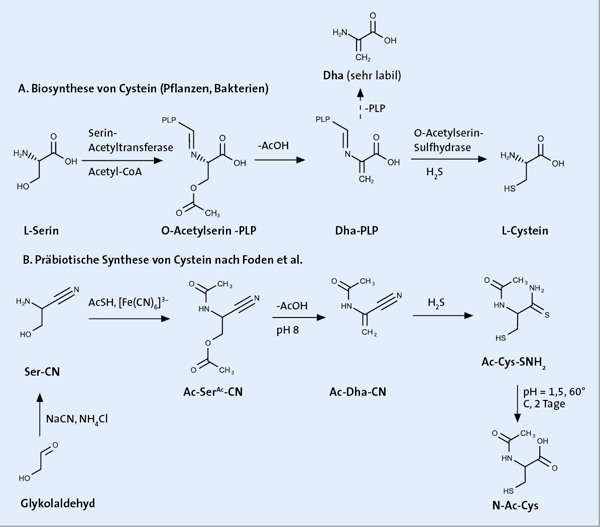
Abb. 3: A Biosynthese des Cysteins, wie sie in Pflanzen und Bakterien abläuft. Als Ausgangsverbindung wird Serin, eine andere Aminosäure, verwendet. Zunächst wird durch das Enzym Serin-Acetyltransferase eine Acetylgruppe an der Seitengruppe des Serins angebracht. Die Acetylgruppe wird dabei von Acetyl-Coenzym-A auf das Serin übertragen. Im darauf folgenden Schritt findet eine Eliminierung eines Acetat-Moleküls und nachfolgende Addition von Schwefelwasserstoff unter Katalyse durch O-Acetylserin-Sulfhydrase statt, sodass die Acetatgruppe durch eine Hydrogensulfid-Gruppe ersetzt wird und schließlich L-Cystein erhalten wird.
B Als „präbiotisch“ bezeichnete Laborsynthese des Cysteins nach Foden et al. Im ersten Schritt wird ausgehend von Glykolaldehyd über eine Strecker-Reaktion mit Natriumcyanid und Ammoniumchlorid das Nitril Ser-CN erhalten, welches durch Reaktion mit Thioacetat sowohl an der Aminogruppe als auch an der Hydroxygruppe acetyliert wird. Aus diesem Molekül spaltet sich bei pH 8 langsam Essigsäure ab. Anschließend kann das resultierte Ac-Dha-CN mit Schwefelwasserstoff zur Reaktion gebracht werden, sodass sich Ac-Cys-CNH2 bildet.
Dieser Sachverhalt verweist auf die weiterführende Frage nach der Entstehung der ersten Proteine. Dazu ist die Verknüpfung einzelner Aminosäuren zu Kettenmolekülen vonnöten – ein Vorgang, der in heute bekannten Organismen ebenfalls von komplexen Enzymen bewirkt und katalysiert wird. Auch dafür suchten Foden et al. einen Lösungsansatz, indem sie das Potenzial des Cysteins und anderer Thiol-Verbindungen als Organokatalysatoren in der Knüpfung von Peptidketten untersuchten.
Um solche Synthesen ohne Beteiligung von Enzymen zu verwirklichen, sodass sie als „präbiotisch“ gelten können, mussten bereits im Voraus einige absehbare Probleme gelöst werden. Aus der Arbeit von Foden et al. geht deutlich hervor, dass die Autoren sich gründlich Gedanken gemacht haben, wie die „präbiotische“ Synthese zum gewünschten Ziel gebracht werden kann. Ein zentrales Problem ist die Tatsache, dass die Vorstufen des Cysteins im Verlauf der kompletten Biosynthese an den Cofaktor Pyridoxalphosphat (PLP) gebunden bleiben. Bei einer Abspaltung einer der Vorstufen würde sich das überaus labile Dehydroalanin (Dha) bilden, das dann durch schnelle Zersetzung verlorenginge. Daher wählten Foden et al. als Schlüsselverbindung für ihre präbiotische Cystein-Synthese N,O-Diacetylserin-Nitril (Ac-SerAc-CN, Abb. 3). Diese chemische Verbindung ist deutlich stabiler als die biologische Zwischenstufe Dha, geht eine Vielzahl an unerwünschten Reaktionen nicht ein und ermöglicht zugleich andere Reaktionen, die zum Syntheseziel Cystein führen können. Entscheidend ist, dass Ac-SerAc-CN bei einem milden pH-Wert 8 in wässriger Lösung zu Acetyl-Dha-Nitril (Ac-Dha-CN) reagiert (unter Abspaltung eines Essigsäure-Moleküls), das im nächsten Schritt durch Reaktion mit Schwefelwasserstoff N-Acetyl-Cystein ergibt. Die Autoren beschreiben ihren Ansatz vielsagend als „einfache biomimetische Strategie für die präbiotische […] Cystein-Synthese“3 (Hervorhebung hinzugefügt). Die Notwendigkeit gründlicher strategischer Überlegungen zur enzymfreien Synthese von Cystein widerspricht jedoch dem Ansatz, nur ungerichtete chemische Vorgänge als Ursache für die Entstehung dieses Moleküls zuzulassen.
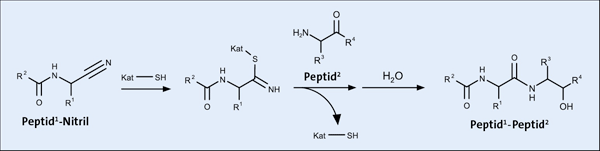
Abb. 4: Kupplung eines Peptid-Nitrils mit einem Peptid unter Katalyse durch ein Thiol (Kat-SH). Vorgehensweise zur Synthese des Cysteins und der Peptide
Als Ausgangsverbindung für die präbiotische Synthese von Cystein wurde Glykolaldehyd gewählt. Durch Strecker-Reaktion mit Natriumcyanid und Ammoniumchlorid in wässriger Lösung wurde daraus Ser-CN erhalten, das durch Reaktion mit Thioessigsäure in Gegenwart von Kaliumhexacyanoferrat(III) zur zweifach acetylierten Verbindung Ac-SerAc-CN umgesetzt wurde. Dieses labile Molekül wandelte sich bei pH 8 langsam zu Ac-Dha-CN um, das dann mit Schwefelwasserstoff zu Acetyl-Cys-SNH2 reagierte. Schließlich wurde durch Erhitzen von Acetyl-Cys-SNH2 in saurer wässriger Lösung (pH 1,5) die Abspaltung der Acetyl-Schutzgruppe und Umwandlung zu N-Acetyl-Cystein bewirkt (Abb. 3). In weiteren Versuchsreihen wurden Kupplungsreaktionen verschiedener Aminosäuren mit Ac-Gly-CN unter Katalyse mittels N-Acetyl-Cystein durchgeführt und verschiedene Katalysatoren für die Peptidkupplung zwischen verschiedenen Di- und Tripeptiden eingesetzt (Abb. 4).
Kritik
Wahl der Chemikalien und Reaktionsbedingungen. Alle von Foden et al. beschriebenen chemischen Reaktionen wurden mit kommerziell erhältlichen chemischen Reagenzien in der üblich hohen Reinheit durchgeführt, wobei demineralisiertes* Wasser als Lösungsmittel diente. Reaktionen mehrstufiger Synthesen wurden isoliert durchgeführt und nicht als Eintopf-Reaktion, wie es in einem realistischen präbiotischen Szenario zu erwarten wäre. Einige dieser Reaktionen wurden unter Argon-Schutzgas durchgeführt, da sie offenbar gegenüber Sauerstoff sehr empfindlich sind (Ac-Dha-CN zu Ac-Cys-SNH2). Zur Aufreinigung einiger Reaktionsprodukte wurden Laboroperationen angewendet, die nicht einmal im Entferntesten natürlichen Bedingungen nahe kommen (Ausschütteln mit reinem Methanol, Gefriertrocknen, Säulenchromatographie).
Genaues Einstellen von Reaktionsparametern. Die Konzentrationen der chemischen Verbindungen in den Reaktionslösungen waren z. T. außerordentlich hoch (bis zu 1 M!). Bei vielen Reaktionen wurde der pH-Wert auf einen sehr genauen Wert eingestellt, damit die Reaktion ablaufen kann (z. B. pH 9,2 bei der Synthese von Ser-CN). Hier wäre es von Interesse gewesen, in welchem Ausmaß die jeweiligen Reaktionen auf Schwankungen der Konzentration bzw. des pH-Werts reagiert hätten. Allein schon diese Sachverhalte reichen aus, um die Behauptung, es handele sich hier um Simulationen möglicher präbiotischer Vorgänge, ad absurdum zu führen – zumal nicht geprüft bzw. nicht dokumentiert wurde, wie empfindlich die Reaktionsverläufe auf störende chemische Verbindungen oder schwankende Parameter reagieren. Solche Kontrollexperimente wären jedoch zwingend nötig, da chemische Robustheit eine notwendige Eigenschaft für ein präbiotisches chemisches System darstellt.
Problematische Schutzgruppenstrategie. Ein unverzichtbarer Teil der als präbiotisch bezeichneten Synthesestrategie waren Acetyl-Schutzgruppen. Um diese Schutzgruppen an den chemischen Verbindungen der Wahl einzuführen, wurde Thioessigsäure verwendet – eine Verbindung, die selbst in kalter wässriger Lösung nur kurzfristig beständig ist und vor allem bei höheren Temperaturen schnell mit Wasser unter Bildung von Essigsäure reagiert (Hipkin & Satchell 1965). Im Rahmen des Transports für kommerzielle Zwecke wird Thioessigsäure üblicherweise durch Zusatz von Chloressigsäure stabilisiert, damit diese Verbindung bei 50° C ca. 1-2 Monate stabil bleibt. Aufgrund ihrer ausgeprägten Labilität würde Thioessigsäure also nicht unter präbiotischen Bedingungen vorkommen können.
Nicht weniger problematisch als die Einführung der Acetylgruppe ist deren abschließende Abspaltung. Diese Reaktion gelingt nur bei relativ unnatürlichen Bedingungen: zwei Tage bei 60°C und pH 1,5. Da andere Reaktionen der von Foden et al. gewählten Abfolge bei mild-alkalischem pH-Wert von 9,2 verlaufen, müsste erklärt werden, wie unter geologischen Bedingungen eine solche Schwankung um knapp 8 pH-Einheiten sich zeitlich passend zur Reaktionsabfolge ereignen könnte. Im Übrigen wurde von den Forschern an keiner Stelle mitgeteilt, dass die vollständige Abspaltung der Acetyl-Schutzgruppen des Cysteins tatsächlich erfolgt ist. Die Synthese ist nur bis zum N-Acetyl-Cystein geführt worden. Daher ist es auch nicht angebracht, von einer „präbiotischen Cystein-Synthese“ zu sprechen, wie dies an verschiedenen Stellen in der Arbeit von Foden et al. getan wurde.
Fazit
Es zeigt sich insgesamt, dass die Synthese der Aminosäure Cystein, wie sie von Foden et al. konzipiert und durchgeführt worden ist, keineswegs als mögliche Erklärung für die erstmalige Entstehung des Cysteins angeführt werden kann. Vielmehr handelt es sich um eine intelligent geplante und sorgfältig durchgeführte chemische Synthese, die in keiner Weise die Bezeichnung als „präbiotische Synthese“ verdient. Zudem ist das eigentliche Produkt der Synthese von Foden et al. gar nicht das Cystein, sondern N-Acetyl-Cystein, da in der Arbeit nirgends gezeigt worden ist, wie die letzte Acetylgruppe abgespalten wurde. Es ist auch aus diesem Grund irreführend, die Synthese als „präbiotische Cystein-Synthese“ zu bezeichnen. Auch für die katalytische Peptidkupplung von Ac-Gly-CN mit Glycin oder andere Peptidkupplungsreaktionen mussten mehrere Parameter zugleich genau eingestellt sein, damit die Reaktion abläuft (pH-Wert, Konzentrationen der Substrate und des Katalysators). Bei den Peptidkupplungen handelte es sich um isoliert durchgeführte Reaktionen und nicht um spontan ablaufende Polymerisations-Kettenreaktionen, die 20 oder mehr Aminosäuren über die für Proteine typischen Peptidbindungen verknüpfen würden.
Die Arbeit gibt somit keinen Aufschluss darüber, wie es unter annähernd natürlichen Bedingungen zur Entstehung von Proteinen hätte kommen können. Außerdem sind alle Produkte (Aminosäuren, Peptide) in racemischer* Form erhalten worden, da die Reaktionen in keiner Weise stereoselektiv* waren. Das grundlegende Problem der Homochiralität* von Aminosäuren und anderen Biomolekülen stellt sich auch hier als unüberwindbares Problem für eine schrittweise natürliche Lebensentstehung dar.
Die Cystein-Synthese von Foden et al. ist intelligent geplant und kann nicht als „präbiotische Synthese“ gelten.
Darüber hinaus stellen sich weiterführende Fragen im Hinblick auf die Entstehung biochemischer Systeme überhaupt. Foden et al. spekulieren in ihrem Artikel, dass „[…] Nitrile als frühe Energiewährung auf der präbiotischen Erde dienten.“4 Hier ist allerdings zu bedenken, dass es dann in der Naturgeschichte zu einer Umstellung von der Energiewährung der Nitrile auf ATP* hätte kommen müssen mitsamt den entsprechenden Änderungen bei allen biochemischen Energieverwertern – ein völlig absurdes Szenario, für dessen Möglichkeit es nicht den geringsten Hinweis gibt.
Die Arbeit von Foden et al. ist aus chemischer Sicht durchaus sehr interessant. Aber wie auch andere präbiotische Experimente zeigt sie keinen Weg eines natürlichen Lebensursprungs auf – im Gegenteil: Es wird einmal mehr deutlich, dass ausgefeilte Versuchsplanung erforderlich ist; damit unterstreicht sie unbeabsichtigt die Plausibilität von Schöpfung.
1 Die Reaktion eines Aldehyds mit einem Amin und Blausäure ergibt ein Aminosäurederivat und wird als „Strecker-Synthese“ bezeichnet
2 „… but modern enzymes are a product of billions of years of evolution. …“
3 „… presents a simple biomimetic strategy for prebiotic Dha synthesis, and we identified N,O-diacetyl-serine nitrile (Ac-SerAC-CN) as a key intermediate for prebiotic cysteine synthesis.“
4 „… in which nitriles served as an early energy currency on the primordial Earth, perhaps acting as a forerunner to adenosine 5-triphosphate and thioesters that drive reactions in extant biology.“
Cysteine biosynthesis, in concert with a novel mechanism, contributes to sulfide detoxification in mitochondria of Arabidopsis thaliana. Biochem. J. 445, doi:10.1042/BJ20120038.
Prebiotic synthesis of cysteine peptides that catalyze peptide ligation in neutral water. Science 370, 865–869.
Reconstruction of cysteine biosynthesis using engineered cysteine-free enzymes. Scientific Reports 8 (12), 1776.
The spontaneous and acid-catalyzed hydrolysis of thiocarboxylic acids. Tetrahedron 21, 835–842.
The structural and biochemical foundations of thiamin biosynthesis. Annu. Rev. Biochem. 78, 569–603.
Transsulfuration is an active pathway for cysteine biosynthesis in Trypanosoma rangeli. Parasites & Vectors 7, 197–208.
Free radical-mediated oxidation of free amino acids and amino acid residues in proteins. Amino Acids 25, 207–218.
Which Amino Acids Should Be Used in Prebiotic Chemistry Studies? Orig. Life Evol. Biosph. 38, 469–488.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 7/2/21
Webmaster