
Themen • Kurzbeiträge • Streiflichter
Mendel’sche Artbildung und die Entstehung der Arten
3. Fortpflanzungsisolation und adaptive Radiationen
1. Woher kommt die Artenvielfalt?
2. Latente Information und präexistente genetische Programme
von Nigel Crompton
Studium Integrale Journal
27. Jahrgang / Heft 2 - Oktober 2020
Seite 78 - 87
Zusammenfassung: Mendels Gesetz der exponentiellen Kombinationen von Merkmalsausprägungen erklärt die Ausprägung einer großen Artenvielfalt innerhalb genetischer Familien auf der Basis präexistenter Programme. Wie aber kommt es zu Fortpflanzungsisolation und zur Entstehung von Arten? Können in der Natur vorkommende Beispiele adaptiver Radiationen mit Mendels Konzept erklärt werden?
• • • • • •
Einführung
In den ersten beiden Teilen unserer Serie wurde gezeigt, dass die Lebewesen ein enormes latentes (verborgenes) Potenzial an genetischer Information besitzen und wie die angelegten Variationsprogramme im Laufe der Generationen zur Ausprägung kommen können. Dieses Variationspotenzial ermöglicht vielfältige Merkmalskombinationen innerhalb einer genetischen Familie (Grundtypen). Wie aber können aus dieser Vielfalt verschiedene abgegrenzte Arten entstehen? Wie kommt es zur Fortpflanzungsisolation und damit zur Artbildung*? Und welche Beispiele gibt es in der Natur, die dynamische Artbildung und Fortpflanzungsisolation belegen?
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.

Introbild: Der Riesen-Säbelschnabel-Nukupu‘u (Hemignathus vorpalis) gehört den Kleidervögeln. Diese Vogelgruppe hat auf den Hawaii-Inseln eine umfangreiche Radiation durchlaufen. Der Gattungsname Hemignathus bezieht sich auf den unteren Schnabel, der im Vergleich zum oberen Schnabel stark reduziert ist. Der Vogel verwendete den unteren Schnabel, um Rinde von Zweigen und kleinen Ästen zu lösen, und den oberen Schnabel, um in Höhlen und weichen Substraten nach Insekten zu suchen. Die Art ist nur aus Fossilienfunden bekannt und leider wie viele ihrer Schwesterarten ausgestorben. Die Radiation der Kleidervögel hat durch die Auswirkungen unbedachter menschlicher Aktivitäten viel zu viele ihrer schönen Artgenossen verloren. (Aus: „Extinct Birds of Hawaii“ von Michael Walther, Mutual Publishing, 2016; © Julian Hume, naturepl.com)
Kompakt
Mendels Gesetz der exponentiellen Kombinationen von Merkmalsausprägungen erklärt, wie eine große Anzahl von phänotypischen* Variationen innerhalb genetischer Familien entstehen bzw. zur Ausprägung kommen kann. Wenn unterschiedliche Kombinationen von Merkmalsausprägungen in den Nachkommen fixiert werden, kann daraus eine Fülle von neuen Arten und Gattungen entstehen. Die für diese (neuen) Arten notwendige Information ist bereits vorhanden, befindet sich latent im Erbgut der Arten und kann durch Homozygotisierung (Entwicklung zu Reinerbigkeit) und Transposition (springende Gene) ausgeprägt werden (vgl. die ersten beiden Teile dieser Artikelserie).
Neue Kombinationen von homozygoten (reinerbigen) Merkmalen können nur erhalten bleiben und fixiert werden, wenn eine Fortpflanzungsisolation auftritt, wenn also Träger verschiedener Merkmalskombinationen nicht (mehr) miteinander hybridisieren*. Durch Selektion werden die geeignetsten dieser Merkmalskombinationen begünstigt, sie werden durch Selektion aber nicht hervorgebracht.
Neue Kombinationen von Merkmalsausprägungen spiegeln die Ausprägung zuvor schon latent vorhandener Information wider. Die Summe aller dieser Kombinationen stellt die Grenzen dar, innerhalb derer eine genetische Familie* sich durch Ausprägung der angelegten Möglichkeiten entfalten kann. Diese intrafamiliäre Evolution (cis-Evolution) erzeugt einen separaten Abstammungsbaum des Lebens. Mehrere solcher separater Familien (Bäume) ergeben einen Wald des Lebens.
Cis-Evolution äußert sich durch vielfältige Aufspaltung innerhalb genetischer Familien, wodurch die latente genetische Information in verschiedensten Kombinationen ausgeprägt wird. Solche Vorgänge werden auch als adaptive Radiation* bezeichnet. Eine Reihe gut untersuchter Beispiele adaptiver Radiationen von genetischen Familien zeigt, dass die entstehende Vielfalt am besten durch präexistente genetische Programme erklärt werden kann. Mutationen können zwar einen zusätzlichen Beitrag zur phänotypischen Vielfalt der Arten leisten, erweisen sich jedoch weder als notwendig noch als förderlich, um die umfangreichen Merkmalsunterschiede hervorzubringen, die man innerhalb der genetischen Familien beobachten kann.
Fortpflanzungsisolation
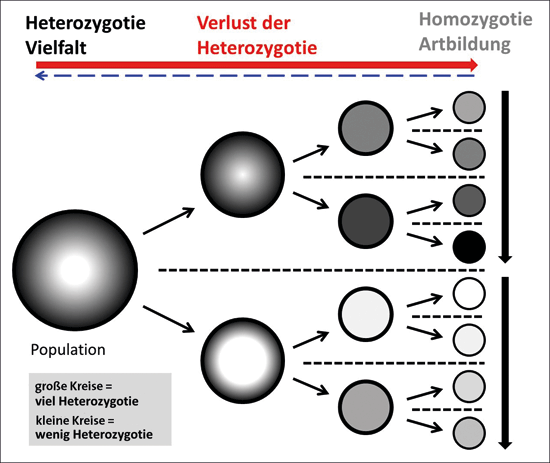
Abb. 1: Verlust der Heterozygotie, Fortpflanzungsisolation und Artbildung. Populationen sind als Kreise dargestellt. Jede Spalte von Kreisen repräsentiert eine aufeinanderfolgende Generation. Mit der Zeit werden Populationen reproduktiv isoliert (gestrichelte Linien). Ursprünglich sind die Populationen genetisch heterozygot (stark abgestufte Schattierung). Wenn sie homozygoter werden, bilden sie genetisch unterschiedliche Gruppen (einheitliche Schattierung). Artbildung erfolgt, wenn die Populationen aus verschiedenen Gründen aufeinanderfolgende Ereignisse erleben, die zur Isolation führen (geringere Größe der Kreise), Verlust von Heterozygotie eintritt und sie zu isolierten, genetisch einzigartigen, homogenen Gruppen werden. Hybridisierungsereignisse können den Trend zum Verlust der Heterozygotie umkehren. Wenn die natürliche Selektion beginnt (vertikale Pfeile, in der zweiten Generation), sind die Populationen mit der günstigsten Konstellation von Eigenschaften (dunklere Schattierung) am besten angepasst und überleben am ehesten.
Für die Mendel’sche Artbildung sind latente phänotypische* Information, der Verlust der Mischerbigkeit sowie Fortpflanzungsisolation* erforderlich. Letztere verhindert Hybridisierung*, die andernfalls zur Wiederherstellung der Heterozygotie (Mischerbigkeit) führen würde, und sie spielt auch eine Rolle bei der Verhinderung von schädlicher Selbstbefruchtung.
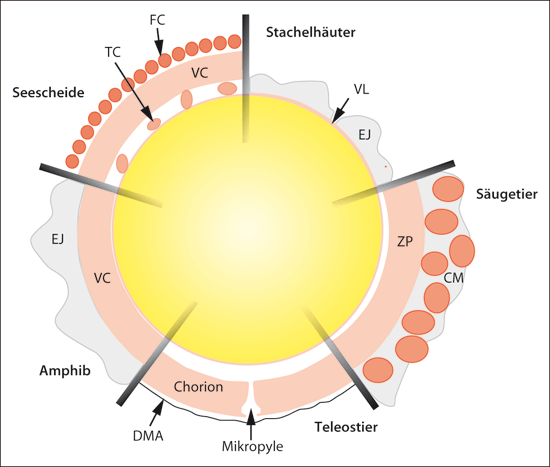
Abb. 2: Die Struktur der äußeren Schichten des Eikomplexes bei verschiedenen Tiergruppen. Bei Euraryoten muss das Spermium das Ei orten, daran haften und mit ihm verschmelzen. Schon bei diesem ersten Stadium weist die Anatomie des Eis extreme Variation auf.
Die Strukturen des Eikomplexes sind hochvariabel und taxonspezifisch (Mengerink & Vacquier 2001). Die Interaktion von Ei und Sperma dient sowohl der Fortpflanzungsisolation als auch der Bewertung der reproduktiven Kompatibilität der beiden Eltern.
Abkürzungen: CM Cumulus-Schutzschicht (Corona radiata); DMA wässrige Schleimzone; EJ Ei-Gallerte; FC Follikelzellen; TC Testzellen; VC Vitelline-Hülle; VL Vitellin-Schicht; ZP Zona pellucida. (Nach Mengerink & Vacquier 2001)
Wenn der Verlust an Mischerbigkeit zur Entstehung mehrerer Arten führen soll, müssen wiederholt Ereignisse auftreten, die zu Fortpflanzungsisolation führen. Bei allopatrischer* Artbildung, die durch räumliche Trennung auf Inseln oder aufgrund von Gebirgszügen verursacht wird, handelt es sich um ein einzelnes Ereignis, durch welches zwei Teilpopulationen getrennt werden. Danach können zwei verschiedene Formen (oder Arten) aufgrund von zufälligem unterschiedlichem Verlust der Mischerbigkeit und durch nachfolgende Selektion entstehen (Abb. 1).
Sympatrische* Artbildung, die durch allmähliche, aber fortschreitende Veränderung der Interaktionsstelle zwischen Rezeptoren der Eizelle und der Bindungsstelle an der Samenzelle verursacht wird, ist ein sich wiederholender Prozess (vgl. Abb. 2 und Crompton 2018). Wie bei der allopatrischen Artbildung werden dabei Teilpopulationen getrennt, und durch den Verlust an Mischerbigkeit und durch nachfolgende Selektion entstehen veränderte Formen (oder Arten). Aber die Änderungsereignisse treten fortwährend auf und führen zu nachfolgenden Abfolgen von Fortpflanzungsisolation, wodurch weitere Teilpopulationen voneinander getrennt werden. Die sympatrische Artbildung kann zur Entstehung mehrerer separater Arten führen (Swanson & Vacquier 2002). Buri (1956) wies nach, dass der Verlust an Mischerbigkeit einfach durch Zufall entsteht, solange in jeder Generation Teilpopulationen reproduktiv isoliert bleiben. Wer die Natur genauer erforscht, lernt eine Fülle phantastischer Mechanismen kennen bezüglich Verhalten, Morphologie oder Genetik, die zur Aufrechterhaltung der Fortpflanzungsisolation der Arten führen, wodurch ihre einzigartigen Merkmalskombinationen erhalten bleiben. Nur wenn diese Mechanismen nicht greifen, entstehen Hybriden. In einigen Fällen kann das sogar bis zum Verlust von Arten führen (Wolfe et al. 2001), nämlich dann, wenn Arten mit geringer Individuenzahl durch Hybridisierung in eine andere Art „einverleibt“ werden.
Die gegenwärtige Fortpflanzungsisolation einer Art mag im Wesentlichen durch einen einzigen Mechanismus verursacht werden. Allerdings können die Vorfahren bei der Entstehung dieser Art die Auswirkungen verschiedener solcher Mechanismen der Fortpflanzungsisolation erfahren haben. Einige mögen durch allopatrische Speziation, andere durch sympatrische Speziation entstanden sein. Einige Mechanismen beruhen auf der genetischen Information einer Art und beeinflussen ihren Phänotyp, ihren Bau, ihr Verhalten oder anderes. Die Geschichte und die Typen der Fortpflanzungsisolationsmechanismen, die für die Entstehung der Art erforderlich waren, tragen vieles zur verbleibenden genetischen Variabilität bei. Wenn nur ein begrenztes Ausmaß an Fortpflanzungsisolation stattgefunden hat, dann gibt es nur einen begrenzten Verlust an Heterozygotie* (vgl. Abb. 9 von Teil 2). Die Art behält dann eine große genetische Variabilität und damit ein großes Anpassungspotenzial. Das ist der Fall z. B. bei der Hain-Bänderschnecke (Cepaea nemoralis; Abb. 3) und beim Wegerichbär (Arctia plantaginis), einem Nachtfalter. Wenn ein deutliches Ausmaß an Fortpflanzungsisolation stattgefunden hat, gibt es entsprechend einen deutlichen Verlust an Heterozygotie. Die Art behält dann nur eine geringe genetische Variabilität und damit ein geringes Anpassungspotenzial. Im Extremfall kommt es zu einer starken Fortpflanzungsisolation und zu einem entsprechend großen Verlust der Heterozygotie. Die daraus resultierende genetisch homogene Art ist dann nicht mehr in der Lage, sich an neue Bedingungen anzupassen (das ist der Fall z. B. bei Geparden und Nördlichen See-Elefanten).

Abb. 3: Ein Beispiel für das Vorhandensein einer großen genetischen Variabilität ist die Hain-Bänderschnecke Cepaea nemoralis. (Aus Junker & Scherer 2013)
Glossar
adaptive Radiation: Entstehung vieler unterschiedlich angepasster Arten aus einer Stammform. Allel: Zustandsform bzw. Variante ein und desselben Gens. Allopatrische Artbildung: → Artbildung im Zusammenhang mit räumlicher (geographischer) Trennung (Separation) der Ausgangsart. Artbildung: Artaufspaltung; Prozess, durch den im Laufe von Generationen eine Art (Spezies) in zwei Tochterarten aufspaltet. dominant: Ein → Allel ist dominant, wenn es die → Merkmalsausprägung eines anderen (→ rezessiven) Allels unterdrückt. Epistasis: Gen-Wechselwirkung. Die Wirkung des einen (epistatischen) Gens verdeckt die Merkmale des anderen (hypostatischen) Gens. eukaryotische Organismen: Lebewesen mit echten Zellkernen, die zur Meiose fähig sind. exprimieren: Das Ablesen und somit Nutzbarmachen von Genen bzw. der durch sie codierten Information im Zellbetrieb. Fortpflanzungsisolation: Trennung von Populationen und Unterdrückung eines Genaustauschs. genetische Familie: Familie, deren zugehörende Arten durch verschiedene Merkmalskombinationen einer präexistenten Vielfalt charakterisierbar sind. Genom: Das gesamte Erbgut eines Individuums. Genotyp: die einzigartige Gesamtheit aller Erbfaktoren eines Individuums. heterozygot: mischerbig (das Gen liegt in zwei verschiedenen Allelen vor.) homozygot: gleicherbig (das Gen liegt in zwei gleichen Allelen vor.) Hybrid: Mischling. hypostatisch: → Epistasis. Karyotyp: Gesamtheit aller zytologisch (den Zellaufbau betreffend) erkennbaren Chromosomeneigenschaften eines Individuums. latent: versteckt, verborgen (hier: im Erbgut). Ein → Merkmal oder → Merkmalszustand ist latent, wenn es / er zwar genetisch angelegt ist, aber nicht ausgeprägt (→ exprimiert) wird. Meiose: Reifeteilung, Bildung der Geschlechtszellen. Mutation: Spontane oder künstlich ausgelöste Änderung des Erbguts. pan-heterozygot: Alle phänotypisch sich auswirkenden Gene liegen mischerbig vor. Phänotyp: äußere Erscheinungsform (Morphologie, Anatomie, Physiologie) betreffend. Radiation: → adaptive Radiation. radiometrische Jahre: Jahre nach gängigen radiometrischen Datierungsmethoden bestimmt. Rekombination: Durchmischung des Erbgutes bei der sexuellen Fortpflanzung. rezessiv: Ein → Allel ist rezessiv, wenn es durch die → Merkmalsausprägung eines anderen (→ dominanten) Allels unterdrückt wird. Sympatrische Artbildung: → Artbildung ohne begleitende räumliche (geographische) Trennung der Ausgangsart. Translokation: Umlagerung von Chromosomenabschnitten. Zygote: Zelle von → Eukaryoten, die bei der geschlechtlichen Fortpflanzung durch Verschmelzung von einer Eizelle und einem Spermium entsteht.
Unterschied Art – Familie
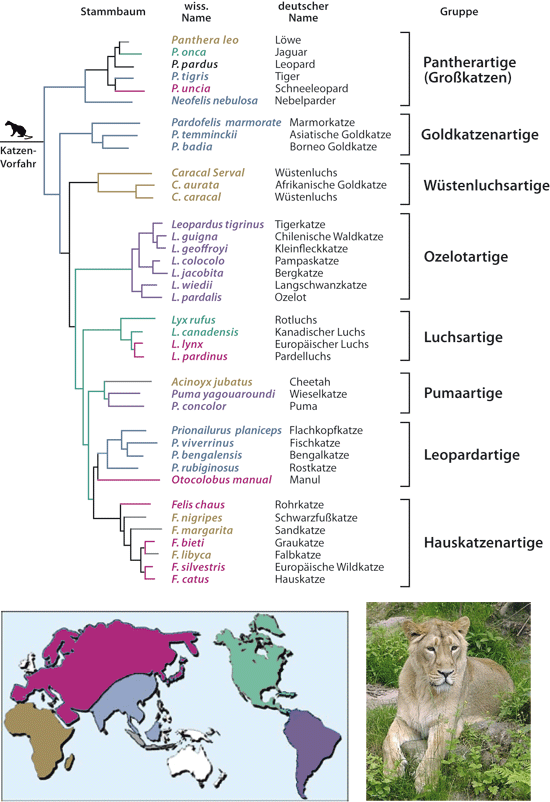
Abb. 4: Dendrogramm der Katzengruppen. Die Endpunkte entsprechen jeweils einer Art. Die Farben korrespondieren jeweils mit dem entsprechenden Erdteil. Der Leopard hat von allen Katzen das weiteste Verbreitungsgebiet, von Afrika über das südliche Eurasien bis Ostasien. Umgezeichnet nach Johnson und Mitarbeiter (2006), dort sind auch weitere Informationen wie die genetische Distanz etc. zu finden. Insertbild: Asiatisches Löwenweibchen (Panthera leo perisca). (Foto: Edradour, CC BY-SA 3.0)
Auf welche Weise helfen Mendels Experimente mit Pflanzenhybriden die Frage zu klären, was eine Art ist und was eine Familie? Nehmen wir einmal an, dass eine Urahnen-Art 20 heterozygote Gene besitzt. Diese Art kann theoretisch mehr als eine Million (220 = 1.048.576) einzigartige reinerbige Nachkommen hervorbringen, deren Phänotypen in 20 unterschiedlichen Merkmalen variieren. Viele dieser Nachkommen werden wegen dieser großen Unterschiede separaten Arten und sogar separaten Gattungen zugeordnet. Diese über eine Million verschiedenen Phänotypen stellen die theoretische Gesamtanzahl der Mendel’schen Vielfalt oder des phänotypischen Ausmaßes der Urahnen-Art und ihrer potenziellen Nachkommen dar. Theoretisch gehören alle ihre Nachkommen zu derselben Art wie ihr pan-heterozygoter* Urahn, doch aus praktischen Gründen werden sie in separate Arten und Gattungen einer übergeordneten genetischen Familie eingeteilt. So sind Löwen, Tiger, Servale, Geparde, Luchse, Leoparden, Pumas und Hauskatzen allesamt Mitglieder der Familie der Felidae. Sie haben wahrscheinlich einen einzigen gemeinsamen panhybriden Vorfahren. Auf der Grundlage ihrer Kreuzungsfähigkeit gehören die meisten Katzenarten zu einem einzigen Grundtyp (Pendragon & Winkler 2008). Sie teilen dieselben Merkmale und dieselben Gene und stellen eine genetische Familie* dar (vgl. Abb. 4). Die Kombinationen konstanter Merkmalsausprägungen (Kombinationen homozygoter* dominanter* und rezessiver* Allele*) sind die Grundlage für ihre Einteilung in einzigartige Arten und Gattungen.
Auf ähnliche Weise weisen die Paradiesvögel ein spektakuläres Spektrum an erstaunlichen Phänotypen auf. DNA-Sequenzuntersuchungen zeigen, dass sie alle Mitglieder der Familie Paradisaeidae sind. Ihre Kreuzungsfähigkeit bestätigt, dass die meisten Arten zu einem einzigen Grundtyp gehören (Scherer 1993). Die Tatsache, dass verschiedene Gattungshybriden ähnliche Phänotypen aufweisen, zeigt, dass sie von einem gemeinsamen panheterozygoten Vorfahren abstammen (Crompton 2020). Man könnte hier noch sehr viel mehr Beispiele nennen.
Dieses genetische Prinzip findet man in der gesamten Welt der Eukaryoten (meiotische* Organismen). Vergleichbare Radiationen können im Fossilbericht als Kombinationen konstanter Merkmalsausprägungen innerhalb einer genetischen Familie interpretiert werden. Als Beispiel dafür seien die Sauropoden genannt (Abb. 5; Erläuterungen in der Legende). In der jüngeren Vergangenheit haben spektakuläre adaptive Radiationen* sogar Hunderte von neuen Arten innerhalb von Pflanzen- und Tierfamilien hervorgebracht, die auf der Mendel’schen Artbildung und der Ausprägung bereits vorhandener genetischer Variationen basieren (s. u. Abschnitt „Adaptive Radiation – einige Beispiele“).
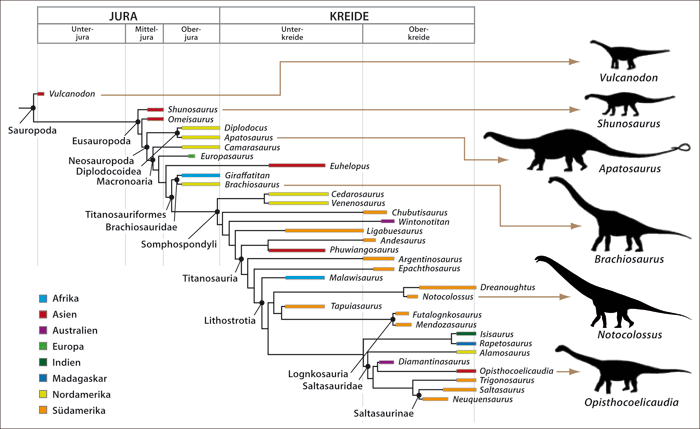
Abb. 5: Dendrogramm der Gruppen der Sauropoda. Die Endpunkte entsprechen jeweils einer Gattung. Die Farben korrespondieren mit dem entsprechenden Erdteil. Gezeigt sind auch die stratigraphischen Stufen, in denen die jeweiligen Gruppen gefunden wurden. Die Sauropoda scheinen eine morphogenetisch einheitliche Familie zu bilden. Sie können sehr gut als eine adaptive Radiation verstanden werden. Ihre latenten präexistenten genetischen Programme haben sich vermutlich nach den Mendel’schen Regeln aufgespalten und eine begrenzte, aber diverse Familie hervorgebracht. Die Möglichkeit, dass es sich bei den Sauropoda um mehr als eine einzige genetische Familie handelt, kann nicht ganz ausgeschlossen werden. Zur sicheren Klärung fehlen bei Fossilien wichtige Daten. (Nach González Riga et al. 2016)
Gegen Schluss seiner wissenschaftlichen Abhandlung formulierte Mendel Überlegungen, wie weit die Artbildung gehen könnte. Wenn die Artbildung keine Grenzen hat, könnte das Leben theoretisch aus einer einzelnen Zelle entstanden sein und einen einzigen umfassenden Abstammungsbaum bilden. Wenn die Artbildung jedoch Grenzen hat, würde man viele stabile genetische Familien beobachten und das Leben wäre wie ein Wald, der aus vielen Bäumen besteht. Das wäre eine elegante Bestätigung der Aussage in der Heiligen Schrift, dass Pflanzen und Tiere nach ihren Arten geschaffen wurden.
Mendels Ergebnisse zeigten, dass es Grenzen gab. Mendel machte auch auf die Experimente von Gärtner aufmerksam, der „in der vollendeten Umwandlung einer Art in eine andere den unzweideutigen Beweis [sah], dass der Species feste Grenzen gesteckt sind, über welche hinaus sie sich nicht ändern vermag“ (s. o.; Gärtner dachte an eine begrenzte Anzahl von Kombinationen, nicht an eine unendliche Anzahl von Mutationen). Mendel war vorsichtig und nannte diese Experimente nur eine „beachtenswerthe Bestätigung“. Doch Gärtners Argument war richtig, und wenn die Artbildung überwiegend aus dem Mendel’schen Gesetz der exponentiellen Kombinationen von Merkmalsausprägungen resultiert, dann haben genetische Familien intrinsische phänotypische Grenzen, die durch das Ausmaß ihrer Merkmalsausprägungen definiert werden, und das Leben auf der Erde ist ein Wald mit vielen Bäumen. Am Schluss seiner Abhandlung führt Mendel die von Gärtner untersuchten Arten auf und bestätigt dadurch seine Überzeugung, dass es Grenzen gibt und dass diese Schlussfolgerung sich auf viel mehr als nur auf Erbsen und Bohnen bezieht, sondern eine allgemeine Gültigkeit hat.
Adaptive Radiationen
Warum ist der Verlust an Mischerbigkeit für die Artbildung so wichtig? Bei völliger Mischerbigkeit zeigt sich nur der pan-dominante Phänotyp (vgl. Abb. 9 in Teil 2). Alle Phänotypen, die sich aus den Kombinationen von rezessiven* und hypostatischen* Merkmalsausprägungen ergeben, sind verdeckt (bzw. unterdrückt). Durch den Verlust der Mischerbigkeit wird dieser gewaltige Reichtum an phänotypischem Potenzial abgerufen, der latent in einem Genom* verborgen liegt. Schon eine so geringe Zahl wie 10 Merkmale (bzw. Gene) ermöglicht die Entstehung von tausend (210 = 1.024) einzigartigen Phänotypen, wobei sich jeder in 10 verschiedenen Merkmalen vom anderen unterscheidet. Doch nur wenige Wirbeltierfamilien zeigen diese Menge an Variationen (bzw. Arten), obwohl sie immer noch recht begrenzt ist. In den meisten Säugetier-Familien gibt es weniger als hundert unterschiedliche Arten.

Abb. 6: Beispiele für die Vielgestaltigkeit der Buntbarsche in ostafrikanischen Seen. Von oben: Pseudotropheus saulosi, Lamprologus spec. und Chalinochromus ndobhoi. (Aus Junker & Scherer 2013)
Wenn doch so viele Variationsmöglichkeiten zur Verfügung stehen, wird man die Varianten jemals tatsächlich in der Natur finden? Zu den spektakulärsten Beispielen gehören heute beobachtbare adaptive Radiationen, allen voran die „Bildflügel“-Drosophilas („picture-wing Drosophila“) auf Hawaii, die Silberschwert-Pflanzengruppe ebenfalls auf Hawaii, die Buntbarsche in den großen ostafrikanischen Seen und die Finken auf den Galápagos-Inseln und auch auf Hawaii. Der Verlust der Mischerbigkeit ist ein Mechanismus, der die bei Pflanzen und Tieren beobachteten üppigen adaptiven Radiationen erklärt. So sollen die nahezu 1000 in Hawaii heimischen Drosophila-Arten aus einer einzigen dorthin gelangten Ursprungsart entstanden sein. Mit Hilfe von Chromosomen-Inversionen wurden die Artbildungsereignisse ausgehend vom standardmäßigen Grundtyp oder Gründerkaryotyp – eventuell aus Südamerika – bis hin zu allen Karyotypen der bestehenden Arten in der Bildflügel-Drosophila-Gruppe nachvollzogen (Carson 1983). Die Inversionen liefern allerdings keine Erklärung dafür, wie die phänotypischen Änderungen zustande gekommen sind (Noor et al. 2001); mit ihrer Hilfe kann man lediglich Abstammungslinien rekonstruieren. Man weiß in der Tat, dass die Radiation der Bildflügel-Gruppe mit ungefähr 112 Arten mit relativ wenigen Änderungen in der DNA-Sequenz vonstattenging (Edwards et al. 2007). Wenn diese Radiation aber durch den Verlust an Mischerbigkeit entstand, wäre wenig DNA-Sequenzänderung erforderlich gewesen, vielmehr lediglich Rekombination* und Homozygotie in neuen Kombinationen bereits vorhandener Allele.
Die Silberschwert-Pflanzen von Hawaii enthalten Bäume, Sträucher, Halbsträucher, semi-holzige Rosettenpflanzen, Teppichpflanzen, Polsterpflanzen und Lianen. Diese Gruppe umfasst drei Gattungen, Argyroxiphium, Dubautia und Wilkesia, mit dreißig Arten. Trotz der großen Formenvielfalt lassen sich fast alle von ihnen untereinander kreuzen und die molekularphylogenetische Analyse zeigt, dass es sich um einen monophyletischen Stammbaum handelt, der durch ein einzelnes Gründerereignis entstanden ist. Die Pflanzen sind allopolyploid (üblicherweise n=14) und man ist der Ansicht, dass sie aus einer Kreuzung zwischen den als „Tarweeds“ bezeichneten Arten Anisocarpus scabridus (n=7) und Carlquistia muirii (n=8) entstanden sind und anschließend eine Chromosomenreduktion (auf n=14) stattgefunden hat. Untersuchungen der homöotischen Blütengene ASAP1 und ASAP3 (Barrier et al. 1999) bieten sehr starke experimentelle Belege für den hybriden Ursprung dieser Pflanzen. Die meisten Arten haben zwei Kopien von beiden Genen. Bei drei Dubautia-Arten fehlt jedoch eins der vier ASAP-Gene. Zwar können solche homöotischen Gene zur Entwicklung der Blütenform beitragen, aber die Tatsache, dass ein Gen ohne negative Folgen fehlen kann, bestätigt, dass nicht die ASAP-Gene, sondern ein anderer Mechanismus in erster Linie für das gewaltige Spektrum morphologischer Vielfalt verantwortlich ist. Die verschiedenen Gattungen zeigen unterschiedliche Translokationsereignisse*, mit deren Hilfe man wie bei Drosophila Abstammungslinien zurückverfolgen kann. Jedoch sind auch sie nicht der Mechanismus, der die verschiedenen morphologischen Formen verursacht (Carlquist et al. 2003), sondern nur Marker der abgelaufenen Divergenzen. Dagegen bietet der Verlust der Mischerbigkeit eine Erklärung für die extensive phänotypische Vielfalt dieser Pflanzengruppe und ihr Potenzial, sich so umfassend anzupassen und in eine große Zahl von Wuchsformen aufzuspalten. Der tetraploide Zustand dieser Pflanzen-Kreuzung kann höchstwahrscheinlich eine Maskierung verschiedener Gene, die durch Mutationen* oder Epistasis* bewirkt worden war, aufheben; dadurch ist die Ausprägung der reichen phänotypischen Vielfalt höchstwahrscheinlich ausgelöst werden.
In den großen ostafrikanischen Seen weisen die Buntbarsche (Abb. 6) größere adaptive Radiationen auf und dienen so als Beispiel für sexuelle Selektion und eventuell für sympatrische Artbildung (Seehausen & van Alphen 1998). Diese Fische weisen eine spektakuläre morphologische Vielfalt in Bezug auf die Nahrungsaufnahme auf – dazu gehören Spezialisten wie Algenschaber, Planktonfresser, Insektenfresser, Fischfresser, Allesfresser, Schneckenbrecher und Flossenbeißer. Dazu kommt eine noch verblüffendere Serie von Farbmustern (Stiassny & Meyer 1999).
Der Malawisee enthält eine Schar von mehr als 500 Arten von Buntbarschen, die nachgewiesenermaßen von einem einzigen Vorfahren abstammen (Albertson et al. 1999). Im Viktoriasee gibt es eine ähnliche Schar von mehr als 500 einheimischen Buntbarscharten, die nur zwei Abstammungslinien haben und vielleicht, wie angenommen, erst innerhalb der letzten 15.000 (radiometrischen*) Jahre entstanden sind (Verheyen et al. 2003). Sie sind genetisch relativ homogen und weisen trotzdem einen hohen Grad an morphologischer Divergenz auf. Als Antriebskräfte für die Artbildung wurden die Fortpflanzungsisolation mittels extremer Brutortstreue (Philopatrie) sowie sexuelle Selektion und „inselähnliche“ See-Lebensräume in Betracht gezogen und intensiv diskutiert (Salzburger & Meyer 2004).
Eine ähnliche explosive Radiation von Buntbarschen, die in einem kurzen Zeitfenster ökologischer Möglichkeiten ablief, scheint sich in dem ausgetrockneten prähistorischen Makgadikgadi-Paläosee ereignet zu haben und sie scheint die Flusssysteme des südlichen Afrikas befruchtet zu haben. Man kann viele faszinierende Merkmalsparallelen zwischen Arten in den Buntbarsch-Radiationen in diesen drei Seen beobachten, die auf präexistente genetische Programme und gemeinsame Abstammung zurückführbar sind (Joyce et al. 2005). Zudem berichten die Autoren aber auch von bedeutsamer Divergenz der haploiden Genotypen* innerhalb von Arten und von Erhaltung der haploiden Genotypen zwischen entfernter verwandten Arten. Das bestätigt, dass die genetische Änderung per se keine ausreichende Erklärung für die Artbildung ist. Dagegen bietet der Verlust der Mischerbigkeit eine angemessene Erklärung für das enorme Ausmaß der vorhandenen Vielfalt. Es wurden an fünf Fischen Sequenzierungs-Untersuchungen durchgeführt (Brawand et al. 2014), und zwar bei jeweils einem Fisch aus den größeren Abstammungslinien der Buntbarsche, um der Frage nach dem Ursprung der Vielfalt nachzugehen. Die 75 Autoren dieser Veröffentlichung kamen zu dem gemeinsamen Schluss, dass bereits bestehende Variation (d. h. präexistente genetische Programme) für die evolutive Diversifikation wichtig war. In seiner Stellungnahme zu der Untersuchung bemerkte Jiggins (2014), dass die Daten über die Buntbarsche andere Arbeiten ergänzen, „welche von Stichlingen bis zu Schmetterlingen reichen“, und nachweisen, dass sich adaptive Radiationen „aus alten gemeinsamen Variationen“ (d. h. präexistente genetische Programme) ergeben.
Adaptive Radiationen speisen sich aus „alten gemeinsamen Variationen“. Dabei dürfte es sich um präexistente genetische Programme handeln.
Diese Vorhersage von Jiggins und zahlreiche damit verbundene Feldstudien über die Entstehung von Arten bei adaptiven Radiationen wurden von Berner & Salzburger (2015) kritisch überprüft. Sie kamen zum Schluss, dass „die Genome dieser Arten adaptive Allelvarianten* enthalten, die lange vor der Entstehung der eigentlichen Arten oder Populationen entstanden sind“. Das entspricht genau dem, was Mendel’sche Artbildung beinhaltet. Seehausen und seine Kollegen haben die Radiation der Buntbarsche erneut untersucht (Meier et al. 2017). Inzwischen haben sie die Genome von über 150 Arten sequenziert. Sie kommen zum Ergebnis, dass die Fische in den verschiedenen großen Seen getrennt wurden (und Fortpflanzungsisolation erfahren haben) und in seltenen Fällen mit ihren angestammten Cousins wieder zusammengebracht wurden (was Hybridisierung zur Folge hatte) und dann erneut getrennt wurden (mit erneuter Fortpflanzungsisolation). Ein Prozess, der als „Spaltung-Fusion-Spaltung“ bezeichnet wird, den Seehausen als „den stärksten Motor für die Bildung neuer Arten und neuer Anpassungen“ bezeichnet hat. Ihre Ergebnisse wurden auf der Konferenz „Origins of Adaptive Radiation“ in Honolulu, Hawaii, vorgestellt (Pennisi 2018). Pennisi fasste zusammen: „Die Artbildung bei Buntbarschen wurde durch bereits bestehende genetische Variation unterstützt“, und der Evolutionsbiologe Schluter bestätigte: „Alle für die Artbildung erforderlichen Variationen sind bereits vorhanden ... Der gleiche Mechanismus soll auch zu Radiationen mariner Stichlinge und von Käfern geführt haben.“ Latente phänotypische Information, die durch Hybridisierungszyklen und durch Verlust der Heterozygotie zur Ausprägung kam, erklären die Entstehung der Arten, die bei adaptiven Radiationen beobachtet wurden.
Schlussfolgerungen
Die Mendel’sche Artbildung basiert auf seinem Gesetz der exponentiellen Kombinationen von Merkmalsausprägungen und dieses ist eine mehr als ausreichende Erklärung für die Entstehung der biologischen Vielfalt. Es erklärt ohne Weiteres die spektakulärsten Beispiele von adaptiven Radiationen innerhalb von Familien. Mendel’sche Artbildung läuft ab, weil die für die Aufspaltung und Veränderung der Arten erforderliche Information bereits im Genom der Organismen vorhanden ist, in einem latenten Zustand gehalten wird und darauf wartet, ausgeprägt zu werden. Diese Erklärung ist weit entfernt von den vielen genetischen Fachartikeln, die sich für die Mutationsereignisse als Quelle neuer genetischer Merkmalsausprägungen stark machen.
Cis-Evolution und Mikroevolution
In kritischen Diskussionen um Evolution werden häufig die Begriffe „Mikroevolution“ und „Makroevolution“ verwendet. Diese beiden Begriffe werden unterschiedlich und nicht selten unscharf definiert (z. B. „Mikroevolution“ als Evolution innerhalb einer Art oder innerhalb einer Familie) oder beide Begriffe werden nur quantitativ unterschieden (wenig oder viel Evolution). Aus diesem Grund werden hier die Begriffe „cis-Evolution“ und „trans-Evolution“ eingeführt, um einen qualitativen und wesentlichen Unterschied zwischen diesen beiden Arten von Veränderungen zum Ausdruck zu bringen (vgl. Abb. 7). Man kann „Mikroevolution“ so definieren wie in Junker & Scherer (2013, 44+48), dass der Begriff identisch ist mit „cis-Evolution“, und „Makroevolution“ so, dass damit dasselbe wie „trans-Evolution“ gemeint ist. Nach Junker & Scherer (2013, 44) ist Mikroevolution „Evolution innerhalb vorgegebener Organisationsmerkmale; quantitative Veränderung bereits vorhandener Organe, Strukturen oder Baupläne“. Makroevolution dagegen bezeichnet die „Entstehung neuer, bisher nicht vorhandener Organe, Strukturen und Bauplantypen; damit verbunden auch die Entstehung qualitativ neuen genetischen Materials.“ Nach diesen beiden Autoren ist ein entscheidendes Unterscheidungskriterium zwischen Mikro- und Makroevolution das Vorliegen verschiedener Fragestellungen bzw. Erklärungsprobleme. Bei Mikroevolution geht es demnach um die Fragestellung, wie vorhandene (latente) Information zur Ausprägung kommt, während es bei Makroevolution um die Frage geht, woher überhaupt präexistente Programme und neue Merkmale kommen.
Hier prallen Weltanschauungen aufeinander. Um zu verstehen, warum das so ist, sollte man den Unterschied erkennen zwischen Evolution innerhalb separater genetischer Familien und Evolution über diese Familien hinaus oder von einer genetischen Familie zur anderen. Die Evolution innerhalb einer genetischen Familie, die cis-Evolution, ist die Art von Evolution, die man tatsächlich in der Praxis beobachtet, sei es im Freiland oder Laborstudien (vgl. Kasten und Abb. 7). Dazu gehören zum Beispiel die Änderungen der hellen und dunklen Morphen des Birkenspanners, die bei den Darwinfinken beschriebenen Änderungen (z. B. in der Schnabelform, Körpergröße oder Gefiederfärbung) oder die oben erwähnte durch adaptive Radiationen entstandene Vielfalt.
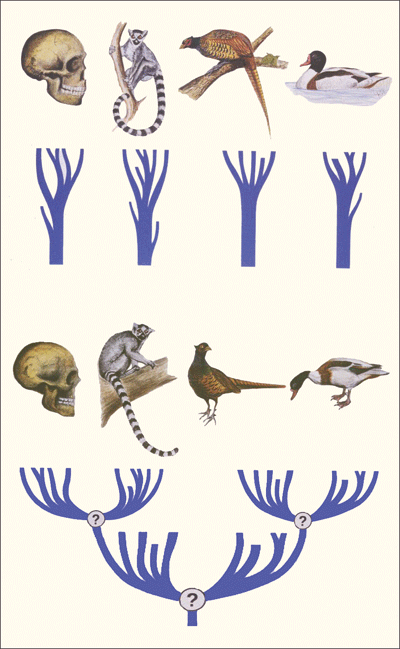
Abb. 7: Cis-Evolution versus trans-Evolution.
Bei der cis-Evolution (oben) sind mehrere separate Familien zu sehen. Jede Familie hat die Form eines Baumes. Die Äste innerhalb eines Baumes werden durch Fortpflanzungsisolation auseinandergehalten, aber können durch sporadische Hybridisierung gelegentlich wiedervereint werden. Es gibt hier einen „Wald“ des Lebens. Dieser soll durch präexistente genetische Programme und Mendel’sche Artbildung zustande gekommen sein.
Bei der trans-Evolution (unten) sind dagegen alle Familien abstammungsmäßig miteinander verbunden. Es gibt hier nur einen einzigen großen Lebensbaum. Dieser soll durch Mutationen und Selektion zustande gekommen sein. (Nach Junker & Scherer 2013, verändert)
Cis-Evolution erfolgt dadurch, dass die für diese Änderungen erforderliche Information schon in Form präexistenter genetischer Programme im Genom latent vorhanden ist. Normalerweise wird diese Information ausgeprägt, wenn die meiotische Rekombination einen Verlust an Mischerbigkeit verursacht. Hierbei spielen Dominanz, Epistasis und auch spezialisierte Mechanismen der Transposon-Aktivierung eine Rolle (vgl. den 2. Teil dieser Artikelserie). Der vollständige Satz von Allelpaaren eines diploiden Organismus lässt ein breites Spektrum von potenziellen Phänotypen entstehen, durch welche die biologischen Grenzen einer Familie definiert werden. Es ist dazu gar keine große Anzahl von präexistenten genetischen Programmen erforderlich. Nur zwanzig solcher Programme (d. h. 10 Gene mit je zwei Allelen) reichen bereits aus, um 1000 verschiedene Arten zu erzeugen (vierzig Programme (d. h. 20 Gene mit je zwei Allelen) könnten 1.000.000 Arten erzeugen). Der Begriff der präexistenten genetischen Programme ist gleichbedeutend mit dem der „standing variation“ (nach Brawand et al. 2014) und mit dem der „alten genetischen Varianten“ (Jiggins 2014). Mit allen drei Begriffen wird zum Ausdruck gebracht, dass die Information für die Variation, welche adaptive Radiationen antreiben, bereits existiert.
Das Gegenstück zur cis-Evolution ist die trans-Evolution, die für unbekannte Mechanismen steht, welche die Entwicklung von Familien über ihre Grenzen hinaus ermöglichen würden. In der Vergangenheit sollte es diese Art von Evolution einem gemeinsamen Vorfahren ermöglicht haben, separate genetische Familien entstehen zu lassen. Ein Ur-Fleischfresser hätte sowohl Katzen als auch Hunde hervorgebracht, und ein Ur-Unpaarhufer hätte Pferde, Tapire und Nashörner entstehen lassen. Was für eine Art von Mechanismus könnte eine trans-Evolution möglich machen? Mendel glaubte nicht, dass ein solcher Mechanismus existiert. Als er die Anpassung von Pflanzen an neue Umgebungen schilderte, schrieb er: „… nichts berechtigt uns zu der Annahme, dass die Neigung zur Varietätenbildung so ausserordentlich gesteigert werde, dass die Arten bald alle Selbstständigkeit verlieren und ihre Nachkommen in einer endlosen Reihe höchst veränderlicher Formen auseinander gehen.“ Offensichtlich waren Wallace (1858) und Darwin (1959) anderer Meinung, obwohl keiner von beiden eine schlüssige Erklärung für trans-Evolution liefern konnte.

Abb. 8: Aus der Felsentaube (links) wurde im Laufe weniger hundert Jahre eine Reihe von z. T. skurrilen Formen gezüchtet. (Zeichnung: Lotti Haller; aus Junker & Scherer 2013)
Der meiotische Mechanismus nach Mendel erklärt die cis-Evolution, aber nicht die trans-Evolution. Deren zweifelhafter „Erfüllungsgehilfe“, die Mutation, verursacht zwar einige cis-evolutionäre Variationen, die überwiegend zum Verlust oder zu Beeinträchtigung oder Dysregulation biologischer Funktionen führen. Mutationen können jedoch keine Artbildungsereignisse erklären, für welche ja umfangreiche phänotypische Änderungen notwendig sind. Zahllose Experimente mit Mutagenen bestätigen die beträchtlichen schädlichen Veränderungen, die durch Mutationen verursacht werden.
Wallace und Darwin erkannten, dass Arten Varietäten hervorbringen können, welche wiederum neue Arten entstehen lassen können. Sie irrten sich aber, indem sie diese Erkenntnisse übermäßig extrapolierten und annahmen, die biologische Veränderung habe keine Grenzen. Das wäre aber eine notwendige Voraussetzung für die trans-Evolution, wenn sie einen einzigen Stammbaum des Lebens hervorbringen soll. Mendel zeigte, dass neue biologische Vielfalt aus latenter Merkmalsinformation entsteht, die auf dem Repertoire der präexistenten Allele basiert, und dass die evolutionäre Veränderung sich im Wesentlichen darauf beschränkt. Nach allem, was man beobachten kann, ist das Leben ein Wald mit vielen Bäumen. Dadurch erklärt sich, dass in Lehrbüchern über die Evolution viele gute Beispiele zur cis-Evolution gebracht werden, aber nur bloße Spekulationen über die Mechanismen der trans-Evolution zu finden sind. Da cis-Evolution auf der Rekombination alternativer Merkmale (präexistente genetische Programme) basiert, ist die logische Erwartung, dass zahlreiche, völlig funktionale alternative Arten auftreten werden. Dasselbe kann für die trans-Evolution nicht gesagt werden, da sie auf vielfachen Mutationsereignissen basiert und die logische Erwartung wäre, dass eine Fülle von dysfunktionalen Phänotypen auftritt. Dagegen sind präexistente genetische Programme eine Grundlage für die reiche Vielfalt des Lebens. Ihre ursprüngliche Quelle kann am ehesten als die Aktivität eines allwissenden Schöpfers verstanden werden (teleologisches bzw. Design-Argument).

Abb. 9: Gregor Johann Mendel (1822–1884), der Vater der modernen Genetik, war in der Frage nach der Quelle der Vielfalt innerhalb genetischer Familien auf der richtigen Spur. (Mit freundlicher Genehmigung der Abtei St. Thomas, Brno)
Das phänotypische Potenzial der Organismen ist enorm. Mendel hat uns gezeigt, wie man dieses Potenzial anzapfen kann. In der Vergangenheit zähmte der Mensch den Grauwolf, Canis lupus, und selektierte Hunderte von Hunderassen mit ihrem gewaltigen Spektrum an Phänotypen. Der Mensch nahm den einfachen Acker-Senf, Brassica oleracea, und gewann durch künstliche Selektion daraus Blumenkohl, Kopfkohl, Brokkoli, Grünkohl, Rosenkohl, Blattkohl und Kohlrabi. Darwin nahm die Taube, Columbia livia, und züchtete daraus eine Anzahl von neuen Rassen (vgl. Abb. 8). Das beschrieb er als „Variieren der Thiere und Pflanzen im Zustande der Domestikation“ (Darwin 1859, Kapitel 1). Rosengimpel tauchten in Hawaii auf und brachten die herrlich vielfältigen Kleidervögel hervor (s. Introbild S. 78). Zwei Vorläufer (kleine krautige Korbblütler, sogenannte „Tarweeds“) der auf Hawaii heimischen Silberschwert-Allianz gelangten aus Kalifornien auf die Hawaii-Inseln und brachten dort äußerst vielfältige Formen hervor. Buntbarsche gelangten in die großen Seen Afrikas und es entstanden daraus Hunderte von neuen Fischarten.
Mendel zeigte, dass latente Information in den Genomen der Organismen gespeichert ist, und er zeigte auch, wie auf diese Information zugegriffen und wie sie ausgeprägt wird. Seine Forschungsergebnisse lassen uns viel besser verstehen, was Arten und genetische Familien sind, und auch, warum die Definition von Arten seit jeher so außergewöhnlich schwierig ist. Familien haben eine gemeinsame Genetik und dieselben Gene, jedoch verschiedene Allele derselben. Das ermöglicht Hybridbildung aus verschiedenen Arten innerhalb von Familien – trotz der vielen Mechanismen, die zur Förderung der Fortpflanzungsisolation eingerichtet sind. Die Fortpflanzungsisolation ist aber entscheidend, weil sie die Ausprägung und Fixierung rezessiver oder hypostatischer Information ermöglicht. Das fördert phänotypische Vielfalt, die sonst durch die Hybridisierung und Mischerbigkeit unterdrückt würde. Die unterschiedlichen Allele gemeinsamer Gene bieten ein großes Potenzial phänotypischer Vielfalt. Sie ermöglichen es einer genetischen Familie, sich durch adaptive Radiation zu einer Überfülle an Arten zu entwickeln. Diese nicht auf Mutationen beruhende Form der Artbildung ist das Erbe Mendels, die Frucht seines Gesetzes der exponentiellen Kombinationen von Merkmalsausprägungen. Seine Versuche über Pflanzenhybriden führten zu umfangreichen und bedeutsamen Erkenntnissen in der Genetik und insbesondere „Über die Entstehung der Arten“.
Danksagung: Dies ist der dritte Teil eines anspruchsvollen Manuskripts. Es ist angebracht, Dr. Reinhard Junker für die wunderbare Arbeit, die er als Herausgeber geleistet hat, zu danken, und sie lobend zu erwähnen. Alle drei Beiträge haben von seinem Wissen und seinen Anregungen stark profitiert. Seine Gaben schätze ich sehr und sie ehren den Schöpfer.
Phylogeny of a rapidly evolving clade: The cichlid fishes of Lake Malawi, East Africa. Proc. Natl. Acad. Sci. 96, 5107–5110.
Interspecific hybrid ancestry of a plant adaptive radiation: allopolyploidy of the Hawaiian silversword alliance (Asteraceae) inferred from floral homeotic gene duplication. Mol. Biol. Evol. 16, 1105–1113.
The genomics of organismal diversification illuminated by adaptive radiations. Trends Genet. 31, 491–499.
he genomic substrate for adaptive radiation in African cichlid fish. Nature 513, 375–381.
Gene frequency drift in small populations of mutant Drosophila. Evolution 10, 367–402.
Tarweeds and Silverswords. Missouri Bot.s Garden Press, St. Louis.
Chromosomal sequences and inter-island colonizations in Hawaiian Drosophila. Genetics 103, 465–482.
Die genetische Familie der Haliotidae – Hybridisierung, Fortpflanzungsisolation und sympatrische Artbildung. http://www.wort-und-wissen.de/artikel/sp/b-18-2_haliotidae.pdf
Die Paradiesvögel, ihre Hybriden und die Rolle der sexuellen Selektion. https://www.wort-und-wissen.org/wp-content/uploads/b-20-3_paradiesvoegel.pdf
On the origin of species by means of natural selection, or the preservation of favoured races in the struggle for life. John Murray, London.
A database of wing diversity in the Hawaiian Drosophila. PloS ONE 2:e487
A gigantic new dinosaur from Argentina and the evolution of the sauropod hind foot. Sci. Rep. 6:19165, doi:10.1038/srep19165.
Radiating genomes. Nature 513, 318–319.
An extant cichlid fish radiation emerged in an extinct Pleistocene lake. Nature 435, 90–94.
Evolution – ein kritisches Lehrbuch: Gießen, 7. Auflage.
Ancient hybridization fuels rapid cichlid fish adaptive radiations. Nat. Comm. 8:14363.
Chromosomal inversions and the reproductive isolation of species. Proc. Natl. Acad. Sci. 98, 12084–12088.
The family of cats: delineation of the feline basic type. J. Creation 25, 118–124.
Hybrids spawned Lake Victoria’s rich fish diversity. Science 361, 539.
The species flocks of East African cichlid fishes: recent advances in molecular phylogenetics and population genetics. Naturwiss. 91, 277–290.
The effect of male coloration on female mate choice in closely related Lake Victoria cichlids (Haplochormis nyererei complex) Behav. Ecol. Sociobiol. 42, 1–8.
Basic types of life. In: Scherer S (Hg) Typen des Lebens, Pascal Verl. Berlin, S. 11–30.
Cichlids of the Rift Lakes. Sci. Am. 280, 64–69.
The rapid evolution of reproductive proteins. Nature Rev. Genet. 3, 137–144.
Origin of the superflock of cichlid fishes from Lake Victoria, East Africa. Science 300, 325–329.
On the tendency of varieties to depart indefinitely from the original type. The Ternate Essay. J. Proc. Linnean Soc. 3, 53–62.
Predicting the risk of extinction through hybridization. Conservation Biol. 15, 1039–1053.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 6/21/21
Webmaster