Themen • Kurzbeiträge • Streiflichter
Leben aus der Tiefe der Erde: Fortschritt in der Lebensursprungsfrage?
von Boris Schmidtgall
Studium Integrale Journal
27. Jahrgang / Heft 2 - Oktober 2020
Seite 112 - 116
Zusammenfassung: Seit der Zeit Darwins galt das Modell des „warmen Tümpels“ als ein Favorit unter den Szenarien der Lebensentstehung. Doch nach über 70 Jahren experimenteller Forschung steht fest, dass dieses Modell in vielerlei Hinsicht problematisch ist. Aus diesem Grund hat eine Forschungsgruppe ein neues Modell aufgestellt: Leben soll demnach tief unter der Erde entstanden sein. Vor nicht langer Zeit wurden Versuche in einer Druckkammer durchgeführt, um das Modell zu untermauern. Wie so oft besteht eine auffällige Diskrepanz zwischen der Deutung der Ergebnisse und den zugrundeliegenden Daten.
• • • • • • •
Einleitung
Einer der wichtigsten gedanklichen Impulse für das Forschungsgebiet der „chemischen Evolution“ stammt von Charles Darwin selbst. In einem seiner Briefe spekulierte er fragend darüber, ob in einem kleinen warmen Tümpel aus verschiedenen anorganischen Salzen und organischen Verbindungen Leben hervorgegangen sein könnte. Später wurde dieser Gedanke von anderen Wissenschaftlern aufgegriffen und durch experimentelle Arbeiten auf Plausibilität hin geprüft. Nach über 70 Jahren intensiver experimenteller Forschung und vielen frustrierenden Ergebnissen konstatierten Wissenschaftler jedoch vermehrt das Naheliegende: In wässriger Lösung ist die Entstehung der Makromoleküle des Lebens, d. h. Proteine und Nukleinsäuren sehr unwahrscheinlich. In aller Deutlichkeit schrieb S. Benner (2012): „Viele chemische Bindungen in der RNA sind bezüglich der Hydrolyse in Wasser instabil. Selbst wenn sie also in Wasser entstehen, werden sie zerfallen.“ In einer kürzlich publizierten Arbeit gaben Damer und Deamer (2020) offen zu: „Sollte aufgrund des oben erwähnten Wasserproblems irgendein katalytisches Polymer, geschweige denn ein so komplexes wie eine primitive ATP-Synthase, ohne die ständige Reparatur und erneute Synthese durch die Enzyme der Biologie zufällig in der Umgebung einer heißen Quelle gebildet werden, würde es bald durch hydrolytische Zersetzung abgebaut werden.“
Aufgrund vieler schwerwiegender Probleme werden seit Langem Alternativen für das Lebensent-stehungsszenario des „warmen Tümpels“ gesucht.
Dabei ist die hydrolytische Zersetzung der Bausteine des Lebens bei weitem nicht das einzige schwerwiegende Problem für hypothetische Szenarien der Entstehung erster Organismen in einem „warmen Tümpel“ an der Erdoberfläche. Auch die harte UV-Strahlung dürfte ein wesentliches Hindernis im Hinblick auf die Bildung erster Lebewesen gewesen sein, denn bei Abwesenheit von Lebewesen dürfte es auch keine vor UV-Strahlung schützende Atmosphäre gegeben haben. Aus diesen Gründen werden seit Langem alternative Ansätze zum „warmen Tümpel“ gesucht. Zuletzt hat eine Forschergruppe von der Universität Duisburg-Essen für einige Schlagzeilen im Hinblick auf die Frage nach dem Ursprung des Lebens gesorgt. Der „Informationsdienst Wissenschaft“ titelte optimistisch: „Möglichen Beginn des Lebens auf der Erde im Labor simuliert.“ In dem Wissenschaftsmagazin „Scinexx“ war im Artikel „Erdkruste statt Ursuppe?“ die Rede davon, dass das Modell eine Alternative zur mittlerweile angeblich für wenig plausibel gehaltenen „klassischen Ursuppe“ sei.
Recht gewagt klingt vor allem die Pressemitteilung der betreffenden Forscher an der Uni Duisburg-Essen: „Es ist das erste Modell zur Entstehung des Lebens, das einen umfassenden Prozess der Zellbildung beschreibt, bei dem die Probleme der Molekülherkunft, Aufkonzentrierung, Energieversorgung und Membranbildung gelöst sind.“ Wenn diese Aussage zutrifft, müsste es sich bei der Arbeit um einen entscheidenden Durchbruch handeln. Was hat es also damit auf sich?
Das experimentelle Konzept

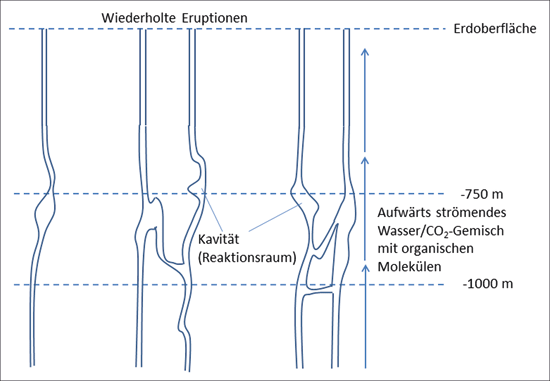
Abb. 1: Veranschaulichung des vermuteten Reaktionsortes: Kanäle und Kavitäten in einer Tiefe von 750–1000 m unter der Erdoberfläche.
Der Geologe Ulrich Schreiber und seine Kollegen Christian Mayer und Oliver J. Schmitz haben für die Fragestellung des Lebensursprungs eine ungewöhnliche Herangehensweise gewählt. Gemäß ihrem Konzept sollen erste Vorstufen des Lebens nicht auf der Erdoberfläche entstanden sein, sondern tief darunter. Die drei Wissenschaftler haben die Hypothese aufgestellt, dass Schritte der Lebensentstehung in Poren und Kavitäten* ca. 750 m – 1000 m unter der Erde in einem Gemisch aus Wasser und CO2 stattgefunden haben können (Mayer et al. 2017, s. Abb. 1). Als wesentliche Verbesserungen gegenüber der vermuteten Entstehung erster Zellen in einem „warmen Tümpel“ an der Erdoberfläche werden folgende Aspekte angeführt:
Der bessere Reaktionsraum. Während die labilen organischen Moleküle an der Erdoberfläche der UV-Strahlung ausgesetzt sind, befinden sie sich in 750–1000 m unter der Erde in einem geschützten Raum. Die Bedingungen in diesem Raum (ca. 40–80 °C, 60–80 bar) passen gut für manche Reaktionsschritte in bisher beschriebenen Szenarien für die Entstehung kleiner organischer Moleküle wie z. B. Aminosäuren.
Das bessere Lösungsmittel. In einer rein wässrigen Lösung, wie sie in einer „Ursuppe“ gegeben ist, sind viele organische Moleküle unlöslich, sodass es nicht zum Aufbau komplexer organischer Moleküle durch chemische Reaktionen kommen kann. Dagegen ermöglichen die Bedingungen in der genannten Tiefe das zeitweise Vorliegen von CO2 in der überkritischen Form (s. Kasten), sodass es sich wie ein organisches Lösungsmittel verhält und Reaktionen ermöglicht, die in einer wässrigen Lösung unmöglich sind. Zudem kommt es beim Phasenübergang (überkritisches CO2 – gasförmiges CO2) zur Bildung winziger Wassertröpfchen, in denen die organischen Moleküle sehr stark aufkonzentriert werden können. Dies kann ebenfalls Reaktionen fördern, die aufgrund der hohen Verdünnung in der Ursuppe nicht stattfinden. Die Phasenübergänge werden durch zyklisch wiederholte Druckschwankungen bewirkt, die z. B. aus Druckentlastungen aufgrund von Eruptionen von Geysiren resultieren.
Die bessere Versorgung mit Rohstoffen. Es wird angenommen, dass unter den genannten Bedingungen nicht nur eine ständige Zufuhr kleiner organischer Moleküle stattfinden kann, sondern dass auch viele Metallionen und andere Rohstoffe vorhanden sind, die an der Erdoberfläche selten vorliegen. Selbst Phosphat soll durch Aufschluss von Apatit unter den Bedingungen in der Tiefe zugänglich sein. Apatit ist ein häufig vorkommendes phosphathaltiges Mineral, das allerdings unter gewöhnlichen Bedingungen an der Erdoberfläche eine viel zu geringe Löslichkeit aufweist, um als Quelle für Phosphat dienen zu können. Phosphationen kommen sehr häufig in biologisch relevanten Molekülen wie Nukleinsäuren, Proteinen und Lipiden vor. Daher ist eine verfügbare Phosphatquelle in Modellen zur Lebensentstehung wichtig.
Ausgehend von diesen theoretischen Überlegungen scheint das Modell in der Tat einige bedeutende Vorteile gegenüber früheren zu bieten. Zudem haben die Autoren einige interessante Experimente durchgeführt, um ihre Hypothese zu überprüfen (Mayer et al 2018).
Überkritischer Zustand
Bei sehr hohen Drücken geht das Kohlendioxid nicht nur in einen Zustand über, in welchem es von seinen Eigenschaften her einem organischen Lösungsmittel ähnlich ist (überkritischer Zustand). Es löst sich auch zu einem viel höheren Anteil im Wasser. Dadurch nimmt die wässrige Lösung einen recht niedrigen pH-Wert von 3 an, sodass Aminogruppen in der positiv geladenen Form vorliegen, wodurch sich ihre wasserliebende Tendenz deutlich erhöht.
Bedingungen der experimentellen Untersuchung der Hypothese
Zur Nachbildung der genannten Bedingungen in 750–1000 m Tiefe wurden chemische Vorgänge in der Reaktionskammer eines Druckreaktors mit einem Wasser/CO2-Gemisch durchgeführt. Zunächst wurde eine wässrige Lösung mit amphiphilen* Fettsäuremolekülen (C18-Ketten), langkettigen aliphatischen Aminen* (C18-Ketten) und einer Auswahl an 12 reinen L-Aminosäuren* versetzt und in die Druckkammer gefüllt (s. Abb. 2). Es wurden dabei nur solche Aminosäuren eingesetzt, die gemäß der Fachliteratur über Simulationsversuche in sog. Miller-Experimenten* nachgewiesen werden konnten. Anschließend wurde CO2 in die Druckkammer gegeben und unter hohen Druck gesetzt, sodass das CO2 den überkritischen Zustand annahm. Die Temperatur in der Druckkammer wurde konstant bei 120 °C gehalten. Dabei wurde der Druck über eine Zeitspanne von 160 Stunden wiederholt zwischen 100 bar und 70 bar zyklisch variiert. Die bei den Versuchen verwendeten Chemikalien (s. o.) wurden in fertiger Form und hoher Reinheit verwendet (>94 %). Das Wasser und das CO2 wurden in noch viel höherer Reinheit verwendet (>99,9 %). In einer weiteren Versuchsreihe wurden dem Gemisch anstelle von Aminosäuren durch chemische Synthese erhaltene Peptide hinzugefügt.
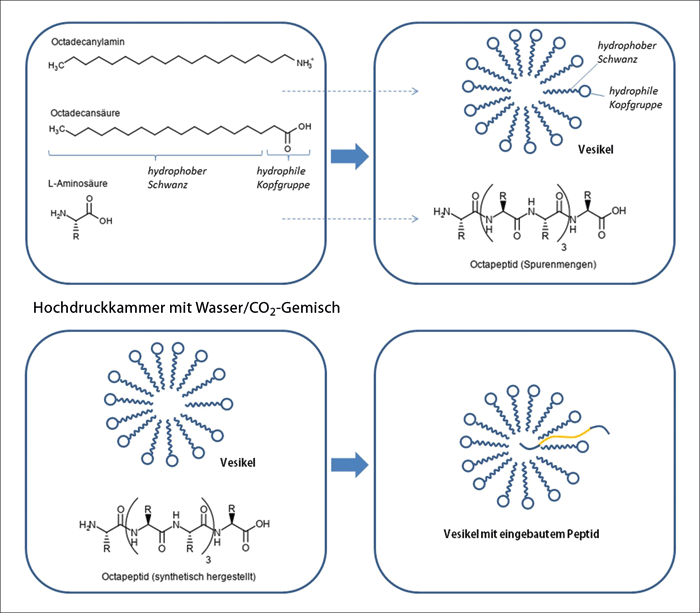
Abb. 2: Schematische Darstellung der zwei von Mayer et al. durchgeführten Versuche in der Druckkammer.
Oben Das Gemisch aus Wasser, CO2, amphiphilen Molekülen (Fettsäure: Octadecansäure, aliphatisches Amin: Octadecanylamin) und L-Aminosäuren bringt bei 120 °C und Drücken von 70–100 bar Vesikel und Peptide einer maximalen Länge von acht Aminosäuren hervor.
Unten Werden unter den gleichen Bedingungen Vesikel und Peptide in ausreichender Menge vorausgesetzt, kommt es zur Bildung von Vesikeln mit integrierten Peptiden in der Vesikelmembran. Dabei ordnet sich das Peptid so an, dass der fettliebende Teil (orange) sich in der Membran befindet, während die wasserliebenden Enden (blau) aus der Membran herausragen.
Befunde
Zur Synthese von Peptiden* aus Aminosäuren wurde der Reaktionsansatz 160 Stunden bei 120 °C gerührt. Dabei wurden wiederholt Proben aus der Kammer des Druckreaktors entnommen. Es konnten Peptide bis zu einer Länge von acht Aminosäuren nachgewiesen werden. Unter den genannten Bedingungen kam es also tatsächlich zur Bildung von Peptidbindungen zwischen den Aminosäuren ohne Zusatz spezieller Reagenzien, die solche Reaktionen fördern. Allerdings war die Konzentration der erhaltenen Peptide sehr niedrig. In manchen Versuchen lag sie nur knapp über der Nachweisgrenze des verwendeten Massenspektrometers, was vereinfacht mit den Worten „verschwindend gering“ ausgedrückt werden kann. Daher wurde für die Demonstration der „Selbstorganisation von Vorstufen von Zellen“ in weiteren Versuchen ein im Labor synthetisiertes Peptid verwendet.
Bei den Versuchen mit vorgegebenen Peptiden erhielt man kurzlebige Vesikel, die nach jedem Druckzyklus zerfielen. Bei Vesikeln handelt es sich um kugelförmige Aggregate mit innerem Hohlraum, die von amphiphilen Molekülen wie Lipiden oder Fettsäuren gebildet werden können. Die im Versuch verwendeten Fettsäuren richten sich dabei so aus, dass der wasserliebende „Kopf“ mit der wässrigen Phase in Kontakt stehend nach außen orientiert ist, während der fettliebende „Schwanz“ ins Innere des Vesikels weist. Bei den Versuchen wurde auch beobachtet, dass bestimmte Peptide in die Membran der Vesikel eingebaut werden. Es handelte sich hierbei um Peptide, die an den Enden jeweils eine bis drei polare Aminosäuren enthalten und in der Mitte der Sequenz wasserabweisende Aminosäuren. Solche Peptide ordneten sich dergestalt in den Vesikeln an, dass der mittlere hydrophobe Teil in der Membran eingebettet war und der hydrophile Kopf mit dem Lösungsmittelgemisch in Kontakt stand. Im Verlauf der Druckzyklen entstanden kombinierte Agglomerate aus Fettsäuren/Peptiden, die mehrere Zyklen überdauerten. Die Aufnahme bestimmter Peptide führte also zur Stabilisierung der Vesikel. Peptide, die entweder nur aus wasserliebenden Aminosäuren bestanden oder nur aus wasserabweisenden, blieben dagegen nicht in den Vesikeln erhalten.
Bildung von Peptiden aus Aminosäuren in Spurenmengen und Bildung von Vesikeln mit integrierten Peptiden = „molekulare Evolution“?
Die Autoren werteten die Ergebnisse als Beleg für die Möglichkeit der Entstehung und Selbstoptimierung eines molekularen Systems unter präbiotischen Bedingungen: „Wir zeigen, dass wachsende Strukturen […] ihre eigene Existenz unterstützen, chemische und strukturelle Evolution eingehen und unvorhergesehene funktionelle Eigenschaften entwickeln“ (Mayer et al. 2018). Insgesamt sehen die Autoren in ihrem Modell und den durchgeführten Experimenten eine plausible Veranschaulichung eines Szenarios der Lebensentstehung. In der Zeitschrift der Universität Duisburg-Essen Unikate beschreiben sie ihr System wie folgt: „…eine große Anzahl von kleinsten Laboratorien, untereinander verknüpft, mit wechselnden Bedingungen, Materialnachschub und Müllabfuhr für nicht brauchbare Bestandteile. Unter solchen Bedingungen muss sich die biologische Zelle LUCA gebildet haben, das erfolgreichste System, das jemals auf der Erde entstanden ist“ (Schreiber et al. 2018).
Glossar
Aliphatisches Amin: Kettenförmiges oder verzweigtkettiges Kohlenwasserstoff-Molekül (s. Abb. 1) mit einer NH2-Gruppe (Amin). Amphiphile Moleküle: besitzen einen wasserliebenden und einen fettliebenden Teil. enantiomerenrein: Wenn von einem Molekül zwei Formen möglich sind, die sich wie Bild und Spiegelbild verhalten, spricht man von zwei „Enantiomeren“. Liegen nur Moleküle der einen spiegelbildlichen Form vor, liegt es in „enantiomerenreiner Form“ vor. Evolutionsexperiment: Experiment, bei dem das Ergebnis nicht bereits durch die gewählten spezifischen Bedingungen von vornherein feststeht und bei dem eine signifikante Entwicklung von einfach zu komplex beobachtet werden kann. Kavität: In dem hier gegebenen Kontext eine kleine Aushöhlung im Gestein, in der sich Moleküle ansammeln können. L-Aminosäuren: Aminosäuren können bezüglich des zentralen Kohlenstoff-Atoms in zwei → enantiomeren Formen vorliegen: D-Form oder L-Form (s. Abb 1). Miller-Experiment: Ein chemisches Experiment, das dazu dienen sollte, die Entstehung von Aminosäuren nachzuvollziehen – durch Blitzentladungen in einem Gasgemisch, welches die hypothetische Ur-Atmosphäre simulieren soll. Peptid: Die Verknüpfung mindestens zweier Moleküle über die Einheit-C(O)NH- wird als „Peptid“ bezeichnet. Das ist auch bei den Verknüpfungen von Aminosäuren in Proteinen gegeben. Kurze Aminosäureketten werden vereinfacht als „Peptide“ bezeichnet.
Kritik und Diskussion
Besonders auffällig sind die gezielte Wahl der Versuchsbedingungen und die ausschließliche Verwendung hochreiner und sehr spezifischer Chemikalien. Die Verwendung von reinen L-Aminosäuren bei Versuchen zur Bildung von Peptiden ist absolut notwendig, um überhaupt annähernd natürliche Peptide zu erhalten. Andererseits ist unter präbiotischen Bedingungen nicht davon auszugehen, dass Aminosäuren chemisch rein und auch noch in enantiomerenreiner* Form vorliegen könnten. Vor allem die Lösungsmittel Wasser und CO2 wurden in einer sehr hohen Reinheit verwendet, die unter natürlichen Bedingungen vollkommen ausgeschlossen ist. Für den (bescheidenen) Erfolg der chemischen Reaktionen war dies allerdings unverzichtbar, denn Verunreinigungen der Lösungsmittel fallen bei chemischen Reaktionen besonders ins Gewicht. Kontrollversuche mit verunreinigten Lösungsmitteln und Chemikalien wurden leider nicht durchgeführt. Das wäre jedoch hilfreich, um einschätzen zu können, wie empfindlich das chemische System auf Verunreinigungen reagiert. Dass aber selbst unter nahezu optimalen Bedingungen die Bildung von Peptiden nur in Spuren nachweisbar ist, wirkt nicht überzeugend. Ausgehend von früheren Experimenten ist es keineswegs überraschend, dass keine durchgängige chemische Evolution ausgehend von Fettsäuren und Aminosäuren hin zu Vesikeln mit integrierten Peptiden erfolgt ist. Stattdessen bestätigt sich einmal mehr das typische Muster der Vorgehensweise in der präbiotischen Chemie: Es werden bestimmte kleine Teilschritte simuliert (Synthese von Peptiden in Spurenmengen), aber das eigentliche Problem wird durch Laborsynthese gelöst (Synthese von Peptiden in ausreichender Menge).
Auch für die Versuche zur Bildung der Vesikel wurden die Bedingungen so gewählt, dass das erhoffte Resultat auch erzielt wurde, ja fast vorprogrammiert war. Die Kombination aus Lösungsmittelgemisch und Druck wurde offenbar so eingestellt, dass die Vesikelbildung stark gefördert wird. Die Autoren beschreiben selbst, dass die Vesikelbildung bei dem eingestellten sauren pH-Wert zu erwarten war – bei neutralem pH-Wert dagegen nicht: „Eine 1:1 Mischung aus Oktadekansäure und Oktadekanylamin weist einzigartige physikalische Eigenschaften auf, die dessen Tendenz zur Vesikelbildung bei einem bestimmten pH-Wert der wässrigen Lösung beeinflussen. Während bei neutralem pH-Wert keine Vesikel gebildet werden, führt eine beliebige Abweichung zur Deprotonierung der Carboxylgruppen der Oktadekansäure oder einer Protonierung der Amine. Folglich kommt es zur Ionisierung der Kopfgruppen und damit zur Bildung von Vesikeln“ (Mayer et al 2018). Aufgrund der hohen Temperatur bei der Reaktionsführung konnten nur thermisch stabile Verbindungen für die Entstehung der Vesikel verwendet werden. Die Autoren beschreiben selbst, wie sie Chemikalien ausgewählt haben, die unter den vorgesehenen Versuchsbedingungen stabil sein würden: „Um die Temperaturstabilität zu erhöhen, wurden beide Komponenten als C18-Ketten ausgewählt (Oktadekansäure und Oktadekanylamin)“ (Mayer et al 2018). Die Analyse der experimentellen Bedingungen zeigt erneut deutlich, dass es sich nicht um ein „Evolutionsexperiment“* handelte, sondern um gezielte Reaktionsführung, also um Design.
Darüber hinaus sind die Ergebnisse ohnehin sehr bescheiden, denn dass amphiphile Moleküle (Fettsäuren oder Alkyamine) unter bestimmten Bedingungen in wässriger Lösung spontan Vesikel bilden können, ist nichts Neues. Die spontane Integration von Peptiden in die Vesikelmembran ist zwar ein interessantes Ergebnis, hat aber entgegen der Behauptung der Autoren nicht viel mit der Entstehung und Weitergabe von „lebenswichtigen Funktionen“ zu tun. Dazu müsste gezeigt werden, wie aus einzelnen Peptiden ganze Transmembranproteine werden, die z. B. einen selektiven Stofftransport ermöglichen, und wie sich die Vesikel teilen und dabei ihre Eigenschaften beibehalten. Auch die Tatsache, dass bestimmte Vesikel mehrere Druckzyklen überstehen, ist noch lange keine „molekulare Evolution“, sondern schlichte Thermodynamik: Das bei bestimmten Bedingungen stabilste Molekül oder Agglomerat bleibt bestehen. Dass die Peptide die Stabilität der Membran erhöhen, ist einfach das Resultat einer Assoziation zweier Makromoleküle. Die Rede von einer „evolutionären Entwicklung von einfachen Vorstadien zu komplexeren“ oder von „Selektionsvorteilen“ ist hier irreführend, da es sich nicht um Lebewesen handelt, sondern um relativ einfache molekulare Gebilde, die keinerlei Tendenzen zur Ausbildung tatsächlicher molekularer Funktionseinheiten wie z. B. Rotoren oder Molekularpumpen aufweisen.
Schließlich gibt es überhaupt keine Anhaltspunkte, wie unter den von Mayer et al. angeführten Bedingungen genetisches Material entstehen könnte – ganz zu schweigen von einem funktionierenden Proteinbiosynthese-Apparat. Es wundert nicht, dass Schreiber in seinem Buch „Das Geheimnis um die erste Zelle“ schreibt, dass der Tag, an dem erste Schritte zur präbiotischen Proteinbiosynthese verstanden werden, gefeiert werden sollte: „Sollte dieser Prozess einmal im Labor nachvollzogen werden, wäre es an dieser Stelle angebracht, eine Flasche Champagner zu öffnen“ (Schreiber 2019). Die Resultate der Experimente jedenfalls rechtfertigen diese Hoffnung in keiner Weise. Noch muss die Champagnerflasche auf unabsehbare Zeit im Kühlschrank verbleiben.
Fazit
Die Verwendung aufwendiger Reaktions-bedingungen und hochreiner Chemikalien entspricht Design und nicht Evolution.
Die Befundlage ermöglicht also bei weitem nicht die vollmundigen Schlussfolgerungen von Mayer et al. Die Behauptung, dass „Vorstufen von Zellen“ identifiziert seien, ist insofern grob irreführend, als die erhaltenen makromolekularen Agglomerate in keiner Weise über typische Eigenschaften von Lebewesen (z. B. Stoffwechsel, genetisches Material, Reaktion auf Reize) verfügen. Der Gebrauch überaus anspruchsvoller experimenteller Vorgehensweisen inklusive hochreiner und spezifischer Chemikalien für die Synthese von sehr primitiven zellähnlichen Gebilden bestätigt aber erneut, dass Schöpfung die einzig plausible Erklärung für den Ursprung des Lebens ist.
Die Interpretation der Befunde durch Mayer, Schreiber und Schmitz ist mehr als fragwürdig. Vor allem die Wahl der Begriffe ist oft suggestiv und unangemessen. Es wird ein Vokabular auf abiotische (rein physikalisch-chemische) Vorgänge angewendet, das ansonsten nur für Lebewesen gebräuchlich ist. Dadurch wird die Grenze zwischen unbelebter Materie und belebter mittels bloßer Rhetorik verwischt. Damit wird Lesern, die die experimentellen Details der Arbeit nicht nachvollziehen können, fälschlicherweise vermittelt, dass die Lösung der Frage, wie Leben durch rein natürliche Vorgänge entstanden sein könnte, zum Greifen nahe sei. Dabei wäre es angebracht zu konstatieren, dass die Befunde vielmehr zur Verschärfung der Probleme beitragen.
Asphalt, Water, and the Prebiotic Synthesis of Ribose, Ribonucleotides, and RNA. Acc. Chem. Res. 45, 2025–2034.
The Hot Spring Hypothesis for an Origin of Life, Astrobiology, 20(3), doi: 10.1089/ast.2019.2045.
Selection of Prebiotic Molecules in Amphiphilic Environments, Life 7(3), doi:10.3390/life7010003.
Molecular Evolution in a Peptide-Vesicle System, Life 8(16), doi:10.3390/life8020016.
Der Ursprung des Lebens. „Die“ Herausforderung der Wissenschaft. Unikate 51.
Das Geheimnis um die erste Zelle. Dem Ursprung des Lebens auf der Spur. Springer, S. 231.
Informationsdienst Wissenschaft: https://nachrichten.idw-online.de/2020/06/12/moeglichen-beginn-des-lebens-im-labor-simuliert-evolution-unter-tage/ abgerufen am 14. 7. 2020.
Erdkruste statt Ursuppe? Erste Zellmembranen könnten unterirdisch entstanden sein. https://www.scinexx.de/news/biowissen/erdkruste-statt-ursuppe/, abgerufen am 18. 6. 2020.
Das Leben entstand in der Erdkruste. https://www.uni-due.de/geologie/forschung/origin.shtml, abgerufen am 18. 6. 20.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 6/28/21
Webmaster