Neues über Lebensentstehung? Oder von der Überinterpretation einfacher chemischer Systeme
Wie aus unbelebter Materie Leben entstehen konnte, ist eine der großen Fragen der Wissenschaft. Zum einen sind sich selbst vervielfältigende (replizierende) Moleküle für den Übergang von der Chemie zu lebenden Systemen notwendig, zum anderen müssen sie aber auch in einen Stoffwechsel eingebunden sein. Chemische Systeme, die entweder replizieren oder stoffwechselähnliche Reaktionen durchführen, wurden bereits im Labor von Chemikern (gezielt) erzeugt, und einige können sogar bei Zugabe von Chemikalien oder unter veränderten Randbedingungen von einer Funktion zur anderen wechseln. Leben braucht jedoch beides gleichzeitig.
Die niederländische Forschungsgruppe um Sijbren Otto beschäftigt sich seit über einem Jahrzehnt mit diesen Fragen. Otto ist nicht daran interessiert, herauszufinden, wie Leben einst entstanden sein könnte, ihn interessiert vielmehr die Frage, ob man das Leben selbst gestalten kann. Dabei ist es ihm gleichgültig, ob es auf DNA, RNA oder Proteinen basiert oder nicht (persönliche Mitteilung). Im Laufe der Zeit hat sich seine Arbeitsgruppe einige ausgeklügelte selbstreplizierende chemische Reaktionen ausgedacht (Colomb-Delsuc et al. 2015, Sadownik et al. 2016). Das von ihnen entwickelte sich replizierende System besteht aus ringförmigen Molekülen, die so konzipiert sind, dass sie in Lösung Stapel bilden. Durch mechanische Beanspruchung (Rühren der Lösung) brechen die Stapel und die Stapelfragmente können jeweils weiterwachsen. Das System stellt eine sehr simple Modellierung der Replikation von biologischen Systemen dar, hat dabei aber den Vorteil, dass es leicht mathematisch beschreibbar ist.

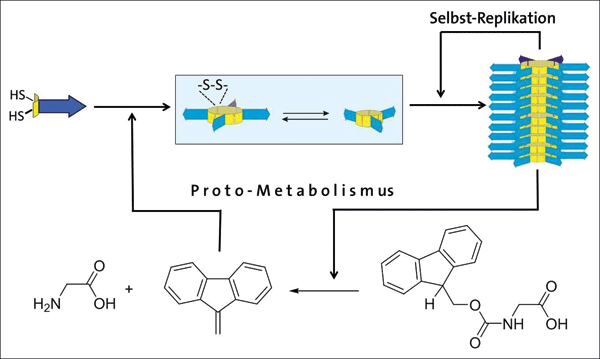
Abb. 1: Ottos selbstreplizierendes System aus sechsgliedrigen Ringen (Hexameren) hat einen einfachen „Metabolismus“, bei dem es die Bildung eigener Bausteine aus Peptiden (blau) mit einer aromatischen Dithiolgruppe (gelb) katalysiert. Aus sechs Bausteinen bilden die Ringe schließlich Stapel. Diese Stapel wachsen und vervielfältigen sich durch Zerbrechen, was zur Replikation der Hexameren führt.
Nun beschreibt diese Gruppe in ihrem Modellsystem eine Art „Stoffwechsel“ in Molekülen. Sie beobachteten, dass die von ihnen verwendeten Replikator-Moleküle eine Reaktion katalysieren, bei der Verbindungen entstehen, die helfen, die eigenen Bausteine des Replikators herzustellen (Ottelé et al. 2020). Es zeigte sich, dass die Stapel aus ringförmigen Molekülen (Replikator) eine Reaktion (Abspaltung einer Schutzgruppe von der Aminosäure Glycin) katalysieren, während die einzelnen Bausteine dies nicht können. Das kommt daher, dass im Stapel zusammengelagerte positive Ladungen (Seitenketten) dicht beieinander sitzen, was lokal eine hohe Basizität erzeugt und damit die Entfernung der Schutzgruppe begünstigt. Dazu reichen die positiven Ladungen an den einzelnen ringförmigen Molekülen nicht aus. In einem populären Hinweis auf die aktuellen Arbeiten schreibt Krämer (2020): „Es könnte eines der lebensechtesten chemischen Systeme sein, das je geschaffen wurde, da es zwei der drei wesentlichen Merkmale des Lebens – Replikation, Metabolismus und Abschottung – kombiniert.“
Ist diese Art von Experimenten für das Verständnis des Ursprungs des Lebens auf der Erde, wie wir es kennen, relevant? Otto schrieb in einem persönlichen E-Mail-Austausch: „Die derzeitigen Systeme werden außerhalb des Labors nicht lange überleben, geschweige denn dort Material zur Reproduktion finden. Die Frage, ob ähnliche [auf begrifflicher Ebene ähnliche, aber auf anderen Molekülen basierende] Systeme spontan entstehen könnten, ist schwieriger zu beantworten. Meiner Meinung nach ist jedoch das spontane Auftauchen [eines solchen Systems] weniger problematisch als das spontane Auftauchen eines Systems, das der heutigen Biochemie ähnelt.“
Tatsächlich verwendet Ottos Gruppe eine recht großzügige Definition von „Selbstreplikator“, die mit der Replikation von Biopolymeren im Leben nichts zu tun hat.
Dennoch soll diese Arbeit zur weiteren Forschung zur Entstehung von Leben aus Nichtleben (Abiogenese) ermutigen. Einige schwerwiegende Einschränkungen für die Anwendung des Begriffs „Selbstreplikator“ auf die Abiogenese seien hier genannt. Erstens: die Ausgangsmonomere (Einzelbauteile; kurze Polypeptide, die mit einem Benzoldithiol verbunden sind) sind gereinigte, konzentrierte, intelligent ausgewählte Moleküle mit einer intrinsischen Fähigkeit zur Aggregation. Diese Bedingungen sind weit von dem entfernt, was in präbiotischen Umgebungen der jungen Erde erwartet wird. Zweitens verbinden sich die Ausgangsmonomere nicht kovalent zu einem Polymer (wie in RNA, DNA oder Proteinen); sie ziehen sich lediglich an, um eine makromolekulare Einheit zu bilden. Mechanische Störungen brechen das wachsende Makromolekül auf, um eine erhöhte Anzahl von Stellen zu ermöglichen, die anschließend die Moleküle wachsen lassen (die Stapelbruchstücke können in Gegenwart ausreichender Mengen an Replikatoren jeweils an beiden Enden weiterwachsen. Dies wird als „Selbst-Replikation“ bezeichnet). Dieser Vorgang gleicht jedoch viel mehr einem Kristallwachstum als der Replikation eines Biopolymers.
Die Neuheit in diesem Artikel besteht darin, dass in der Struktur des aggregierenden Stapels katalytische Fähigkeiten vorhanden sind, die dann die Wachstumsrate dieses Makromoleküls weiter aufrecht erhalten. Wie oben von Otto selbst anerkannt, unterscheidet sich diese Struktur aber völlig von den Systemen, die in Lebewesen vorkommen. Aber sie soll wenigstens ein Prinzip aufzeigen, das für die Abiogenese erforderlich ist. Die Tatsache, dass diese Arbeit in Nature Catalysis veröffentlicht wurde, zeugt davon, wie unkritisch Arbeiten in renommierten wissenschaftlichen Journalen akzeptiert werden, wenn darin der Eindruck erweckt wird, dass irgend ein Beitrag zum Verständnis einer möglichen Lebensentstehung präsentiert wird.
P. Borger
[Ottelé J, Hussain AS, Mayer C & Otto S (2020). Chance emergence of catalytic activity and promiscuity in a self-replicator. Nature Catalysis 3, 547–553 • Krämer K (2020) Self-replicating molecules show signs of metabolism for the first time. https://www.chemistryworld.com/news/self-replicating-molecules-show-signs-of-metabolism-for-the-first-time/4012152.article • Colomb-Delsuc M, Mattia E, Sadownik JW & Otto S (2015) Exponential self-replication enabled through a fibre elongation/breakage mechanism. Nat. Commun., doi:10.1038/ncomms8427 • Sadownik JW, Mattia E, Nowak P & Otto S (2016) Diversification of self-replicating molecules. Nat. Chem. 8, 264–269.]