
Themen • Kurzbeiträge • Streiflichter
Primeln und Lungenkraut im Frühlingswald
Wie Supergene die Polyvalenz von Grundtypen nahelegen
von Peter Borger
Studium Integrale Journal
27. Jahrgang / Heft 1 - Mai 2020
Seite 20 - 28
Zusammenfassung: Naturfreunde staunen über die beiden Blütentypen der Schlüsselblumen (Primeln) und anderer Blütenpflanzen. Hinter dem Phänomen der Verschiedengriffligkeit (Heterostylie) stecken aber auch spannende genetische Grundlagen, die interessante Aspekte des Erbguts offenbaren und für eine geplante Konstellation sprechen.
• • • • • • • • • • •
Einleitung
Wer im Frühlingswald schon einmal Schlüsselblumen oder das Lungenkraut mit einer Lupe näher betrachtet hat, hat vielleicht die beiden unterschiedlichen Blütentypen entdeckt. Manche Blüten besitzen lange Griffel und tief ansitzende Staubblätter, andere haben kurze Griffel und hoch ansitzende Staubblätter (Abb. 1). Der Einfachheit halber sollen die beiden Staubblatttypen als „kurz“ und „lang“ bezeichnet werden. Die Kombination aus langem Griffel mit kurzen Staubblättern nennt man den L (Lang)-Phänotyp (bzw. für „long“), während die Kombination aus einem kurzen Griffel und langen Staubblättern als K (Kurz)-Phänotyp* bezeichnet wird (bzw. üblicherweise S für „short“). Diese Zweiförmigkeit wird in der Botanik als Heterostylie (Verschiedengriffligkeit) bezeichnet.
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.

Kompakt
Heterostylie (Verschiedengriffligkeit) ist ein faszinierendes Merkmal von Blüten in einer Vielzahl von Pflanzenfamilien und dient dazu, Inzucht zu verhindern. Bei der verbreitetsten Ausprägung der Heterostylie entwickeln Pflanzen entweder Blüten mit kurzem Griffel und oben in der Kronröhre ansitzenden Staubblättern (K-Typ) oder mit langem Griffel und unten in der Kronröhre ansitzenden Staubblättern (L-Typ). Die Tatsache, dass man ausschließlich Pflanzen mit entweder K- oder L-Typen beobachtet, deutet auf die Beteiligung nur eines einzigen Gens hin. Eine Besonderheit besteht jedoch darin, dass mehrere klar abgegrenzte Merkmale (Griffellänge, Staubblattposition, Pollenkorngröße) gleichzeitig ausgeprägt sind, was auf mindestens drei Gene schließen lässt. Es hat sich herausgestellt, dass Heterostylie durch einen einzigen genetischen Locus (Genort) mit fünf Genen bestimmt wird, der als ein einziges Supergen vererbt wird. Nach evolutionstheoretischen Vorstellungen ist dasselbe Supergen 6-mal unabhängig in unterschiedlichen Pflanzenfamilien entstanden, ein Phänomen, das als Konvergenz gedeutet wird. Die molekulargenetischen Beobachtungen legen jedoch nahe, dass die zugrunde liegende Genetik als Beleg für programmierte Variabilität (Polyvalenz) gewertet werden kann.
Eine kleine Geschichte der Heterostylie
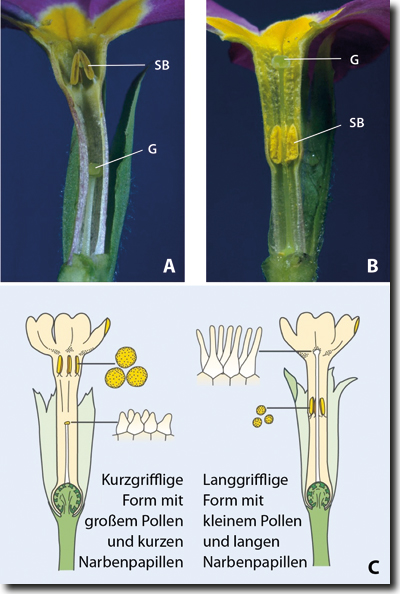
Abb. 1: Heterostylie bei Gartenprimeln.
A Längsschnitt durch eine Blüte des K-Typs. Die Blüte hat einen kurzen Griffel (G) und hoch platzierte Staubbeutel (SB).
B Längsschnitt durch eine Blüte des L-Typs. Die Blüte hat einen langen Griffel und niedrig platzierte Staubbeutel.
C Die zwei Blütentypen der Wald-Schlüsselblume in einem stark schematisierten Längsschnitt. Erläuterungen im Text. (Aus Junker & Wiskin 2017)
Die erste Beschreibung dessen, was wir heute als Heterostylie bezeichnen, geht auf eine lateinische Veröffentlichung von Carolus Clusius, einem flämisch-niederländischen Botaniker des 16. Jahrhunderts, zurück. In einer frühen Veröffentlichung seines Buches Rariorum aliquot Stirpium, per Pannoniam, Austriam, & vicinas quasdam Provincias observatarum Historia beschreibt er im Jahr 1583 die zwei unterschiedlichen Blütentypen, nicht nur für Primeln, sondern auch für mehrere andere Arten (einen Überblick über die Geschichte der Erforschung der Heterostylie liefert Gilmartin 2015). Der berühmte Botaniker Carolus Linnaeus übersah offenbar die Heterostylie, denn in seiner Arbeit Systema Naturae von 1787 beschreibt er nur den L-Phänotyp für Primula. Auch in seinen anderen Werken finden sich keine Erwähnungen der unterschiedlichen Typen der Primelblüten. Erst 1818 präsentierte der französische Naturforscher Pierre Jean Francoise Turpin Bilder von Primeln, die die L- und K-Phänotypen zeigen, etwa zeitgleich mit dem britischen Botaniker J. S. Henslow, der 1826 beide Blütentypen zeichnete.
Obwohl mehrere Naturforscher die beiden Blütentypen beschrieben oder gezeichnet hatten, erkannten sie ihre Bedeutung nicht. Es erforderte einen ausgezeichneten Beobachter, der die typischen Blüten der Primeln interpretierte: Charles Darwin. Im Jahr 1860 schrieb Darwin in einer Reihe von Briefen an seinen Freund und Vertrauten J. D. Hooker und an den Botaniker J. S. Henslow, dass er zwei Primelarten untersucht hatte und dass diese konsequent zwei Blütentypen hervorbrachten. Henslow erzählte er weitere Details und berichtete, dass beide Arten in zwei Formen von etwa gleicher Anzahl existieren, die männlich oder weiblich zu sein schienen. Für die eine Form, das vermeintlich weibliche Exemplar, beschrieb Darwin kurze Staubfäden, kleine längliche Pollenkörner und einen über die Staubblätter hinausragenden langen Griffel mit langen Narbenpapillen. Von der zweiten Form, der vermeintlich männlichen, beschrieb er lange Staubfäden, große runde Pollenkörner und einen kurzen Griffel mit kurzen Narbenpapillen (Abb. 1).
Im November 1861 stellte Darwin seine Beobachtungen der Linnaean Society vor. Sein Artikel, On the two forms, or dimorphic condition, in species of Primula, and on their remarkable sexual relations, wurde ein Jahr später publiziert. Darwin erkannte, dass die verschiedenen Blütentypen unterschiedliche Fortpflanzungssysteme darstellen, die er „distyly“ nannte. Er fand auch heraus, dass beide Blütentypen zwittrig sind und dass „Der Pollen von A für den Griffel von B angepasst ist, und umgekehrt“.1 In den folgenden Jahren veröffentlichte Darwin weitere Arbeiten über Heterostylie, insbesondere dessen Vorkommen beim Lein (Linum) und bei den Weiderich-Arten (Lythrum). Im Jahr 1877 stellte er seine Forschungen zum Thema Heterostylie im Buch Different Forms of Flowers zusammen. Aufgrund dieser Arbeiten wird Darwin weithin als erster angesehen, der die Heterostylie bei Primeln näher untersuchte und die funktionelle Bedeutung der beiden Blütentypen herausfand (Gilmartin 2015).
Glossar
Allel: Erscheinungsform eines Gens. Centromer: Bereich der primären Einschnürungsstelle (die sog. „Wespentaille“) eines Metaphase-Chromosoms. Duplikation: Verdopplung einer DNA-Sequenz. exprimieren: Ablesen und Nutzen von Genen. Genom: Das gesamte Erbgut eines Organismus. hemizygot: DNA-Region, die nur einmal (mono-allelisch) im diploiden Genom vorkommt. heterozygot: Ein Organismus ist heterozygot für ein Merkmal, wenn zwei unterschiedliche Kopien (Allele) eines bestimmten Gens auf den homologen Chromosomen vorliegen. homozygot: Ein Organismus ist homozygot für ein Merkmal, wenn zwei gleiche Kopien (→ Allele) eines bestimmten Gens auf den beiden homologen Chromosomen vorliegen. Locus (Plural: Loci): In der Genetik die physische Position eines Gens im Genom. Neofunktionalisierung: Hypothetischer Vorgang, bei dem eine duplizierte DNA-Sequenz eine neue Funktion erwirbt (durch Ansammlung von Mutationen). Phänotyp: Erscheinungsbild mit sämtlichen Merkmalen eines Organismus. Phylogenetische Rekonstruktion: Ermittlung mutmaßlicher Abstammunglinien. Polyvalenz: In Grundtypen ist nicht nur eine einzige, festgelegte genetische Ausstattung vorhanden, sondern das Erbgut ist ausgeprägt mischerbig und mit genetischen Programmen zur Variabilitätserzeugung ausgestattet. Referenzgenomsequenz: Das öffentlich zugängliche, repräsentative, digital gespeicherte Musterbeispiel für den vollständigen Satz und die Reihenfolge der Gene einer Spezies. Supergen: Chromosomenabschnitt mit mehreren hochverknüpften individuellen Genen, die zusammen einen integrierten Phänotyp mit mehreren Merkmalen steuern. Transkriptom: Momentaufnahme der gesamten RNA-Transkripte, die in einer Zelle oder Gewebe vorhanden sind. Transkriptomanalyse: Studie zur Bestimmung des → Transkriptoms.
Funktion der Heterostylie
Pflanzen mit Heterostylie besitzen oft sogenannte Stieltellerblumen, deren unterer Teil röhrenförmig ausgebildet ist. Dabei sind die Staubfäden mit der Blütenröhre verwachsen. Beim L-Phänotyp führt dies dazu, dass die Staubbeutel in der Blütenröhre in einer niedrigen Position befestigt sind. In Blüten des K-Phänotyps sind die Staubbeutel dagegen viel weiter oben in Richtung der Öffnung der Blütenröhre positioniert (Ganders 1979). Man kann sich schon denken, wozu diese Einrichtung gedacht ist: Blüten besuchende Insekten transportieren den Pollen von den kurzen Staubblättern zu den Blüten mit kurzen Griffeln; entsprechend erfolgt der Transport des Pollens bei den Blüten mit langen Staubblättern und langen Griffeln. Die Höhe der kurzen bzw. langen Blütenorgane ist passend aufeinander abgestimmt, so dass der Pollen gezielt auf das Narbengewebe gelangen kann. Nur der Fremdpollen ist in der Lage, auf den Narben auszukeimen. Die Selbstbestäubung wird zusätzlich dadurch verhindert, dass die beiden Blütentypen verschieden gestaltete Pollenkörner produzieren und die Narbenoberflächen unterschiedlich gestaltet sind: Kurzgrifflige Blüten besitzen oben in der Kronröhre positionierte Staubbeutel, in denen viel größere Pollenkörner gebildet werden als in den in der Mitte positionierten Staubbeuteln der langgriffligen Blüten. Und die Narben der letzeren haben lange Papillen, die der ersteren kurze. Die Blütenorgane der beiden Blütentypen sind also genauestens aufeinander abgestimmt (Junker & Wiskin 2017, 43).
Heterostylie hat einen doppelten Nutzen: Es verhindert die Selbstbestäubung und fördert die sexuelle Fortpflanzung.
Die räumliche Trennung der an der Bestäubung beteiligten Fortpflanzungsorgane (Griffel und Staubblätter) innerhalb einer Blüte, wie sie z. B. bei Primula vorliegt, bezeichnet man auch als Herkogamie. Im vorliegenden Fall handelt es sich um reziproke Herkogamie, d. h. die Position der männlichen und weiblichen Organe bei den Blüten der beiden verschiedenen Morphen stimmt überein (Abb. 1 und 2). Diese Konstellation ist speziell darauf ausgelegt, Pollenverschwendung zu reduzieren und die Fremdbestäubung zu fördern. Heterostylie hat also einen doppelten Nutzen: Sie verhindert die Selbstbestäubung und fördert die sexuelle Fortpflanzung. In evolutionärer Deutung heißt es, die Heterostylie fördere sowohl die männliche als auch die weibliche Fitness (Barrett & Shore 2008).
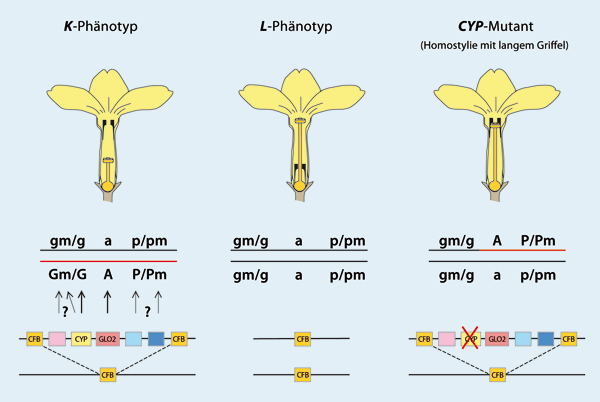
Abb. 2: Genetische Grundlagen der Heterostylie.
Oben: Schematische Darstellung des K-Phänotyps (links) und des L-Phänotyps (Mitte) zur Veranschaulichung der gegenseitigen Herkogamie (räumliche Trennung von Blütenorganen). Es gibt eine räumliche Übereinstimmung zwischen der Narbe des K-Typs und den Staubbeuteln des L-Typs sowie zwischen der Narbe des L-Typs und den Staubbeuteln des K-Typs.
Mitte: Das klassisch-genetische Modell für den S-Locus mit zwei Allelen, der fünf Gene enthält: G Griffellänge, Gm weibliche Unverträglichkeit, A Position der Staubblätter, P Pollengröße und Pm männliche Unverträglichkeit. Dominante Allele werden durch Großbuchstaben, rezessive Allele durch Kleinbuchstaben gekennzeichnet.
Unten: Schematische Darstellung der molekularen genetischen Struktur des S-Locus, in dem Gene als Kästchen dargestellt werden. Der dominante K-Phänotyp verfügt über den kompletten S-Locus mit fünf Genen (links), während der rezessive L-Phänotyp durch ein völliges Fehlen des S-Locus gekennzeichnet ist (Mitte). Seltene homostylische Formen können durch Mutationen in den Genen des S-Locus entstehen (rechts). Verlustmutationen des CYP-Gens wurden mit langen homostylen Blüten in Verbindung gebracht. (Nach Kappel 2017) Das Supergen
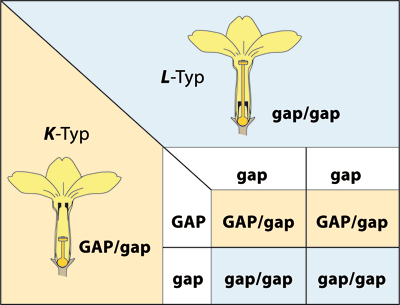
Abb. 3: Veranschaulichung der mutmaßlichen Vererbung des Supergens auf klassisch-genetische Weise. Kreuzungen zwischen dem heterozygoten K-Phänotyp (Allele GAP und gap) und dem homozygoten L-Phänotyp (Allele gap und gap) erzeugen immer K- und L-Phänotypen im Verhältnis 1:1. Dass es kein physisches gap-Allel gibt, wurde erst vor Kurzem entdeckt (siehe Abb. 2).
Das Erstaunliche bei der geschilderten Situation der Primeln ist, dass entweder die Merkmalskombination „langer Griffel, niedriger Staubblattansatz, kleine Pollenkörner, lange Narbenpapillen“ auftritt oder aber das entsprechende Gegenstück, aber normalerweise nie eine Situation irgendwie dazwischen. Dies legt nahe, dass die zugehörigen Erbanlagen in sehr diskreten Paketen vorliegen, nämlich an einem einzigen Genort. Dass die genetische Erbinformation quantisiert (gleichsam in Paketen) ist und ihre Vererbung nach mathematischen Regeln erfolgt, wurde 1866 erstmals von Gregor Mendel beschrieben (Mendel 1866). Mendel wurde jedoch ignoriert und seine Forschungsergebnisse gerieten in Vergessenheit, vor allem, weil seine Gesetze belegten, dass Variationen unveränderlich und vorhersehbar sind, eine Feststellung, die dem darwinistischen evolutionären Zeitgeist widersprach. Es sollte mehrere Jahrzehnte dauern, bis Mendels Erkenntnisse von mehreren Biologen wie Hugo de Vries, Carl Correns und William Bateson wiederentdeckt wurden. Bald nach der Wiederentdeckung der Mendel‘schen Gesetze zeigten die britischen Genetiker Bateson und Gregory, dass die Heterostylie, wie sie bei Primeln vorliegt, von einem einzigen Locus* kontrolliert wird (Bateson & Gregory 1905). Von diesem sog. S-Locus existieren ein dominantes Allel* (S) und ein rezessives Allel (s). Nun konnte die Vererbung der Phänotypen auf Mendel‘sche Weise verstanden werden.
In den meisten experimentellen Kreuzungen mit Primeln wird die Konstellation des jeweiligen Blütentyps so vererbt, als ob sie auf ein einziges Allelpaar (S und s) zurückzuführen wäre. Primeln des K-Phänotyps sind also S/s-Heterozygoten*, während solche des L-Phänotyps als s/s-Homozygoten* verstanden werden können. Dennoch findet man ab und zu auch sog. homostyle Blüten, in denen sich die Narbe und die Staubbeutel auf gleicher Ebene befinden (Abb. 2). Diese Blütentypen zeigen, dass die Besonderheiten der Blüte durch mindestens zwei getrennte, aber eng miteinander verknüpfte Gene festgelegt werden. In der klassischen Mendel‘schen Genetik wird deswegen die Griffellänge durch die Allele G und g bestimmt, die Länge der Staubblätter durch A und a. Die Verwendung der Großbuchstaben bedeutet, dass G und A dominant sind über g und a. Der K-Phänotyp hat also den Genotyp GA/ga, der L-Phänotyp ga/ga (Ford 1971).2
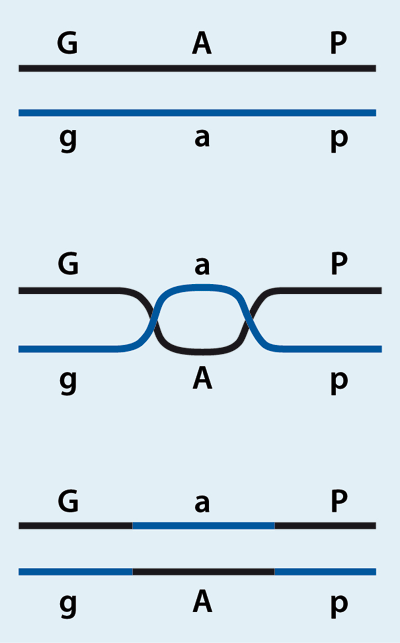
Abb. 4: Rekombination zweier Chromosomen. Veranschaulichung der mutmaßlichen doppelten Überkreuzung zweier Chromosomen, wobei der seltene homostyle Phänotyp entstehen sollte. Dass es kein physisches gap-Allel gibt, wurde erst vor Kurzem entdeckt. Anstatt einer solchen Überkreuzung werden homostyle Blüten durch Verlustmutationen verursacht (siehe Abb. 2).
Dann tauchten in Kreuzungsexperimenten einige sehr seltene und ungewöhnliche Blütentypen auf, von denen einige lange Staubblätter und kleine Pollenkörner, andere kurze Staubblätter und große Pollenkörner aufwiesen, also eine normalerweise nicht ausgebildete Kombination. Sie belegen, dass die Pollenkorngröße auch unabhängig vererbt werden kann und daher als unabhängiges genetisches Merkmal bewertet werden muss. Die neuen Blütentypen mussten durch neue Allele im S-Locus verursacht werden, was zu dem Schluss führte, dass der S-Locus in Wirklichkeit mindestens drei verschiedene, aber sehr eng miteinander verknüpfte Gene repräsentiert, die die verschiedenen Merkmale der Heterostylie bestimmen (Ernst 1936).
Bis in die 1990er-Jahre herrschte die Ansicht vor, dass der S-Locus mindestens drei verschiedene Gene enthält, die als dominante und rezessive Allele vorhanden waren. Das erste Gen (mit den Allelen G und g) bestimmte demnach die Länge der Griffel und der Narbenpapillen, das zweite Gen (mit den Allelen A und a) die Position der Staubblätter, während das dritte Gen (mit den Allelen P und p) die Pollenkorngröße und damit die männliche Kompatibilität festlegte. Der L-Phänotyp hat somit den Genotyp GAP/gap und der K-Phänotyp gap/gap. Kreuzungen zwischen GAP/gap- und gap/gap-Pflanzen produzieren immer K- und L-Phänotypen im Verhältnis 1:1 (Abb. 3), was den Beobachtungen in der Natur entspricht. Man vermutete, dass die extrem seltenen homostylen Blüten auf ein Rekombinationsereignis der Chromosomen zurückzuführen sind, bei dem die Gene ausgetauscht werden und auf diese Weise die atypische Kombination gebildet wird (Abb. 4). Die homostylen Pflanzen werden sich allerdings kaum durchsetzen können, da die Pollenkorngröße und die Narben mit den L- und K-Phänotypen nicht kompatibel sind.
Außerdem wurde vermutet, dass noch zwei weitere Gene existieren, die für die weibliche und männliche Inkompatibilität verantwortlich sind, da es unwahrscheinlich ist, dass ein einziges Gen sowohl morphologische als auch Inkompatibilitätsaspekte der Blüten kontrollieren würde (Kappel 2017). Der S-Locus ist also ein sog. Supergen*, d. h. ein chromosomales Segment mit mehreren ziemlich strikt verknüpften individuellen Genen, die zusammen einen integrierten Phänotyp mit mehreren Merkmalen steuern. Supergene werden immer als eine einzige Gruppe vererbt. Sie sind ein weit verbreitetes genetisches Design-Prinzip, das evolutionstheoretisch durch nur ein einziges genetisches Ereignis erklärt wird, in der Regel eine genomische Inversion (Abb. 5). Inversionen können sofort zu einem völlig neuen Phänotyp führen, ohne dass neue genetische Information hinzugefügt werden muss.
Supergene ermöglichen programmierte Anpassungen, die in nur einem oder wenigen Schritten freigegeben werden können. Sie erklären Mimikry in Schmetterlingen und Sexualdimorphismus bei Kampfläufern sowie Anpassungen bei Honigbienen und Zebrafischen (Pennisi 2017). Das Supergen in Primeln erklärt nicht nur die Heterostylie, sondern auch das Vorkommen der sehr seltenen Phänotypen, einschließlich der homostylen Blütentypen und der Polleninkompatibilität. Die Identität und die Funktion der im S-Locus vorhandenen Gene sowie eine Erklärung für die dominanten und rezessiven Allele blieben jedoch zunächst noch ungeklärt.
Mittlerweile konnte der molekulargenetische Ursprung der Heterostylie jedoch ermittelt werden. Er ist recht überraschend. Es stellte sich heraus, dass der dominante Phänotyp auf einem Supergen beruht, das fünf Gene enthält, während die rezessive Ausprägung auf die völlige Abwesenheit dieser Gene zurückzuführen ist. Das heißt: Dieses Merkmal wird auf hemizygote Weise vererbt. Die Einzelheiten dieses erstaunlichen Designs sind im Kasten beschrieben.
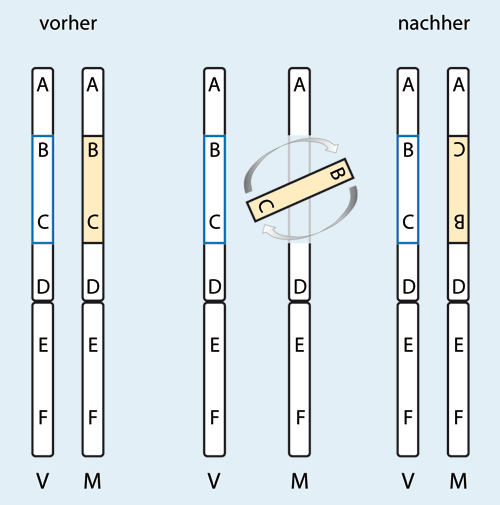
Abb. 5: Veranschaulichung einer chromosomalen Inversion. Normalerweise sind die von Vater (V) und Mutter (M) vererbten Chromosomen kolinear, d. h. die Gene sind auf beiden Chromosomen in genau der gleichen Reihenfolge vorhanden. Die Inversion des mütterlichen Chromosoms verändert die Ausrichtung der Gene abrupt. Nach der Inversion können die Chromosomen zwischen A und D (im gelben Bereich) keine Information mehr austauschen, da sie nicht mehr kolinear sind und deswegen nicht mehr rekombinieren können. Generatio spontanea (Selbst-Entwicklung) der Heterostylie?
Nach evolutionären Erkenntnissen muss Homostylie als sekundärer Zustand interpretiert werden; sie hat sich demnach als eine Ansammlung von selektierbaren Mutationen des DNA-Moleküls, darunter Genduplikationen (Verdopplungen) und Punktmutationen, entwickelt.
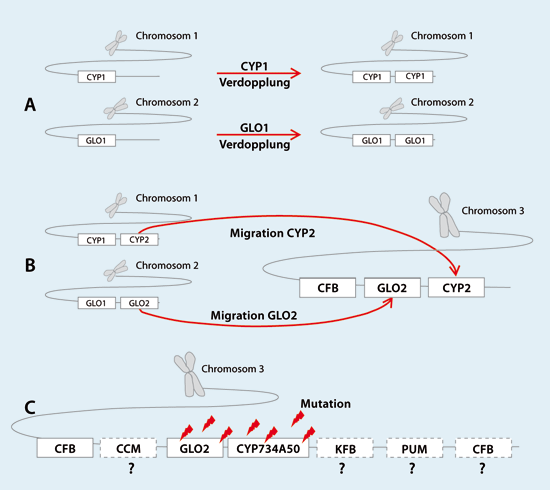
Abb. 6: Hypothetische evolutive Entstehung des S-Locus.
A Im Genom des Pflanzen befinden sich CYP1 und GLO1 auf unterschiedlichen Chromosomen.
B Durch zufällige Verdopplungen entstehen die Vorläufer von CYP734A50 (CYP2) und GLO2.
C Die duplizierten Gene wandern zum gleichen chromosomalen Ort neben das CFB-Gen. Um den S-Locus zu bilden, müssen sich noch weitere Gene mit völlig ungeklärtem Ursprung (PUM, KFB und CCM) an diesem Ort ansiedeln.
Während dieser mutmaßlichen Prozesse verwandelten sich die Gene CYP2 und GLO2 in die heutigen Gene CYP734A50 und GLO2 durch eine zufällige Anhäufung von Mutationen. Auch Evolutionsbiologen halten dieses Szenario für sehr unwahrscheinlich. (Nach Kappel 2017)
Wie stellen sich Evolutionsbiologen die Selbstentwicklung des Supergens vor? Als erster Schritt in der Evolution von Heterostylie wird der Erwerb einer dominanten Mutation vermutet, durch die der Griffel verkürzt wurde, gefolgt von einer zweiten Mutation zur Veränderung der Staubblattposition. Erst danach hätte sich die Selbstinkompatibilität entwickelt, wahrscheinlich als Anpassung der Pollenschläuche an das Wachstum in den verschiedenen Narbengeweben (Lloyd & Webb 1992). Es wurde auch der umgekehrte Weg vorgeschlagen, d. h. die Evolution der Selbstinkompatibilität war zuerst, gefolgt von Anpassungen der Griffel- und Staubblattlänge (Charlesworth & Charlesworth 1979). Letzteres wird von den meisten Evolutionsbiologen allerdings infrage gestellt und man bevorzugt das erste Szenario. Keines dieser Modelle gibt jedoch Auskunft über molekulare oder genetische Details.
Wir wissen heute, dass die Verkürzung des Griffels ein neues gewebespezifisches Cytochrom-C-Gen erfordert: CYP734A50 (siehe Kasten). Dieses Gen darf nur im Griffel von K-Blüten exprimiert werden, damit die Zellwachstumshormone inaktiviert werden und ein kurzer Griffel entsteht. Ebenso benötigt es das gewebespezifische GLO2-Gen. Insgesamt benötigt der S-Locus fünf neue Gene, einschließlich aller regulatorischen Schalter-Sequenzen für eine abgestimmte und kontrollierte Expression dieser Gene. Diese Erkenntnisse erfordern sehr anspruchsvolle Bedingungen für ein tragfähiges Modell für die chromosomale Evolution des Supergens im S-Locus. Es ist klar, dass diese Gene nicht nach dem Zufallsprinzip aus einer nicht-codierenden Region stammen können.
Eine Gruppe von Botanikern der Universität Potsdam argumentiert, dass das CYP734A50-Gen durch eine Duplikation* entstand, gefolgt vom Erwerb von griffelspezifischen Expressionselementen (genetische und epigenetische Schalter). Dieses komplexe genetische Ereignis soll in der Stammpopulation der Familie der Primelgewächse (Primulaceae) stattgefunden haben und wird als die oben erwähnte dominante griffelreduzierende Mutation interpretiert. Die Tatsache, dass ein ähnliches CYP-Gen außerhalb des S-Locus gefunden wird, soll die Hypothese von der mutmaßlichen Duplikation stützen (Huu 2016). Ebenso geht man davon aus, dass das GLO2-Gen durch Duplikation aus GLO1 entstand (Kappel 2017). Zudem zeigen phylogenetische Rekonstruktionen*, dass der anzunehmende gemeinsame Vorfahr der gesamten Gattung Primula bereits das Supergen besaß (Mast 2006).
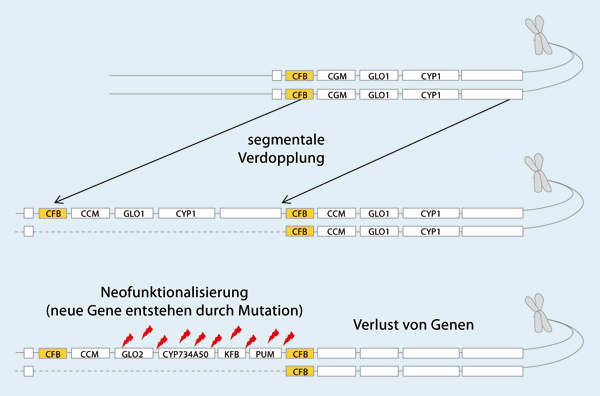
Abb. 7: Alternative hypothetische evolutive Entstehung des S-Locus.
Oben: Im Genom der Pflanzen befinden sich die Gene CCM, CYP1 und GLO1 bereits kolinear auf einem Chromosom.
Mitte: Durch eine zufällige segmentale Verdopplung soll der Vorläufer des S-Locus mit den Genen CCM, CYP2 und GLO2 entstanden sein.
Unten: Durch eine Anhäufung von Mutationen verwandeln sich die duplizierten CYP2- und GLO2- Gene in die heutigen Gene CYP734A50 und GLO2. Zusätzliche duplizierte Sequenzen (offene Kästchen) erwerben neue Funktionen und werden zu PUM und KFB mutiert.
Es ist fraglich, ob dieser evolutionäre Vorgang plausibler ist als der in Abb. 6 beschriebene. (Nach Kappel 2017)
Ein Szenario der schrittweisen Gen-für-Gen-Duplikation, bei dem die Duplikate zufällig nebeneinander gelangen, wird allerdings als äußerst unwahrscheinlich betrachtet (Abb. 6), auch von den Potsdamer Forschern. Daher schlagen sie die Duplikation eines großen DNA-Segments um das GLO1-Gen vor, aus denen sich beide Gene, CYP734A50 und GLO2, entwickeln konnten. Das verdoppelte Segment wurde so zum Vorläufer des S-Locus (Abb. 7). Man würde nun erwarten, dass man im Bereich des ursprünglichen GLO1-Gens ähnliche Gene findet wie im heutigen S-Locus. Diese Erwartung ist nicht weit hergeholt, denn nach dem vorgeschlagenen Szenario lieferte die DNA um das GLO1-Gen auch die Sequenzen für die anderen Gene des S-Locus. Die Tatsache, dass solche Sequenzen jedoch nicht im GLO1-Genbereich angetroffen werden (Nowak 2015), steht im Widerspruch zu diesem Vorschlag.
Ohne Zielvorgabe ist eine schrittweise Entstehung unplausibel, aber Evolution kennt keine Ziele.
Um eine evolutive Entstehung des S-Locus zu modellieren, muss man von zusätzlichen Genverlusten, Neofunktionalisierung* und Mutationen ausgehen (Kappel 2017). Das bedeutet, dass man Ereignisse annehmen muss, die keine Spuren im Genom* hinterlassen haben. Dies würde eine schrittweise Evolution des Supergens jedoch nicht plausibler machen. Man kann sich zwar immer ein Schritt-für-Schritt-Szenario ausdenken, um alle erforderlichen genetischen Elemente, die im S-Locus vorhanden sind, anzuhäufen, doch funktioniert dies nur, wenn ein Ziel vorgegeben ist, an dem jeder Schritt selektiv bewertet werden kann. Evolutionstheoretisch wird eine Zielvorgabe jedoch ausdrücklich ausgeschlossen. Die Tatsache, dass der dominante S-Locus von CFB-Genen flankiert wird (Abb. 2), könnte man als Beleg für ein einziges Rekombinationsereignis bewerten, bei dem der gesamte S-Locus auf einmal im Genom integriert wurde. Manche Rekombinationen hinterlassen genau dieses flankierende Markenzeichen.
Angesichts der aktuellen Erkenntnisse über den S-Locus sind die vorgeschlagenen evolutionären Szenarien höchst unwahrscheinlich, wenn nicht gar unmöglich. Was einen zufälligen Entwicklungsprozess noch schwieriger macht, ist die Tatsache, dass sich evolutionstheoretisch gesehen das Supergen immer wieder neu entwickelt haben müsste. Darauf kommen wir im nächsten Abschnitt zu sprechen.
Molekulargenetische Grundlage der Heterostylie
Im 20. Jahrhundert ermöglichten molekulargenetische Untersuchungen an Primeln die Erstellung einer Genkarte des S-Locus. Zudem führte die genetische Forschung an Primula veris zu einer Referenzgenomsequenz* aus einem Pool von L- und K-Phänotypen. Außerdem identifizierten Transkriptomanalysen* die Gene, die in beiden Blütentypen am stärksten exprimiert* werden (Nowak et al. 2015; Huu et al. 2016). Diese Studien bildeten die Grundlage für zwei wichtige Durchbrüche in unserem Verständnis von Heterostylie in Primeln: zum einen die Identifizierung und zum anderen die funktionelle Beschreibung des kompletten S-Locus in den L- und K-Phänotypen (Li et al. 2016; Burrows & McCubbin 2017). Sie zeigen auf, dass sich der S-Locus direkt neben dem Centromer* des größten Chromosoms befindet. Das erklärt, warum im S-Locus kaum Rekombinationen auftreten. Wenn Genetiker von Rekombination sprechen, dann meinen sie den Austausch von Allelen, die auf verschiedenen Chromosomenarmen vorhanden sind (Abb. 4). Der Austausch wird als mechanischer Prozess verstanden, dessen Häufigkeit von der Länge des chromosomalen Armes abhängt. Befindet sich ein Gen jedoch in der Nähe des Centromers, kommt es kaum zu Rekombinationen, und der genetische Austausch ist selten. Dadurch verhält sich die Vererbung des gesamten Merkmalskomplexes wie ein einziger Mendel’scher Locus (also so, als ob es nur ein Merkmal wäre) und diese Situation hat zur Folge, dass die L-und K-Phänotypen in etwa gleichen Mengen bestehen bleiben.
Erst in jüngster Zeit wurden die Gene identifiziert, die die Heterostylie in Primeln koordinieren. Im Jahr 2016 wurde beschrieben, wie bei Blüten des K-Phänotyps mehrere einzigartige Gene exprimiert werden, die im L-Phänotyp nicht vorhanden waren (Huu 2016). Wie erwartet wurden die Gene für Griffellänge, Staubblattlänge und Pollengröße im dominanten S-Locus vorgefunden, außerdem Sequenzen für weibliche und männliche Inkompatibilität. Von den fünf identifizierten Genen waren zwei zuvor schon bekannt gewesen: CYP734A50 und GLO2. Das CYP734A50-Gen codiert für ein Cytochrom-P450-Enzym, das eine Klasse von Zellwachstumshormonen (die sog. Brassinosteroide) inaktiviert, wodurch verständlich wird, dass ein mutiertes CYP734A50-Gen mit langen homostylen Blüten verbunden ist. Im Gegensatz dazu war ein inaktives GLO2-Gen mit kurzen Staubblättern assoziiert worden. Das GLO2-Gen gehört zu einer Familie von morphogenetischen Genen, die genetische Programme in Bezug auf Form und Größe steuern.
Das CYP734A50-Gen bestimmt also die Griffellänge und möglicherweise die weibliche Inkompatibilität, während das GLO2-Gen für die Länge der Staubblätter verantwortlich ist (Kappel 2017). Diese zwei Gene bilden damit die Grundlage für die G/g- und A/a-Allele der klassischen Genetik. Die restlichen drei Gene codieren für ein Kelch-repeat F Box Protein (KFB), ein Pumilio-like RNA-Binding Protein (PUM) und für ein Protein mit einer stark konservierten C-terminalen Domäne (CCM). Es ist noch nicht völlig geklärt, wie diese Gene mit dem Phänotyp zusammenhängen, obwohl KFB und PUM für die Pollengröße und männliche Inkompatibilität verantwortlich zu sein scheinen (Kappel 2017). Darüber hinaus wurde auf beiden Seiten des dominanten S-Locus das Gen CBF gefunden (Abb. 2). Die faszinierendste Beobachtung war aber, dass der rezessive S-Locus um etwa 280.000 DNA-Buchstaben kürzer war als der dominante S-Locus. Im Gegensatz zum dominanten S-Locus enthielt der rezessive S-Locus nur ein einziges CFB-Gen, von den anderen Genen gab es keine Spur (Kappel 2017). Der S-Locus in Primeln ist somit ein hemizygoter* Locus, d. h. eine einzigartige DNA-Region, die nur einmal (mono-allelisch) pro Genom* vorkommt. Diese Erkenntnis liefert eine elegante Erklärung für die unterdrückte Rekombination, da es auf dem s-Locus kein entsprechendes Gegenstück zum Austausch von Genen gibt. Mendels rezessive Eigenschaften werden hier also nicht durch Gene verursacht, sondern durch das Fehlen von Genen!
Konvergenz

Abb. 8: Konvergenz der gleichen genetischen Prozesse oder geplantes Design? Heterostylie bei Wald-Schlüsselblume (Primula elatior, oben) und beim Lungenkraut (Pulmonaria officinalis, unten). Deutlich erkennbar sind die Narben des langen Griffels in den L-Phänotypen (A und C) und die Pollenfächer der langen Staubblätter im K-Phänotyp (B und D). (Fotos: R. Wiskin)
Das Supergen im S-Locus und seine Wirkungsweise wurden überwiegend in der Genforschung bei Primeln entschlüsselt. Dieses interessante Phänomen kommt jedoch nicht nur bei Primeln, sondern u. a. auch beim nicht näher verwandten Lungenkraut (Pulmonaria officinalis) vor (Abb. 8). Vergleicht man die Blüten vieler weiterer Arten miteinander, so fällt immer wieder Heterostylie auf, auch bei Arten, die weit entfernt voneinander im System der Blütenpflanzen stehen. Nach gängiger evolutionstheoretischer Vorstellung ist die Heterostylie mindestens 20 Mal unabhängig in 28 Pflanzenfamilien entstanden (Ganders 1979; Kappel 2017). Selbst innerhalb von Familien, wie beispielsweise den Raublattgewächsen (Boraginaceae), zu denen das Lungenkraut (Abb. 8) gehört, werden mehrere unabhängige Ursprünge angenommen (Cohen 2011). Die Frage ist nun: Wird die Heterostylie in diesen Pflanzen auch von einem Supergen gesteuert?
In insgesamt sechs bisher untersuchten Gattungen scheint die Heterostylie tatsächlich von einem einzigen Locus kontrolliert zu werden, der dem Supergen von Primeln sehr ähnlich ist (Lewis & Jones 1992). So konnte beispielsweise in Safranmalven (Turnera spp.) Homostylie auf ein neuartiges Allel im S-Locus zurückgeführt werden, das sowohl lange Griffel als auch lange Staubblätter verursacht (Shore & Barrett 1985). Auch im Buchweizen (Fagopyrum) waren die Homostylie-Mutanten auf ein hemizygotes* Supergen zurückzuführen (Matsui et al. 2003). Dies bedeutet, dass die Supergene für Heterostylie – evolutionstheoretisch gesehen – immer wieder unabhängig entstanden sein müssen. Evolutionsbiologen bezeichnen eine solche unabhängige Entstehung ähnlicher struktureller oder genetischer Konstellationen als Konvergenz und gehen davon aus, dass natürliche Selektion immer wieder zu den gleichen oder sehr ähnlichen Supergenen führen kann. Konvergenz ist in diesem Fall umso erstaunlicher, als ohnehin unklar ist, welcher Selektionsdruck die ausgefeilte Supergen-Konstruktion überhaupt ein einziges Mal begünstigt haben sollte. Die von dem Supergen vermittelte Fremdbestäubung und Förderung der sexuellen Fortpflanzung würden eher zu einem Evolutionsstillstand führen als der Weiterentwicklung von Arten zu verhelfen.3
Polyvalenz und Schöpfung
Der S-Locus in Primeln ist eindeutig eine polyvalente* DNA-Region mit mindestens fünf Genen und unterstützt somit das Polyvalenz-Konzept der Schöpfungslehre und das Grundtypkonzept. Dieses Konzept beinhaltet einerseits die Annahme von separat erschaffenen Grundtypen, andererseits die Annahme, dass die Grundtypen von Anfang an mit einem breiten Variationsspektrum ausgestattet waren (Junker & Scherer 2013, Kapitel VII.16). Grundtypen waren genetisch vielseitig und verfügten über Mechanismen zur schnellen Anpassung und Bildung neuer Arten. Einer dieser Mechanismen ist die Polyvalenz, was bedeutet, dass Grundtypen nicht eine einzige, fixe genetische Ausstattung hatten, sondern dass das Erbgut vermutlich ausgeprägt mischerbig und mit genetischen Programmen zur Variabilitätserzeugung ausgestattet war (vgl. Crompton 2019; Borger 2018).
Bis vor Kurzem wurde stillschweigend davon ausgegangen, dass Individuen einer Art etwa die gleiche Anzahl von Genen haben sollten. Dies liegt daran, dass nach der Darwin‘schen Theorie natürliche Selektion der Antrieb für Entstehung, Veränderung und Erhaltung des Erbguts ist. Diese Vorstellung hat sich jedoch als falsch erwiesen. Die jüngere Molekulargenetik belegt, dass die Genome von Organismen, die zur selben Art gerechnet werden, so variabel sind, dass Genetiker heute davon ausgehen, dass es so etwas wie ein Spezies-Genom nicht gibt. So sind beispielsweise in den wilden Formen der Acker-Schmalwand (Arabidopsis thaliana) etwa vier Prozent der Gene völlig anders als im Referenzgenom oder in diesem gar nicht vorhanden (Clark 2007). Etwas sehr Ähnliches ist bei den K- und L-Phänotypen der Primeln zu beobachten. Vergleicht man die Genome der beiden Phänotypen, stellt man fest, dass mindestens fünf Gene in den L-Pflanzen fehlen: GLO2, CYP734A50, KFB, PUM und CCM. Die Aufteilung dieser hemizygoten Gene auf verschiedene Chromosomen ist ein klarer Beleg für Polyvalenz, also für programmierte Variationsmöglichkeiten, besonders auch da es keine plausible evolutionäre Erklärung für die Existenz und das mehrfach unabhängige Vorkommen dieser Gene (Konvergenz, s. o.) gibt.
Genetische Entropie
Unter genetischer Entropie versteht man die langsame, aber anhaltende Ansammlung von schwach schädlichen Mutationen, die nicht durch Selektion ausgemerzt werden, was letztendlich zu einem genomischen Zusammenbruch führen wird (Sanford 2005). Die Tatsache, dass nur der S-Locus die fünf für die Heterostylie erforderlichen Gene enthält (Hemizygotie), macht das Merkmal sehr anfällig für Verlustmutationen. Dies ist leicht zu verstehen, wenn man sich Folgendes klar macht: Sexuell sich vermehrende Organismen haben normalerweise zwei Kopien von jedem Gen (abgesehen von Geschlechtschromosomen). Eine Kopie wurde vom Vater geerbt, die andere von der Mutter. Wenn eine der Kopien durch Mutation beschädigt wird, ist die andere weiterhin funktionsfähig. Dieses Backup-System verhindert einen unmittelbaren genetischen Zusammenbruch durch Mutationen. Für den hemizygoten S-Locus (nur einmal vorhanden) gibt es dagegen kein Backup, sodass sich genetische Verluste sofort phänotypisch auswirken.
Vor diesem Hintergrund ist zu erwarten, dass viele Pflanzenarten die Heterostylie als Familienmerkmal verloren haben. Eine aktuelle Studie zeigt nun, dass dies tatsächlich der Fall ist. In praktisch allen heterostylen Familien ist Homostylie mehrfach durch Verlustmutationen entstanden, überwiegend durch Inaktivierung der Gene CYP734A50 und GLO2 (Zhong et al. 2019). So ist das ausgefeilte Design des Supergens dazu verurteilt, durch Mutationen zu verschwinden, und die natürliche Auslese scheint nicht in der Lage zu sein, diesen degenerativen Prozess zu unterbinden. Damit bleiben zwei offene Fragen. Erstens, kann derselbe degenerative Prozess, den wir heute beobachten, in Zukunft ein Supergen erzeugen? Zweitens, wie war die natürliche Selektion an der Entstehung des Supergens überhaupt beteiligt? Die Erkenntnisse der aktuellen Biologie zeigen, dass evolutionäre Erklärungen unzureichend sind, und rechtfertigen Modellierungen und Deutungen im Rahmen einer Schöpfungslehre.
Mendel und die genetische Entropie
Mendel führte schätzungsweise 28.000 Kreuzungsexperimente mit Erbsen durch und untersuchte dabei sieben klar abgegrenzte Merkmale (vgl. Crompton 2019). Durch die Erforschung der Vererbung der Farbe der Samenschale fand er heraus, dass die gelbe Farbe über die grüne dominierte. Im Jahr 2007 wurde festgestellt, dass das sog. Stay Green (STG)-Gen die Samenfarbe bestimmt. Dieser Name ist etwas irreführend, weil das STG-Gen ein Enzym produziert, das das grüne Pigment während der Reifung entfernt, damit sich die gelben Samen bilden. Wenn das STG-Gen durch Mutationen ausfällt, wird das grüne Pigment nicht mehr entfernt und die Erbse bleibt grün. Jetzt verstehen wir, warum Gelb dominant ist und Grün rezessiv: Gelbe Samen werden durch ein funktionales Gen verursacht, dessen Genprodukt das grüne Pigment aktiv entfernt. Die Samen bleiben also grün, wenn das Gen kein funktionierendes Protein produziert. Das Ergebnis ist, dass man entweder gelbe oder grüne Samen beobachtet, nicht irgendeine Mischfarbe.
Wenn Gene verloren gehen müssen, damit rezessive Merkmale ausgeprägt werden können, wie sind dann diese Gene ursprünglich entstanden?
Mendel zeigte, dass die Genetik quantisiert ist, d. h. in „Pakete“ gegliedert, und wir wissen heute, dass die individuellen Informationspakete durch Gene definiert sind. Dominante und rezessive Merkmale werden dann einfach als das Vorhandensein und Fehlen von funktionalen Genen verstanden. Wird ein defektes Gen von nur einem Elternteil vererbt, kann es durch das Gen des anderen Elternteils kompensiert werden. Das läuft darauf hinaus, dass eine Merkmalsausprägung, die mit einem bestimmten Gen verbunden ist, dominant ist. Ein rezessives Merkmal wird erst dann ans Licht gebracht, wenn ein Individuum von beiden Elternteilen defekte Kopien erhält.
Diese neuen Erkenntnisse haben schwerwiegende Auswirkungen auf unser Verständnis von Biologie. Wenn Gene verloren gehen müssen, damit rezessive Merkmale ausgeprägt werden können, wie sind dann diese Gene ursprünglich entstanden? Offensichtlich gibt es im Genom viel mehr Gene, als sich durch die bekannten Evolutionsmechanismen erklären lassen. Die Gesetze von Mendel zeigen sich bei Genen, die für das Überleben des Organismus nicht unbedingt notwendig sind. Sie dürfen sogar defekt oder auch gar nicht vorhanden sein, ohne dass dies zu schweren Schäden führt. Verlustmutationen sind der Grund, warum Mendel kurze und lange Pflanzen, weiße und rosa Blüten, gelbe und grüne Samen fand. Verlust von Genen bzw. Allelen (Homozygotisierung) ist ein eleganter Mechanismus, um Variationen, Anpassungen und neue Arten zu erzeugen. Da es sich aber um einen Zerfallsmechanismus handelt, sprechen die Zerfallstendenzen des Erbguts (genetische Entropie) dagegen, dass auf diesem Wege neue genetische Information hervorgebracht werden kann.
1 Original: „The pollen of A is fitted for stigma of B, and conversely.“ (In einem Brief an den Botaniker Asa Gray im Jahr 1861)
2 Dies könnte darauf hindeuten, dass die Blüten ursprünglich mit kurzen Griffeln und langen Staubblättern gestaltet waren.
3 Das hängt damit zusammen, dass Mutanten im heterozygoten Zustand meist rezessiv sind, sich daher nicht auswirken und nicht selektiv festgehalten werden können. Auf diese Problematik soll hier aber nicht weiter eingegangen werden.
Barrett SC (2002)
The evolution of plant sexual diversity. Nat. Rev. Genet. 3, 274–284.
Barrett SCH & Shore JS (2008)
New insights on heterostyly: Comparative biology, ecology and genetics. In: Franklin-Tong VE (ed) Self-incompatibility in flowering plants: evolution, diversity and mechanisms, Berlin: Springer, pp 3–32.
Bateson W & Gregory RP (1905)
On the inheritance of heterostylism in Primula. Proc. R. Soc. Lond. B 76, 581–586.
Borger P (2018) Darwin Revisited.
Or how to understand biology in the 21st century. Scholars’ Press.
Burrows BA & McCubbin AG (2017)
Sequencing the genomic regions flanking S-linked PvGLO sequences confirms the presence of two GLO loci, one of which lies adjacent to the style-length determinant gene CYP734A50. Plant Reproduction 30, 53–67.
Clark RM, Schweikert G et al. (2007)
Common sequence polymorphisms shaping genetic diversity in Arabidopsis thaliana. Science 317, 338–342.
Cohen JI (2011)
A phylogenetic analysis of morphological and molecular characters of Lithospermum L. (Boraginaceae) and related taxa: evolutionary relationships and character evolution. Cladistics 27, 559–580.
Crompton N (2019)
Mendel‘sche Artbildung und die Entstehung der Arten. http://www.wort-und-wissen.de/artikel/sp/b-19-3_mendel.pdf
Charlesworth D & Charlesworth B (1979)
A model for the evolution of distyly. Amer. Nat. 114, 467–498.
Ernst A (1936)
Heterostylie-Forschung: Versuche zur genetischen Analyse eines Organisations- und „Anpassungs“merkmales. Z. Ind. Abst. Vererb.lehre 71, 156–230.
Ford EB (1971)
Ecological Genetics. Chapman & Hall, London.
Ganders FR (1979)
The biology of heterostyly. New Zealand J. Bot. 17, 607–635;
Gilmartin PM (2015)
On the origins of observations of heterostyly in Primula. New Phytol. 208, 39–51.
Huu CN, Kappel C, Keller B, et al. 2016.
Presence versus absence of CYP734A50 underlies the style-length dimorphism in primroses. eLife 5, e17956.
Junker R & Scherer S (Hg., 2013)
Evolution. Ein kritisches Lehrbuch. Gießen.
Junker R & Wiskin R (2017)
Der Natur auf der Spur im Frühlingswald. CV Dillenburg, 4. Auflage.
Kappel C, Huu CN & Lenhard M (2017)
A short story gets longer: recent insights into the molecular basis of heterostyly. J. Exp. Bot. 68, 5719–5730.
Lewis D & Jones DA (1992)
The genetics of heterostyly. In: Barrett SCH (ed) Evolution and function of heterostyly, Berlin Heidelberg: Springer, pp 129–150.
Li J, Cocker JM, Wright J et al. 2016.
Genetic architecture and evolution of the S locus supergene in Primula vulgaris. Nature Plants 2, 16188.
Lloyd DG & Webb CJ (1992)
The evolution of heterostyly. In: Barrett SCH (ed) Evolution and function of heterostyly, Berlin Heidelberg: Springer, pp 151–178.
Mast AR, Kelso S & Conti E (2006)
Are any primroses (Primula) primitively monomorphic? New Phytologist 171, 605–616.
Matsui K, Tetsuka T, Nishio T & Hara T (2003)
Heteromorphic incompatibility retained in self-compatible plants produced by a cross between common and wild buckwheat. New Phytologist 159, 701–708.
Mendel G (1866)
Versuche über Pflanzen-Hybriden. Verh. Naturforsch. Ver. Brünn 4, 3–47. http://www.deutschestextarchiv.de/book/view/mendel_pflanzenhybriden_1866?p=14.
Nowak MD, Russo G, Schlapbach R, Huu CN, Lenhard M & Conti E (2015)
The draft genome of Primula veris yields insights into the molecular basis of heterostyly. Genome Biology 16, 12.
Pennisi E (2017)
‘Supergenes’ drive evolution. Science 357, 1083.
Sanford S (2005)
Genetic Entropy & The Mystery of the Genome. Elim Publishing, Lima NY.
Zhong L, Barrett SCH et al.(2019)
Phylogenomic analysis reveals multiple evolutionary origins of selfing from outcrossing in a lineage of heterostylous plants. New Phytol. 224, 1290–1303.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 6/21/21
Webmaster