
Themen • Kurzbeiträge • Streiflichter
DNA als Retter der RNA-Welt-Hypothese?
von Boris Schmidtgall
Studium Integrale Journal
26. Jahrgang / Heft 2 - Oktober 2019
Seite 113 - 115
Zusammenfassung: Ungeachtet ihrer Beliebtheit weist die RNA-Welt-Hypothese als Erklärung eines natürlichen Ursprungs der ersten Organismen große Defizite auf. Im Sinne einer Ergänzung dieser Hypothese veröffentlichte die Forschungsgruppe um Oliver Trapp eine Arbeit zur präbiotischen Synthese von Desoxy-Nukleosiden (DNA-Bausteine). Die Autoren vertreten die Auffassung, dass ihr Modell ein geochemisch plausibles Szenario für die Entstehung von DNA-Bausteinen darstellt. Eine genauere Analyse zeigt jedoch, dass sich ein gänzlich anderes Bild ergibt.
• • • • •
Einführung
Unter Naturwissenschaftlern gilt es als ausgemacht, dass Leben „von alleine“, d. h. unter rein natürlichen Umständen ohne schöpferischen Input, entstanden ist, obwohl es dafür bis heute keine tragfähigen Belege gibt. Nach Ansicht der meisten Lebensursprungs-Forscher stellten sich selbst vervielfältigende molekulare Systeme auf der Basis von RNA-Molekülen das Vorstadium zu den ersten Organismen dar. Die RNA gilt als der beste Kandidat für einen möglichst einfachen Ursprung des Lebens, weil sie als einziges Biomolekül zugleich zwei wichtige Eigenschaften in sich vereint: sowohl die Fähigkeit zur Informationsspeicherung und -übertragung als auch zur Katalyse (Beschleunigung) bestimmter chemischer Reaktionen. Damit wären zumindest hypothetisch chemische Verbindungen in einer „RNA-Welt“ vorhanden, die sowohl Stoffwechsel als auch Vererbung ermöglichen (Gilbert 1986).

Suche nach neuen Erklärungen
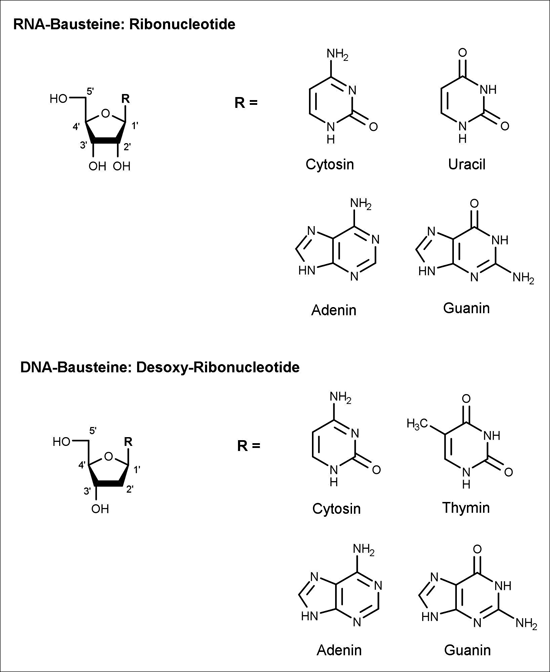
Abb. 1: Strukturformeln der Bausteine der RNA (Ribonukleotide) und der DNA (Desoxy-Ribonukleotide). Die zwei strukturellen Unterschiede zwischen den Bausteinen sind die fehlende OH-Gruppe an der 2‘-Position bei den DNA-Bausteinen und das Thymin anstelle des Uracil als eine der kanonischen Nukleobasen. Damit also Desoxy-Ribonukleotide hergestellt werden können, muss die 2‘-OH Gruppe der Ribonukleotide entfernt werden. In Organismen ist dafür das Enzym Ribonukleotid-Reduktase zuständig.
Allerdings sind gravierende Schwächen des RNA-Welt-Modells in der Fachwelt allgemein bekannt. Weder für die Möglichkeit der Entstehung der notwendigen Bausteine der RNA, der Ribonukleotide, noch für ihre anschließende Polymerisation (Verknüpfung) zu RNA-Strängen sind plausible präbiotische Bedingungen aufgezeigt worden. „Präbiotisch“ bedeutet dabei „vor der Anwesenheit von Leben“. Noch weit größer ist die Herausforderung, die anschließend erforderliche Replikation (Vermehrung) der RNA in einem wässrigen, annähernd natürlichen Milieu zu realisieren. Das Kernproblem dabei ist die ausgeprägte Labilität sowohl der RNA-Bausteine als auch des Makromoleküls RNA selbst in wässriger Lösung. Behauptungen, dass diese Probleme schon gelöst seien, sind nicht überzeugend, denn die Publikationen, auf die dabei oft verwiesen wird (Powner 2009, Ferris 2006, Deck 2011), beschreiben Kunstgriffe, die auf chemischer Erfahrung beruhen und die keinerlei Bezug zu realistischen präbiotischen Bedingungen auf einer frühen Erde haben. Diese offenkundigen Schwächen des RNA-Welt-Modells veranlassen Forscher immer wieder dazu, bestehende Modelle abzuwandeln oder neue Ideen für einen hypothetischen Anfang des Lebens zu entwickeln. Kritische Kommentare dazu wurden in diesem Journal bereits publiziert (Binder 2009, Schmidtgall 2014).
Die Schwächen des RNA-Welt-Modells veranlassen Forscher immer wieder dazu, neue Ideen für einen hypothetischen Anfang des Lebens zu entwickeln.
Eine Möglichkeit, die bereits früher erwogen worden ist, besteht in der stabilisierenden Wirkung des chemisch verwandten Biopolymers der RNA, der DNA (Lindahl 1993). Allerdings galt ihre Entstehung bisher als problematisch, weil nach den gängigen Vorstellungen DNA aus RNA gebildet worden sein soll und dazu das komplexe Enzym Ribonukleotid-Reduktase erforderlich ist. Dieses entfernt die Hydroxy-Gruppe an der 2‘-Position der Ribose und wandelt sie in 2-Desoxyribose um (Abb. 1). Das wäre aber kein einfacher Anfang des Lebens. Abgesehen davon ist bisher kein Experiment beschrieben worden, das eine gute Erklärung für den Ursprung von DNA-Bausteinen (ebenso wie für diejenige von RNA-Bausteinen) darstellen würde.
Daher wurde kürzlich von der Münchner Forschungsgruppe um Oliver Trapp (Teichert et al. 2019) in der chemischen Fachzeitschrift Angewandte Chemie ein Artikel veröffentlicht, in welchem eine Reihe von chemischen Reaktionen beschrieben ist, die von den Autoren als ein mögliches Szenario der Entstehung von DNA-Bausteinen beschrieben wird.
Ohne exakte Reaktionsführung keine DNA-Bausteine
Den Autoren der Arbeit gelang es, alle vier kanonischen Nukleoside ausgehend von drei verschiedenen Molekülen (Aldehyd, Nukleobase und D-Glyceraldehyd, Abb. 2) herzustellen. Gegenüber früheren Arbeiten auf diesem Gebiet können die Forscher um Trapp durchaus einige Fortschritte vorweisen. Die Reaktionen wurden allesamt in wässrigem Milieu und ohne die Isolierung und Aufreinigung von Zwischenprodukten durchgeführt. Die Reaktionen liefen unter relativ milden Bedingungen (40-70 °C) ab und es waren keine Veränderungen der Temperatur oder anderer Parameter (pH, Konzentration) nötig. Das klingt in der Tat nach einem beachtlichen Erfolg auf der Suche nach einem plausiblen Szenario für den Ursprung erster Biomoleküle. Allerdings fällt bei näherer Betrachtung der experimentellen Details auf, dass die Versuche geradezu meisterhaft geplant wurden, um DNA-Nukleotide zu erhalten.
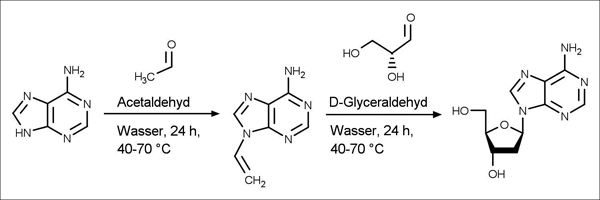
Abb. 2: In der Arbeit von Trapp et al. untersuchter Reaktionsweg ausgehend von Nukleobasen, Acetaldehyd und D-Glyceraldehyd. Hier ist der Reaktionsweg exemplarisch am Adenin gezeigt. Die Reaktion ergibt aber ebenso auch Desoxy-Nukleotide bei Verwendung der anderen drei Nukleobasen. Die Ausbeuten der Reaktionen waren mit unter einem Prozent (Adenosin, Guanosin, Thymidin) bzw. 2,5 % für Cytidin recht niedrig.
Es bedarf keiner vertieften Erörterung, dass die Verwendung hochreiner chemischer Verbindungen (Nukleobasen, Acetaldehyd und D-Glyceraldehyd) in demineralisiertem Wasser – wie in den Versuchen von Teichert et al. geschehen – keineswegs eine Nähe zu natürlichen Bedingungen darstellt. Zudem wurden die Versuche stets in geschlossenen Ampullen durchgeführt, da anderenfalls der flüchtige Acetaldehyd (Siedepunkt 20 °C) aus der Reaktionsmischung schnell entweichen würde. In dem Originalartikel wird der Einsatz geschlossener Ampullen damit begründet, dass auf der frühen Erde ein deutlich höherer Atmosphärendruck geherrscht haben soll – eine kaum überprüfbare Vermutung.
Außerdem wurde mit D-Glyceraldehyd gezielt ein Molekül gewählt, das von seiner geometrischen Beschaffenheit (Konfiguration) her für das anvisierte Resultat genau passend ist. Das Spiegelbild-Molekül L-Glyceraldehyd findet in der Publikation von Teichert et al. dagegen keine Erwähnung, obwohl dessen Entstehung unter natürlichen Bedingungen genauso wahrscheinlich ist wie diejenige des D-Glyceraldehyds. Die Verwendung von L-Glyceraldehyd anstelle des D-Glyceraldehyds ist problematisch, weil seine entsprechende Reaktion Nukleoside hervorbringt, die für die Bildung von Erbmolekülen aufgrund ihrer Geometrie ungeeignet sind. Selbst wenn der L-Glyceraldehyd nur einen Teil des Gemischs ausmacht, würde das die Synthese von funktionsfähigen DNA-Molekülen wirksam verhindern. Für einen erfolgreichen Reaktionsverlauf ist es also nötig, dass der D-Glyceraldehyd in reiner Form vorliegt. Hier wird also das Problem der Entstehung enantiomerenreiner (nur D-Form oder nur L-Form liegt vor) chemischer Verbindungen ohne gezielte Steuerung durch einen Experimentator schlicht übergangen. Dabei ist jedem Chemiker bekannt, dass die Herstellung enantiomerenreiner chemischer Verbindungen selbst mit fortschrittlichen Methoden der Synthesechemie oft eine Herausforderung ist. Die angebliche Spezifität der von Teichert et al. aufgezeigten Synthese wird auch durch mögliche Reaktionen mit anderen Carbonylverbindungen eingeschränkt. In präbiotischen Szenarien ist zu erwarten, dass neben D-Glyceraldehyd auch andere Aldehyde vorhanden sind und damit den resultierenden Cocktail in seiner Zusammensetzung komplex werden lassen. Im Hinblick auf die beabsichtigte Synthese von DNA wäre ein solches Gemisch unbrauchbar.
Das in der Erdkruste häufig vorkommende Magnesium-Ion müsste fehlen, damit die Reaktion stattfindet – ein praktisch unüberwindbares Problem.
Ein weiteres Problem sind die Ausbeuten der von Teichert et al. veröffentlichten Reaktionen. Die angesprochene Reaktion wurde für alle vier kanonischen Nukleoside durchgeführt. Dabei ergaben sich für drei 2‘-Desoxy-Nukleoside (Adenosin, Guanosin, Thymidin) Ausbeuten von unter einem Prozent. Nur im Fall von 2‘-Desoxy-Cytidin lag die Ausbeute bei immer noch mageren 2,5 %. Das sind relativ dürftige Ergebnisse. Angesichts des schwerwiegenden präbiotischen „Verdünnungsproblems“ sind diese Resultate in keiner Weise überzeugend.
Es ist noch wichtig zu erwähnen, dass die Reaktion in Gegenwart von Magnesium-Salzen kaum abläuft, wie der Originalliteratur entnommen werden kann. Das aber bedeutet, dass ein in der Erdkruste häufig vorkommendes Ion abwesend sein müsste, damit die Reaktion stattfindet – ein praktisch unüberwindbares Problem für dieses hypothetische Szenario der Entstehung der Bausteine der DNA. Schließlich stellt sich die Frage, warum Teichert et al. die Entstehung von DNA-Bausteinen ohne angefügte Phosphatgruppen simulierten. Denn ohne Phosphatgruppen ist die Weiterreaktion der Bausteine zu DNA-Makromolekülen absolut ausgeschlossen.
Fazit
Insgesamt liefert die Arbeit von Teichert et al. kein gutes Argument für eine mögliche Entstehung von Desoxy-Nukleosiden unter plausiblen präbiotischen Bedingungen. Vielmehr verdeutlicht die Arbeit erneut, dass Moleküle des Lebens nur mithilfe ausgefeilter Experimentierkunst hergestellt werden können.
Asphalt, Water, and the Prebiotic Synthesis of Ribose, Ribonucleotides and RNA. Acc. Chem. Res. 12, 2025-2034.
Neue Synthese für Nukleinsäure-Bausteine – ein plausibler Weg zu ersten Nukleinsäuren? Stud. Integr. J. 16, 111-113.
Efficient enzyme-free copying of all four nucleobases template by immobilized RNA. Nature Chemistry 3, 603-608.
One-Step, Regioselective Synthesis of up to 50-mers of RNA Oligomers by Montmorillonite Catalysis. J. Am. Chem. Soc. 128, 8914-8919.
The RNA world, Nature 319, 618.
Instability and decay of the primary structure of DNA. Nature 362, 709-715.
Synthesis of activated pyrimidine ribonucleotides in prebiotically plausible conditions. Nature 459, 239-242.
RNA-Welt: Krise überwunden? Stud. Integr. J. 21, 22-28.
Directed prebiotic pathway of DNA nucleosides. Angew. Chem. 131, 10049-10052; Angew. Chem. Int. Ed. 58, 9944-9947.
Themen | Kurzbeiträge | Streiflichter
Studiengemeinschaft WORT und WISSEN e.V.
Letzte Änderung: 6/15/21
Webmaster