Das Geheimnis der Verformbarkeit roter Blutzellen
Rote Blutzellen (Erythrozyten) sind bekanntlich verantwortlich für den Transport von Sauerstoff im Blut und für den Rücktransport von Kohlendioxid zu den Lungen. Diese Funktion basiert hauptsächlich auf der chemischen Struktur des roten Blutfarbstoffes Hämoglobin und den besonderen Eigenschaften ihres Zellskeletts. Die Abgabe von Sauerstoff beziehungsweise die Aufnahme von Kohlendioxid erfolgt in Kapillaren der Lungen bzw. des Zielgewebes; die Kapillaren sind die kleinsten Blutgefäße des Organismus. Sie sind etwa 0,5 mm lang und haben einen Durchmesser von 5 bis 10 µm. Der maximale Durchmesser der Erythrozyten beträgt ca. 7,5 µm und an ihren Rändern sind sie ca. 2 µm dick (Abb. 1). Diese frisbeeähnliche Form garantiert eine große Kontaktfläche für den Gasaustausch. Würde man die Oberflächen aller Erythrozyten nebeneinanderlegen, würde man bei einem gesunden Erwachsenen auf eine Fläche von ca. 4000-4500 m2 kommen, das entspricht etwa 75 % eines Fußballfeldes. Wie gelangen aber die 7,5 µm „dicken“ Blutzellen durch die teilweise nur 5 µm großen Kapillaren, ohne zu zerplatzen bzw. die Kapillaren zu verstopfen?

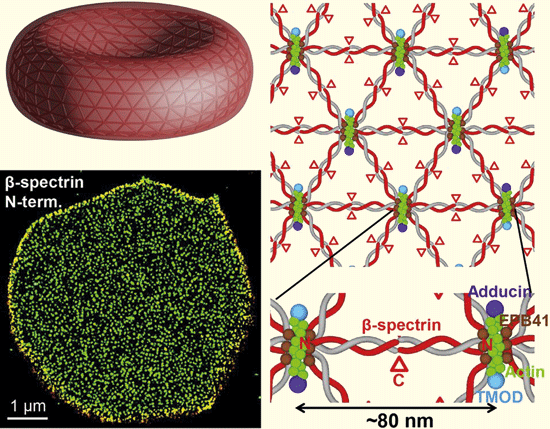
Abb. 1: Oben links: Erythrozyt (rotes Blutkörperchen) mit seiner typischen frisbeeähnlichen Form, Durchmesser 7,5 µm, Dicke am Rand 2 µm. Unten links: Darstellung der für die Elastizität verantwortlichen Proteine (Spektrin) in der Membran von Erythrozyten (grüne Punkte), einzelne schwarze Lücken in dem Proteinteppich sind keine Defekte, sondern dienen einer schnellen Formänderung. Rechts: Schema der Anordnung der Proteinketten des Spektrins als Netzwerk, entspannt haben die einzelnen Knotenpunkte einen Abstand von 80 nm, unter Spannung kann der Abstand der Knotenpunkte bis auf 180-190 nm vergrößert werden. (Aus Pan et al. 2018, Abdruck mit freundlicher Genehmigung)
Elektronenmikroskopisch konnte bislang an toten Erythrozyten gezeigt werden, dass ihre Membran (äußere Hülle) und ihr Zellskelett hochflexibel und sehr robust sind. Diese Untersuchungen beantworteten aber nicht alle Fragen. Eine neue innovative Mikroskopiertechnik mit einer örtlichen Auflösung von 25 nm (nm = Millionstel Millimeter) (STORM – Stochastic Optical Reconstruktion Microscopy) erlaubte es dem Team um L. Pan von der University of California in Berkeley, die Ultrastruktur des Zellskeletts lebender Blutzellen zu entschlüsseln. Dabei wiesen sie in den Membranen der Erythrozyten ein netzförmig aufgebautes Protein nach, das Spektrin, welches aus zu Dreiecken verknüpften, elastischen Molekülketten mit einer Kantenlänge von 80 nm besteht (Abb. 1b und c).
Vergleichbare netzförmige Proteinverbände wurden bereits in den Zellwänden von neuronalen Zellen (Zellen, die zum Nervensystem gehören) gefunden; dort zeigen die einzelnen Molekülketten eine Kantenlänge von 180-190 nm. Dieser Unterschied erklärt sich daraus, dass die Molekülketten bei Letzteren durch andere Zellbestandteile (Mikrotubuli, Neurofilamente) unter ständiger Spannung gehalten werden, die in den Erythrozyten fehlen, weshalb dort die Molekülketten entspannt bzw. relaxiert vorliegen. Das ist funktionell höchst sinnvoll.Die in den Erythrozyten angeordneten entspannten Molekülketten lassen eine Dehnung bis auf 190 nm zu und bilden damit ein hochflexibles federndes Maschenwerk. Daraus erklärt sich einerseits die hohe Verformbarkeit und Elastizität und anderseits die Robustheit der Erythrozyten, wenn sie durch die Kapillaren „gequetscht“ werden. Überrascht wurde die Forschergruppe durch den Befund, dass innerhalb des hochelastischen Netzwerkes große Lücken klaffen. Diese stellen keine Defekte und keine Fehlkonstruktion dar, sondern erlauben den Erythrozyten eine sehr schnelle Formänderung – so die Interpretation der Forscher. Die Löcher wirken hier wie Beugepunkte und garantieren ein noch größeres Potenzial für eine kurzfristig erforderliche Verformbarkeit in den Kapillaren. Diese Erkenntnisse sind auch für die medizinische Erforschung der Malaria von größtem Interesse, da bekannt ist, dass die Malaria-Erreger mit dem Zellskelett der roten Blutkörperchen interagieren. Blutzellen, die ihre Flexibilität und damit die Funktionalität des oben beschriebenen elastischen Netzwerkes der Zellmembran aufgrund von Veränderungen der chemischen Struktur des Hämoglobins verloren haben (sogenannte Sichelzellen), sind bekanntlich resistent gegenüber den Malariaerregern.
Diskussion. Der von der Arbeitsgruppe um L. Pan beschriebene Merkmalskomplex ist ein herausforderndes Design-Merkmal. Das elastische maschenartige Netzwerk ist nicht genetisch codiert (nur dessen Eiweißbausteine), aber höchst präzise in die physiologischen Wechselwirkungen sowie anatomischen Gegebenheiten eingepasst, und das über mehrere hierarchische Stufen, von der molekularen Ebene im Nanometerbereich bis zur Organebene. Ein evolutionärer Mechanismus, der unabhängig von Veränderungen der genetischen Grundlagen kreativ agiert und, wie hier gezeigt, die beste stereochemische Konfiguration von Proteinen in Korrelation zu den lokal erforderlichen funktionellen Anforderungen ermöglicht, ist unbekannt. Rote Blutzellen sind Abkömmlinge von Stammzellen der Blutbildung, in denen ein riesiges Potential an Entwicklungsprogrammen angelegt ist (z. B. für die bekannte Vielzahl weißer Blutzellen oder für Thrombozyten). Diese Entwicklungsprogramme werden unter dem Einfluss hochkomplexer biochemischer Steuermechanismen aktiviert oder unterdrückt. Die evolutionäre Ableitung roter Blutkörperchen und des speziell hier beschriebenen elastischen Netzwerkes innerhalb der Zellmembranen ist ohne koordinierte und korrelierende Veränderungen des ursprünglichen Blutbildungssystems undenkbar und deshalb auf der Basis bisher diskutierter Evolutionsmechanismen nicht einmal in Ansätzen zu verstehen.
H. Ullrich
[Pan L, Yan R, Li W & Ku K (2018) Super-Resolution Microscopy Reveals the Native Ultrastructure of the Erythrocyte Cytoskeleton. Cell Reports 22, 1151-1158.]