Neues zur präbiotischen Entstehung von Stickstoffbasen
In der Biogeneseforschung (erstmalige Entstehung des Lebens) wird eine unmittelbare Bildung von Nukleinsäuren (DNA, RNA) aus einfachen anorganischen Molekülen unter anderem aufgrund der hohen Komplexität dieser Makromoleküle generell ausgeschlossen. Alternativ dazu bleibt die Möglichkeit der stufenweisen Synthese über die weniger komplexen organischen Moleküle (Desoxy-)Ribose und Stickstoffbasen.1 Neben einer Vielzahl offener Fragen zur Herkunft der Zuckereinheiten (Ribose bzw. Desoxyribose) von Nukleinsäuren ist auch der Hergang der präbiotischen Entstehung der Stickstoffbasen (Adenin, Guanin, Purin etc.) nicht geklärt. In der Literatur werden zwei verschiedene Erklärungen für den Ursprung dieser Molekülsorte angeführt. Als eine mögliche Quelle von Stickstoffbasen werden Meteoriten in Betracht gezogen (Callahan 2011). Allerdings ist das nachgewiesene Vorkommen von Stickstoffbasen auf Meteoritengestein im Vergleich zu anderen organischen Verbindungen sehr gering. Ebenso sind Fälle von Kontaminationen irdischen Ursprungs im Zusammenhang mit der Untersuchung von Meteoritengestein auf Stickstoffbasen bekannt. Als Alternative wird die Entstehung von Stickstoffbasen auf unserem Planeten diskutiert.

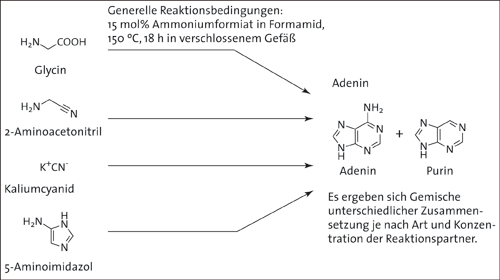
Abb. 1: Ausgangsstoffe, Reaktionsbedingungen und Produkte der von Krishnamurthy diskutierten, potentiell präbiotischen Entstehung der Stickstoffbasen Adenin und Purin.
Ein kürzlich veröffentlichter Artikel zu dieser Fragestellung stammt von der Forschergruppe um Krishnamurthy (2012). Darin wird die Synthese von Purin bzw. Adenin durch Erhitzen von Kaliumcyanid oder einfacher Moleküle wie Glycin, 2-Aminoacetonitril bzw. 5-Aminoimidazol in einer hoch konzentrierten Lösung von Ammoniumformiat in reinem Formamid auf 150 °C beschrieben (siehe Abb. 1). Zur Stützung der Plausibilität dieses Reaktionswegs werden hauptsächlich zwei Argumente angeführt: Zum einen sei eine Anreicherung des Formamids aufgrund des im Vergleich zum Wasser geringeren Dampfdrucks wahrscheinlicher als diejenige von Blausäure, die in früheren experimentellen Arbeiten als Ausgangsstoff angenommen wurde (Oró 1960). Zum anderen wird die Ähnlichkeit des Reaktionsverlaufs zur Biosynthese des Adenins angeführt. Solche Ähnlichkeiten könnten nach Ansicht der Autoren bei der Aufklärung der Evolution früher, für den Stoffwechsel von Lebewesen relevanter Reaktionskaskaden hilfreich sein.
Auch wenn die Ergebnisse der Arbeit gegenüber früheren Modellen (Oró 1960) einige Vorteile aufweisen, kann dieses Experiment jedoch kaum als plausible Simulation einer präbiotischen Synthese gewertet werden. Denn die angenommenen Voraussetzungen sind unter geologischen Verhältnissen sehr unwahrscheinlich. Dazu gehören die außerordentlich hohe Konzentration an Ammoniumformiat (4.4 M oder 15 mol%, d. h. das Verhältnis von Ammoniumformiat zu Formamid ist 3:17, eine unwahrscheinlich hohe Konzentration!), die Verwendung reiner Ausgangsverbindungen wie z. B. des Lösungsmittels Formamid und eines geschlossenen Reaktionsgefäßes, das keinen Austausch von Materie mit der Umgebung ermöglicht und eine Verflüchtigung der Bestandteile des Gemischs verhindert. Auch das allgegenwärtige Wasser durfte in diesen Gemischen nicht enthalten gewesen sein.
Noch wesentlich größere Schwierigkeiten beinhaltet die Frage, wie ein solches Gemisch zustande gekommen sein könnte. Es ist fraglich und eine Untersuchung wert, ob ein vergleichbares Experiment im Sinne einer Anreicherung der Komponenten aus einer verdünnten wässrigen Lösung ebenfalls zu Stickstoffbasen führen würde. Denn in diesem Fall könnten auch die wichtigen, zwischenzeitlich gebildeten Komponenten Blausäure und Ammoniak aus der Lösung verdampfen. Es erscheint daher naheliegend, dass die Wahl der Reaktionsbedingungen im Blick auf das erwünschte Ergebnis konzipiert worden ist. Auch der Verweis auf die Ähnlichkeit des diskutierten Reaktionswegs mit der Biosynthese von Adenin ist nicht notwendigerweise ein hilfreiches Indiz für die Aufklärung postulierter evolutiver Prozesse. Diese Resultate zeigen nur, dass es möglich ist, Bedingungen zu finden, unter denen eine Reaktionskaskade außerhalb des zellulären Kontextes über einen ähnlichen Weg verläuft wie diejenige des betrachteten Stoffwechselvorgangs.
B. Schmidtgall
[Binder H (2009) Neue Synthese für Nukleinsäure-Bausteine – ein plausibler Weg zu ersten Nukleinsäuren? Stud. Int. J. 16, 111-113; Callahan MP, Smith KE, Cleaves HJ, Ruzicka J, Stern JC, Glavin DP, House CH & Dworkin JP (2011) Carbonaceous meteorites contain a wide range of extraterrestrial nucleobases. Proc. Natl. Acad. Sci. 108, 13995-13998; Hudson JS, Eberle JF, Vachhani RH, Rogers LC, Wade JH, Krishnamurthy & Springsteen G (2012) A unified Mechanism for Abiotic Adenine and Purine Synthesis in Formamide. Angew. Chem. 124, 5224-5227; Oró J (1960) Synthesis of adenine from ammonium cyanide. Biochem. Biophys. Res. Commun. 2, 407-412; Powner MW, Gerland B & Sutherland JD (2009) Synthesis of activated pyrimidine ribonucleotides in prebiotically plausible conditions. Nature 459, 239-242.]
1 Die Arbeitsgruppe von Sutherland (Powner et al. 2009) hat eine Synthese von Nukleotiden vorgestellt, die freie Ribose und N-Basen umgeht. Auch dieser Vorschlag stellt bisher jedoch keine plausible Antwort auf die Frage nach ersten Nukleotiden dar (Binder 2009).