Homochiralität: astrophysikalischer Mechanismus
zur Anreicherung von Aminosäure-Enantiomeren?
Für die Entstehung homochiraler Bausteine für die Synthese von Biomakromolekülen liegt nach wie vor keine befriedigende rein kausalmechanistische Erklärung vor (Imming 2006). Wie können Moleküle, die in spiegelbildlichen Strukturvarianten (Enantiomeren; vgl. Abb. 1) vorkommen und sich in ihren chemischen Eigenschaften praktisch nicht unterscheiden (wie z.B. Aminosäuren und Kohlehydrate) so getrennt werden, dass daraus einheitliche Makromoleküle aufgebaut werden können?

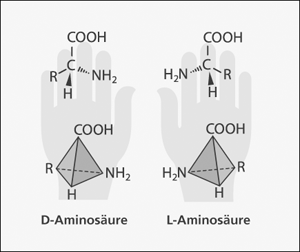
Abb.1: D- und L-Aminosäure. Die beiden Formen sind spiegelbildlich zueinander. Alle Aminosäuren haben die gleiche Grundstruktur (L-Aminosäuren) und unterscheiden sich nur im Rest R. In Ursuppenexperimenten werden immer beide Formen zu gleichenTeilen gebildet (Razemate). (Aus Junker & Scherer 2006)
Ohne homochirale Bausteine ist Leben – wie wir es kennen – nicht möglich. Die Trennung von Enantiomeren gelingt im Labor, erfordert jedoch zwingend den Einsatz homochiraler Chemikalien sowie geplante und regulierte Versuchsabläufe.
Schon seit längerem und auch jetzt wieder in neuen Untersuchungen sind Techniken ausgearbeitet worden, um Mischungen mit einem geringen Enantiomerenüberschuss so anzureichern, dass anschließend ein Enantiomer stark überwiegt. Perry et al. (2007) haben gefunden, dass das D/L-Gemisch der Aminosäure Serin mit einem geringen Enantiomerenüberschuss durch Sublimation angereichert werden kann. Bei der Sublimation geht ein Stoff direkt aus der festen Phase in die Gasphase über (und umgekehrt). Dieses Phänomen ist thermodynamisch gut beschreibbar und wird im Labor z.B. zur Reinigung von Reaktionsprodukten genutzt. Klussmann et al. (2006) haben kürzlich gezeigt, dass eine Anreicherung von Aminosäure-Enantiomeren auch durch Nutzung des Phasenübergangs fest – gelöst möglich ist.
Die Publikation von Perry et al. (2007) veranlasste Ben Feringa und Mitarbeiter, eigene Untersuchungen über die Anreicherung von Enantiomeren durch Sublimation zu veröffentlichen (Fletscher et al. 2007). Sie sublimierten verschiedene Aminosäuren mit einem geringen Enantiomerenüberschuss von 0,5 bis 10%. Das im Überschuss vorliegende Enantiomer wurde dabei angereichert. Dabei darf nur eine geringe Menge (im Promille-Bereich) des Ausgangsmaterials sublimiert werden. Der Effekt zeigt außerdem eine Abhängigkeit von Druck und Temperatur. In der Überschrift vermitteln die Autoren den Eindruck, einen relevanten astrophysikalischen Mechanismus zur Anreicherung von L-Aminosäuren vorzustellen. Aufgrund der bisher vorliegenden Daten sollte diese Behauptung allerdings kritisch hinterfragt werden. Im Kosmos können lokal hohe Temperaturunterschiede auftreten und es herrscht ein stark reduzierter Druck (Vakuum). Diese Randbedingungen sind für Sublimation günstig, trotzdem wäre zu zeigen, wie gut eine Sublimationsapparatur die Situation im Kosmos modelliert. Nachzuweisen bleibt ebenso, ob der Anreicherungseffekt auch bei Ausgangssituationen auftritt, in denen nicht reine Aminosäuren vorgelegt werden, sondern komplexe Substanzgemische mit Spuren von Aminosäuren, wie das unter präbiotischen Bedingungen zu erwarten ist. Wie soll außerdem unter ungesteuerten Bedingungen sichergestellt werden, dass nur geringste Anteile (Promille) der Aminosäuren sublimiert werden?
Abschließend sei auf die schon vor längerem von Klaus Dose (1987) gemachte Feststellung hingewiesen: „Es gibt zwar schwache asymmetrische Kräfte in der unbelebten Natur, aber jedes geringfügige Vorherrschen von D- oder L-Formen bei präbiotischen Prozessen würde in einer geologischen Umgebung durch Razemisierungsreaktionen wieder aufgehoben werden.“ An dieser Einschätzung hat sich bis heute nichts geändert, wie Cataldo (2005) in ihrem Übersichtsartikel belegen, wenn sie schreiben: „The enantiomeric excess found in meteorites usually involves unusual aminoacids which are not common in terrestrial environment and which are much less prone to racemization than the corresponding terrestrial a-aminoacids which instead are usually found as chiral mixtures.“
Unter natürlichen Bedingungen, z.B. im Kosmos, razemisieren Aminosäuren schneller, als dass durch Mechanismen wie die hier beschriebenen Enantiomerenüberschüsse verstärkt werden könnten.
Selbst wenn die aufgezeigten Schwierigkeiten befriedigend gelöst werden könnten, wäre damit immer noch nicht plausibel erklärt, warum in der Natur fast ausschließlich L-Aminosäuren in Proteine eingebaut werden und D-Zucker in Nukleinsäuren. Manche mutig formulierte Überschriften wünschte man sich mit einem Fragezeichen abgeschlossen.
HB
[Cataldo F, Brucato JR & Keheyan Y (2005) Chirality in prebiotic molecules and the phenomenon of photo- and radioracemization, J. Phys., Conference Series 6, 136-148; Dose K (1987) Präbiotische Evolution und der Ursprung des Lebens. Chemie in unserer Zeit 21, 177-185; Fletcher SP, Jagt RBC & Feringa BL (2007) An astrophysically-relevant mechanism for amino acid enantiomer enrichment. Chem. Commun. 2578-2580; Imming P (2006) Die fehlenden Spiegelbilder. Erklärungsversuche für das Phänomen der natürlichen Homochiralität. Stud. Int. J. 13, 14-21 und http://www.genesisnet.info/schoepfung_evolution/e42081.php; Klussmann M, Iwamura H, Mathew SP, Wells Jr DH, Pandya U, Amstrong A & Blackmond DG (2006) Thermodynamic control of asymmetric amplification in amino acid catalysis. Nature 441, 621-623; Perry RH, Wu C, Nefliu M & Cooks RG (2007) Serine sublimes with spontaneous chiral amplification. Chem. Commun. 1071-1073]