Der Evolution auf die Sprünge helfen
Downloads
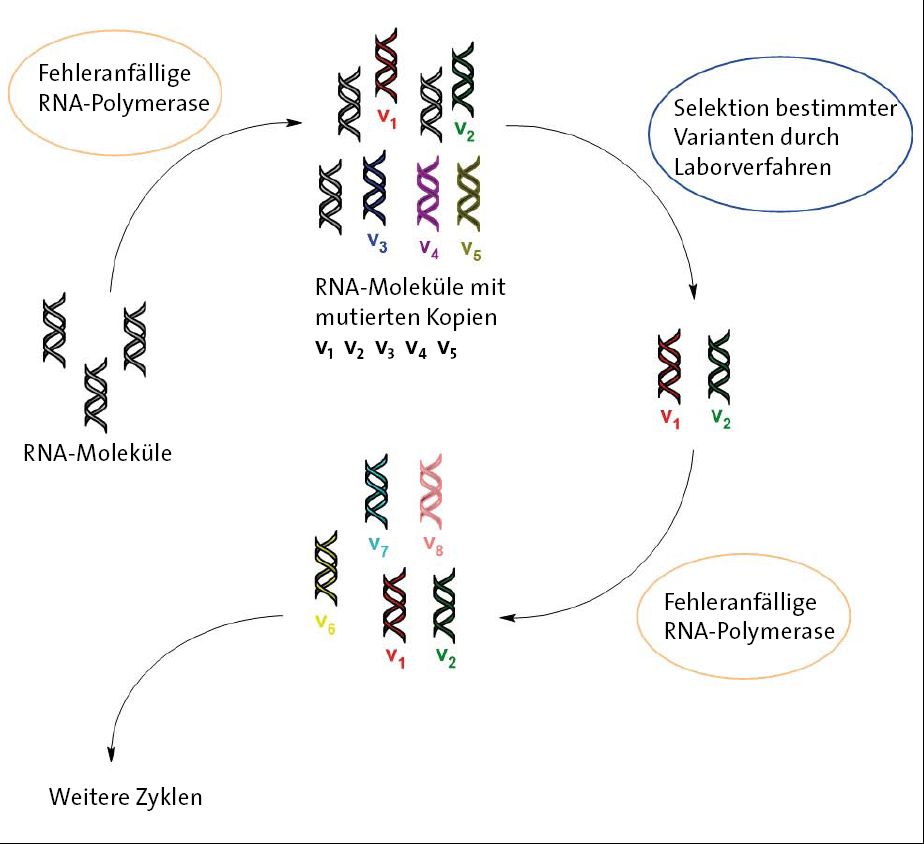
Abb. 1 (Introbild) Vereinfachtes Schema der gerichteten Evolution von RNA-Molekülen.
Bis heute gilt die „RNA-Welt“ als eines der beliebtesten Modelle für den „primitiven“ Anfang des Lebens (Gilbert 1986). Der Grund dafür ist die Fähigkeit von RNA-Molekülen, sowohl genetische Information zu speichern, als auch chemische Reaktionen zu beschleunigen (Katalyse). Dagegen können DNA-Moleküle lediglich Information speichern und Proteine sind auf die Katalyse beschränkt.
Es sind bereits viele Versuche unternommen worden, die RNA-Welt-Hypothese experimentell zu bestätigen. Der Ansatz, RNA-Moleküle in Abwesenheit von Enzymen zu replizieren, erwies sich als chemisch außerordentlich anspruchsvoll und konnte nur mithilfe von ausgefeilten Verfahren im Labor bewerkstelligt werden (Deck et al. 2011; Schmidtgall 2013). Neuere, verfeinerte RNA-Welt-Hypothesen erwiesen sich ebenfalls als unrealistisch und beruhen auf der Betrachtung hochgradig artifizieller chemischer Systeme (Hernandez & Piccirilli 2013; Schmidtgall 2014).
Kürzlich hat die Forschungsgruppe um Gerald Joyce die Ergebnisse einer Arbeit zur „Evolution katalytisch aktiver RNA“ veröffentlicht (Papastavrou et al. 2024). Darin vergleichen sie zwei durch „gerichtete Evolution“ erhaltene Ribozym-Polymerasen (katalytisch aktive RNA-Moleküle) hinsichtlich ihrer Fähigkeit, das Hammerhead-Ribozym zu vervielfachen – ein RNA-Molekül, das andere RNA-Moleküle spaltet. Von der stärker fehleranfälligen Variante der Ribozym-
Polymerase wurde schon früher berichtet. In der aktuellen Veröffentlichung stand die Leistungsfähigkeit der deutlich verbesserten Variante im Vordergrund. Auf den unbedarften Leser können die Ausführungen zunächst den Eindruck erwecken, hier sei im Labor durch natürliche Evolution eine Höherentwicklung der Ribozym-Polymerase erreicht worden, die eine verbesserte Fitness zur Folge hatte. Ist damit die RNA-Welt-Hypothese tatsächlich plausibilisiert worden?
Bei näherer Betrachtung des Schlüsselbegriffs „gerichtete Evolution“ und der experimentellen Daten ergibt sich jedoch ein anderes Bild. Unter „gerichteter Evolution“ versteht man eine Labormethode zur Herstellung von biologischen Kettenmolekülen wie Proteinen oder RNA durch wiederholte Zyklen aus Mutationen und Selektion an Makromolekül-Bibliotheken (große Zahl verschiedener Varianten) (Vidal et al. 2023). Mutierte Varianten von RNA-Molekülen werden meistens durch Vervielfältigung (Replikation) mit einem speziellen, fehleranfälligen Kopierverfahren erhalten – der Polymerase-Kettenreaktion mit einer weniger effizienten RNA-Polymerase. Auf diese Weise wird die natürliche Mutationsrate beschleunigt, um in einem akzeptablen Zeitrahmen zu Ergebnissen kommen zu können. Die Identifikation der gewünschten Varianten erfolgt durch verschiedene Methoden, die allgemein als „Screening“ oder „Selektion“ bezeichnet werden. Beim „Screening“ werden alle erhaltenen Varianten auf bestimmte chemische oder physikalische Eigenschaften hin untersucht. Das kann z. B. die Beschleunigung bestimmter chemischer Reaktionen sein oder die Fähigkeit der Fluoreszenz (Protein emittiert Licht nach Aufnahme von Energie). Bei der „Selektion“ werden die gesuchten Varianten durch Bindung an andere Moleküle gezielt von den anderen Molekülen getrennt. Bei dem Verfahren handelt es sich also offenkundig um ein reines Laborexperiment, das nur entfernt etwas mit dem natürlichen Evolutionsvorgang gemeinsam hat. Sowohl die Vorgabe der fehleranfälligen Polymerase für die Synthese der Ribozym-Varianten als auch das labortechnische Auswahlverfahren der RNA-Varianten entsprechen in keiner Weise einem „natürlichen“ Evolutionsvorgang.
Abgesehen davon zeigte das Experiment, dass das Hammerhead-Ribozym nach acht durch die Ribozym-Polymerasen bewirkten Kopierzyklen weniger gut RNA-Moleküle spaltete als vorher. Es kam also zu teilweisem Funktionsverlust, wenn auch in unterschiedlichem Ausmaß. Beim Einsatz der weniger effizienten Polymerase verlor das Hammerhead-Ribozym seine Funktion nahezu vollständig, bei der verbesserten Polymerase teilweise. Dass im zweiten Fall die Kopierbarkeit des Hammerhead-Ribozyms zunahm, dürfte hierbei wenig relevant sein. Das Ergebnis sieht eher nach Degeneration als nach Höherentwicklung aus. Es scheint also alles andere als leicht zu sein, der molekularen Evolution auf die Sprünge zu helfen.
[Deck C, Jauker M & Richert C (2011) Efficient enzyme-free copying of all four nucleobases template by immobilized RNA. Nature Chemistry 3, 603–608 • Gilbert W (1986) The RNA world. Nature 319, 618 • Hernandez AR & Piccirilli JA (2013) Prebiotic RNA unstuck. Nat. Chem. 5, 360–361 • Papastavrou N et al. (2024) RNA-catalyzed evolution of catalytic RNA. PNAS 121, e2321592121 • Schmidtgall B (2013) Enzymfreie Replikation im Labor – ein plausibles Modell für erste Replikationssysteme? Stud. Integr. J. 20, 48–51 • Schmidtgall B (2014) RNA-Welt: Krise überwunden? Stud. Integr. J. 21, 22–28 • Vidal LS et al. (2023) A primer to directed evolution: current methodologies and future directions. RSC Chem. Biol. 4, 271]
Abb. 1 (Introbild) Vereinfachtes Schema der gerichteten Evolution von RNA-Molekülen.
Bis heute gilt die „RNA-Welt“ als eines der beliebtesten Modelle für den „primitiven“ Anfang des Lebens (Gilbert 1986). Der Grund dafür ist die Fähigkeit von RNA-Molekülen, sowohl genetische Information zu speichern, als auch chemische Reaktionen zu beschleunigen (Katalyse). Dagegen können DNA-Moleküle lediglich Information speichern und Proteine sind auf die Katalyse beschränkt.
Es sind bereits viele Versuche unternommen worden, die RNA-Welt-Hypothese experimentell zu bestätigen. Der Ansatz, RNA-Moleküle in Abwesenheit von Enzymen zu replizieren, erwies sich als chemisch außerordentlich anspruchsvoll und konnte nur mithilfe von ausgefeilten Verfahren im Labor bewerkstelligt werden (Deck et al. 2011; Schmidtgall 2013). Neuere, verfeinerte RNA-Welt-Hypothesen erwiesen sich ebenfalls als unrealistisch und beruhen auf der Betrachtung hochgradig artifizieller chemischer Systeme (Hernandez & Piccirilli 2013; Schmidtgall 2014).
Kürzlich hat die Forschungsgruppe um Gerald Joyce die Ergebnisse einer Arbeit zur „Evolution katalytisch aktiver RNA“ veröffentlicht (Papastavrou et al. 2024). Darin vergleichen sie zwei durch „gerichtete Evolution“ erhaltene Ribozym-Polymerasen (katalytisch aktive RNA-Moleküle) hinsichtlich ihrer Fähigkeit, das Hammerhead-Ribozym zu vervielfachen – ein RNA-Molekül, das andere RNA-Moleküle spaltet. Von der stärker fehleranfälligen Variante der Ribozym-
Polymerase wurde schon früher berichtet. In der aktuellen Veröffentlichung stand die Leistungsfähigkeit der deutlich verbesserten Variante im Vordergrund. Auf den unbedarften Leser können die Ausführungen zunächst den Eindruck erwecken, hier sei im Labor durch natürliche Evolution eine Höherentwicklung der Ribozym-Polymerase erreicht worden, die eine verbesserte Fitness zur Folge hatte. Ist damit die RNA-Welt-Hypothese tatsächlich plausibilisiert worden?
Bei näherer Betrachtung des Schlüsselbegriffs „gerichtete Evolution“ und der experimentellen Daten ergibt sich jedoch ein anderes Bild. Unter „gerichteter Evolution“ versteht man eine Labormethode zur Herstellung von biologischen Kettenmolekülen wie Proteinen oder RNA durch wiederholte Zyklen aus Mutationen und Selektion an Makromolekül-Bibliotheken (große Zahl verschiedener Varianten) (Vidal et al. 2023). Mutierte Varianten von RNA-Molekülen werden meistens durch Vervielfältigung (Replikation) mit einem speziellen, fehleranfälligen Kopierverfahren erhalten – der Polymerase-Kettenreaktion mit einer weniger effizienten RNA-Polymerase. Auf diese Weise wird die natürliche Mutationsrate beschleunigt, um in einem akzeptablen Zeitrahmen zu Ergebnissen kommen zu können. Die Identifikation der gewünschten Varianten erfolgt durch verschiedene Methoden, die allgemein als „Screening“ oder „Selektion“ bezeichnet werden. Beim „Screening“ werden alle erhaltenen Varianten auf bestimmte chemische oder physikalische Eigenschaften hin untersucht. Das kann z. B. die Beschleunigung bestimmter chemischer Reaktionen sein oder die Fähigkeit der Fluoreszenz (Protein emittiert Licht nach Aufnahme von Energie). Bei der „Selektion“ werden die gesuchten Varianten durch Bindung an andere Moleküle gezielt von den anderen Molekülen getrennt. Bei dem Verfahren handelt es sich also offenkundig um ein reines Laborexperiment, das nur entfernt etwas mit dem natürlichen Evolutionsvorgang gemeinsam hat. Sowohl die Vorgabe der fehleranfälligen Polymerase für die Synthese der Ribozym-Varianten als auch das labortechnische Auswahlverfahren der RNA-Varianten entsprechen in keiner Weise einem „natürlichen“ Evolutionsvorgang.
Abgesehen davon zeigte das Experiment, dass das Hammerhead-Ribozym nach acht durch die Ribozym-Polymerasen bewirkten Kopierzyklen weniger gut RNA-Moleküle spaltete als vorher. Es kam also zu teilweisem Funktionsverlust, wenn auch in unterschiedlichem Ausmaß. Beim Einsatz der weniger effizienten Polymerase verlor das Hammerhead-Ribozym seine Funktion nahezu vollständig, bei der verbesserten Polymerase teilweise. Dass im zweiten Fall die Kopierbarkeit des Hammerhead-Ribozyms zunahm, dürfte hierbei wenig relevant sein. Das Ergebnis sieht eher nach Degeneration als nach Höherentwicklung aus. Es scheint also alles andere als leicht zu sein, der molekularen Evolution auf die Sprünge zu helfen.
[Deck C, Jauker M & Richert C (2011) Efficient enzyme-free copying of all four nucleobases template by immobilized RNA. Nature Chemistry 3, 603–608 • Gilbert W (1986) The RNA world. Nature 319, 618 • Hernandez AR & Piccirilli JA (2013) Prebiotic RNA unstuck. Nat. Chem. 5, 360–361 • Papastavrou N et al. (2024) RNA-catalyzed evolution of catalytic RNA. PNAS 121, e2321592121 • Schmidtgall B (2013) Enzymfreie Replikation im Labor – ein plausibles Modell für erste Replikationssysteme? Stud. Integr. J. 20, 48–51 • Schmidtgall B (2014) RNA-Welt: Krise überwunden? Stud. Integr. J. 21, 22–28 • Vidal LS et al. (2023) A primer to directed evolution: current methodologies and future directions. RSC Chem. Biol. 4, 271]
