Die „Sauerstoffkatastrophe“
3. Biologische Schutzvorrichtungen gegen oxidativen Stress
Downloads
Die „Sauerstoffkatastrophe“
3. Biologische Schutzvorrichtungen gegen oxidativen Stress
Sauerstoff ist für den Energiehaushalt vieler Lebewesen unverzichtbar. Zugleich sind viele Reaktionsprodukte des Sauerstoffs für Organismen in hohem Maße schädlich. Sie verursachen sogenannten „oxidativen Stress“. Daher sind vielfältige hochkomplexe molekulare Schutzvorrichtungen gegen oxidativen Stress lebensnotwendig. Die Entstehung solcher Vorrichtungen in Lebewesen im Zuge der postulierten großen Sauerstoffkatastrophe durch evolutive Vorgänge erscheint in hohem Maße unplausibel. Aus schöpfungstheoretischer Perspektive bieten sich hier weit bessere Erklärungsmöglichkeiten.
Kompakt
Im Rahmen der Evolutionslehre wird angenommen, dass der auf Sauerstoff beruhende (aerobe) Energiestoffwechsel in den Zellen im Zuge der „großen Sauerstoffkatastrophe“ durch Evolution aus strikt anaeroben* Organismen entstand. Während der aerobe* Stoffwechsel hinsichtlich der Effektivität gegenüber dem anaeroben vorteilhaft ist, stellt der Umgang mit giftigen Reaktionsprodukten des Sauerstoffs, den „reactive oxygen species“ (ROS), eine besondere Herausforderung dar. Schäden durch ROS treten sehr schnell und bei sehr vielen Arten von Biomolekülen ein. Proteine werden durch Reaktionen mit ROS zur Entfaltung (Denaturierung) veranlasst und verlieren ihre Funktion, bei der DNA kommt es zu Mutationen oder der Blockade von Ableseprozessen, mehrfach ungesättigte Fettsäurebausteine aus Membranen von Eukaryoten* sind ebenfalls für Schäden durch ROS anfällig. Daher verfügen alle aeroben Organismen über eine große Vielfalt an Einrichtungen zum Schutz und zur Reparatur von Biomolekülen. Untersuchungen solcher Vorrichtungen haben wiederholt gezeigt, dass es sich dabei in der Regel um anspruchsvolle und nichtreduzierbar komplexe Systeme handelt, die offenkundig teleologischer (zielgerichteter) Natur sind. Zudem können Organismen ohne solche Systeme nicht in einer mit Sauerstoff angereicherten Atmosphäre überleben.
Evolutionäre Hypothesen beschränken sich auf das Herausgreifen von Einzelaspekten wie etwa der vergleichenden Analyse von ROS-abbauenden Enzymen in allen Lebewesen oder rein hypothetischen Annahmen wie der Vorbereitung von Organismen auf ROS durch „reactive sulfur species“ (RSS). Insgesamt wird jedoch deutlich, dass schrittweise verlaufende Darwin’sche Vorgänge als Erklärung für eine sehr schnelle und äußerst anspruchsvolle Umrüstung von anaeroben Organismen zu aeroben nicht einmal ansatzweise taugen. Vielmehr weisen die raffiniert eingerichteten und sich gegenseitig ergänzenden Schutzfunktionen auf intelligente Schöpfung hin.
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.
Einleitung
Wann immer ein Antrieb konstruiert wird, stellt sich unmittelbar die Frage nach einer möglichst effizienten Energieverwertung. Nicht weniger wichtig sind jedoch sicherheitstechnische Überlegungen. Treibstoffe von Automobilen sind hochentzündlich, diejenigen von Raketen explosiv. Darüber hinaus sollte die Konstruktion möglichst wenig störanfällig funktionieren. Dies ist wegen einer kaum überschaubaren Zahl an möglichen Ursachen für Funktionsausfälle eine besondere Herausforderung. Dementsprechend heißt es auf der Internetseite eines Expertenteams im Bereich Maschinenbau: „Für Maschinenbauer gehört die Sicherheitstechnik wohl zu den komplexesten und unbeliebtesten Themen.“1 Es müssen viele Eventualitäten im Voraus bedacht und schwierige Entscheidungen getroffen werden, da eingerichtete Sicherheitsfunktionen auch unter unterschiedlichen Bedingungen ihren Zweck erfüllen müssen. Zudem muss gewährleistet sein, dass die Sicherheitsfunktionen die eigentliche Funktion der Maschine nicht nennenswert beeinträchtigen.
Auch in Organismen gibt es eine Vielzahl von Einrichtungen, die Schäden verhindern sollen. Bekannte Beispiele sind das Immunsystem und zelluläre Mechanismen, die Mutationen vorbeugen. Eine weitere Klasse sehr wichtiger Schutzfunktionen bei Lebewesen ist ausgerechnet auf denjenigen chemischen Stoff ausgerichtet, den sehr viele Organismen für ihren Energiehaushalt brauchen: molekularen Sauerstoff (O2). Der Grund dafür ist die Entstehung schädlicher Reaktionsprodukte als Folge verschiedener chemischer Reaktionen von Sauerstoff in Organismen. Für die Evolutionslehre ist dieser Sachverhalt problematisch, da erklärt werden muss, wie Organismen durch einen schrittweisen Vorgang gleichzeitig sowohl einen sauerstoffabhängigen Energiehaushalt als auch eine Reihe von Sicherheitsfunktionen gegen Schäden durch Sauerstoffderivate* erlangt haben können.
Wie in den beiden ersten Folgen zum Thema „Sauerstoffkatastrophe“ ausgeführt, gehen viele Forscher gegenwärtig davon aus, dass die ersten Organismen vor ca. 4 Milliarden Jahren in einer nahezu sauerstofffreien Erdatmosphäre entstanden sein sollen (Knoll & Nowak 2017). Demnach müssten die ersten Organismen Anaerobier* gewesen sein, was unter Kennern des Themas derzeit Konsens ist (Neubeck & Freund 2020). Vor etwa 3 Milliarden Jahren seien dann Sauerstoff-generierende Mikroorganismen evolviert, die für die Anreicherung der Atmosphäre mit Sauerstoff vor ca. 2,4 Milliarden Jahren (Great Oxygenation Event, GOE) verantwortlich sein sollen. Hierbei gehen die Auffassungen bezüglich der Ursachen und des genauen Verlaufs dieses Vorgangs jedoch recht weit auseinander (Schmidtgall 2021). Darüber hinaus wird allgemein angenommen, dass der GOE die Entstehung höherer Organismen überhaupt erst ermöglicht hat – und das trotz der oben erwähnten Schädlichkeit von Sauerstoff. Im Folgenden soll die Frage erörtert werden, ob die Entstehung von Schutzvorrichtungen gegen Schäden durch Sauerstoff durch evolutive Vorgänge im Zuge des GOE plausibel ist.
Schäden durch Sauerstoff in der Zelle
Für den Energiehaushalt vieler Organismen ist molekularer Sauerstoff unverzichtbar. Seine Umwandlung in Wasser in dem als „Zellatmung“ bezeichneten biochemischen Prozess macht den wesentlichen Teil der thermodynamischen* Triebkraft aus, die zur Bildung von ATP, der Energiewährung der Zelle, genutzt wird.
(1) Glucose + 6 O2 ➝ 6 H2O + 6 CO2
∆G = –2870 kJ/Mol Glucose
(Gesamtreaktion der Zellatmung)
Die Nutzung dieser „kontrollierten Verbrennung“ von Kohlenhydraten ermöglicht aeroben* Organismen eine effektivere Art der Energiegewinnung als den Anaerobiern. Der „Treibstoff“ der Aerobier weist eine deutlich höhere Energiedichte auf als derjenige von anaerob lebenden Organismen. Man könnte dies mit der Überlegenheit des Dieseltreibstoffs gegenüber einem Akku elektrisch getriebener Fahrzeuge vergleichen – der erste hat eine ca. 50-fach höhere Energiedichte.
Die Kehrseite der Verwendung von Sauerstoff ist jedoch die Schädlichkeit seiner Reaktionsprodukte. Während das Sauerstoffmolekül selbst praktisch unschädlich ist, wird es bei vielen chemischen und physikalischen Vorgängen in der Zelle in reaktivere Moleküle umgewandelt, die gravierende Schäden verursachen können. Für solche Moleküle hat sich in der Literatur die Sammelbezeichnung „reactive oxygen species“ (ROS) etabliert (Krumova & Cosa 2016). In vielen chemischen Reaktionen des Sauerstoffs in der Zelle entstehen zunächst Superoxidradikale, die anschließend häufig in Wasserstoffperoxid umgesetzt werden (Abb. 1). In weiteren Reaktionen können das besonders reaktive Hydroxylradikal bzw. Radikale verschiedener organischer Verbindungen gebildet werden.
Figure 1. Abb. 1 Die wichtigsten ROS („reactive oxygen species“) und ihre Entstehung aus Sauerstoff durch Aufnahme von Elektronen (e-).
Die jeweiligen ROS gehen je nach ihren Eigenschaften in unterschiedlichem Ausmaß und an verschiedenen molekularen Komponenten der Zelle chemische Reaktionen ein (D’Autréaux & Toledano 2007). Superoxidradikale weisen eine moderate chemische Reaktivität auf und reagieren bevorzugt mit Eisen-Schwefel-Clustern, die in allen Organismen wichtige Funktionen im Energiehaushalt und der Synthese molekularer Bausteine ausführen. Solche Reaktionen können daher zentrale Stoffwechselwege wie die Glykolyse, den Zitratzyklus oder die Synthese bestimmter Aminosäuren beeinträchtigen bzw. zum Erliegen bringen. Wasserstoffperoxid reagiert bevorzugt mit dem Schwefelatom des Cysteins, einer Aminosäure, die in einer Vielzahl von Proteinen aller Organismen vorhanden ist. Durch solche Reaktionen kann es zur Veränderung der dreidimensionalen Struktur der Proteine kommen, sodass sie funktionsunfähig werden. Zudem führen solche Verformungen (Entfaltungen) von Proteinen dazu, dass sie aneinander haften (Aggregation), wodurch sich schwer lösliche und für die Zelle sehr schädliche Plaques bilden.
Aufgrund ihrer Reaktivität unterliegen ROS einer genauen Kontrolle innerhalb der Zelle. Die Konzentration des etwas stabileren Wasserstoffperoxids liegt etwa im nanomolaren* Bereich und ist ungefähr um den Faktor Tausend höher als diejenige des labileren Superoxidradikals (Sies & Jones 2020). Zu Schäden durch ROS kommt es vor allem dann, wenn die hochreaktiven Hydroxylradikale entstehen. Von besonderer Wichtigkeit ist hierbei ein chemischer Prozess, der als Fenton-Reaktion bezeichnet wird (Koppenol & Hider 2019).
(2)2 O2•– + 2 H+ ➝ H2O2 + O2
(Katalysator: Superoxid-Dismutase)
Fenton-Reaktion:
(3)Fe2+ + H2O2 ➝ Fe3+ + OH• + OH–
Superoxidradikale werden schnell durch das Enzym Superoxid-Dismutase (SOD) in Wasserstoffperoxid umgewandelt, das bei Vorhandensein von Fe2+ gespalten wird, sodass sich Hydroxylradikale bilden. Diese Radikale reagieren wahllos mit allen molekularen Komponenten der Zelle. Ob Nukleinsäuren (DNA und RNA), Proteine oder Bestandteile der Zellwand – durch Reaktion mit Hydroxylradikalen entstehen gravierende Schäden in allen Typen biochemischer Funktionseinheiten.
Durch Reaktionen von Hydroxylradikalen mit DNA kommt es zu Mutationen oder zur vollständigen Blockade des Ablesevorgangs der RNA-Polymerase. Vor allem letztere Schäden können für Organismen tödlich sein, wenn sie nicht rechtzeitig repariert werden. In diesem Zusammenhang ist auch zu berücksichtigen, dass die Bildung von ROS in hohem Maße gefördert wird, wenn Moleküle vorhanden sind, die Elektronen auf den Sauerstoff übertragen (s. Kasten „Entstehung von ROS“). Daher muss in Zellen auch die Konzentration freier Metallionen wie Fe2+/3+ und organischer Elektronenüberträger streng kontrolliert werden (Galaris et al. 2019; Imlay 2013). Erhöhte Konzentrationen von ROS und damit einhergehender oxidativer Stress führen relativ schnell zum programmierten Zelltod.
Die Geschwindigkeit, mit der die beschriebenen Schäden durch ROS eintreten, ist unter heutigen Bedingungen sehr hoch. Beispielsweise liegt die Halbwertszeit für beschädigte Eisen-Schwefel-Cluster im Darmbakterium E. coli selbst bei Vorhandensein von ausreichend SOD und einer niedrigen Konzentration von 0,1 nM Superoxidionen im zellulären Milieu bei nur 20 Minuten (Imlay 2013). Das daraus resultierende Problem beschreibt Imlay wie folgt: „Dieser Zeitrahmen ist im Vergleich zu der Zellteilungsrate sehr kurz, weswegen diese Situation nur tolerabel ist, weil Zellen beständig die beschädigten Cluster durch chemische Reduktion und Remetallierung reparieren.“
Es wäre jedoch zu kurz gegriffen, nur im Überschuss an ROS eine Gefahr für die reibungslose Funktion der Zellbiochemie zu sehen. Inzwischen ist auch bekannt, dass eine zu niedrige Konzentration an ROS ebenfalls schädlich ist, da diese Moleküle in allen aeroben Organismen als Botenstoffe fungieren (Go et al. 2015; Sies & Jones 2020). Dementsprechend ist für diese Moleküle auch das Wahren einer definierten Konzentration (Homöostase) notwendig.
Kasten 1 | Entstehung und Nutzung von ROS in der Zelle
ROS können durch chemische Reaktionen des Sauerstoffs mit Biomolekülen der Zelle (endogene* Quellen) oder mit von außen stammenden chemischen Verbindungen (exogene* Quellen) gebildet werden. Bei den Reaktionspartnern, die zur Entstehung von ROS führen, handelt es sich im Allgemeinen um Moleküle, die leicht ein einzelnes Elektron auf Sauerstoffmoleküle übertragen, sodass Superoxidionen entstehen. Zu solchen Quellen von ROS gehören vor allem ungebundene Metallionen (Fe2+, Cu1+) oder organische Elektronenüberträger wie Chinole oder Phenazine (Abb. 2). Aber auch Eisenspeicherproteine und bestimmte eisenhaltige Enzyme können zur Entstehung von ROS beitragen. Bei höheren Lebewesen kommen solche Vorgänge vor allem in Phagozyten (weißen Blutkörperchen) vor. Phagozyten enthalten Transmembran-Enzyme mit der Bezeichnung NADPH-Oxidasen (NOXs), die zur Abtötung von Krankheitserregern Superoxidionen erzeugen und darüber hinaus unverzichtbare Funktionen in der Zelldifferenzierung und dem programmierten Zelltod ausüben (Magnani et al. 2017).
Eine andere bedeutende Quelle von ROS sind Mitochondrien – die „Kraftwerke“ der Zelle. Dort sind vor allem die NADH-Dehydrogenasen (Komplex I) und die Chinole des Q-Pools für einen hohen Eintrag von Superoxidionen ursächlich (Krumova & Cosa 2016). Insgesamt gibt es in menschlichen Zellen über 40 Enzyme, die Superoxidradikale bzw. Wasserstoffperoxid generieren (Go et al. 2015). Darüber hinaus gibt es noch eine Reihe an Enzymen, bei deren normaler Funktion als Nebenprodukt ROS anfallen. Hier sind insbesondere eisenhaltige Cytochrome und Fettsäure-oxidierende Lipoxygenasen zu nennen.
Neben chemischen Reaktionen kann energiereiche Strahlung durch Spaltung chemischer Bindungen (z. B. bei Wasserstoffperoxid) Sauerstoffradikale erzeugen oder das Sauerstoffmolekül in einen angeregten Zustand versetzen (Singulett-Sauerstoff). Solche Vorgänge sind vor allem in Organismen und Geweben relevant, die in erhöhtem Ausmaß dem Licht ausgesetzt sind (Sies & Jones 2020). Es kann also durchaus davon gesprochen werden, dass die Bildung von ROS ein ständiger und weit verbreiteter Vorgang in Zellen ist.
Figure 2. Abb. 2 Strukturformeln und Kalottenmodelle der organischen Elektronenüberträger Chinol und Phenazin (Atomsymbole: grau: Kohlenstoff, rot: Sauerstoff, blau: Stickstoff, weiß: Wasserstoff).
Zelluläre Vorrichtungen zum Schutz gegen oxidativen Stress
Kontrolle der Konzentration an ROS in der Zelle
Da ROS im zellulären Geschehen bei vielen Vorgängen und in vielen Kompartimenten anfallen, bedarf es einer großen Vielfalt von Mechanismen, die für einen Abbau der ROS sorgen. Die Notwendigkeit solcher Schutzvorrichtungen ist bei allen Lebewesen gegeben, die mit Sauerstoff in Kontakt kommen. Bei höheren Lebewesen gelangt der Sauerstoff über Transportmechanismen in die Zellen, während er bei Mikroorganismen einfach durch die Zellwand diffundiert.
Bakterielle Zellwände sind im Unterschied zu denjenigen von höheren Organismen deutlich weniger für Schäden durch ROS anfällig, da sie überwiegend aus gesättigten bzw. einfach ungesättigten Fettsäure-Bausteinen bestehen. Dagegen müssen alle anderen molekularen Komponenten von Zellen stets vor den schädlichen Wirkungen der ROS geschützt werden, und angesichts sehr schnell eintretender Schäden müssen rasche Reparaturprozesse erfolgen. So besitzen selbst kleine Bakterien ausgefeilte mehrstufige Systeme zur Abwehr von oxidativem Stress.
Enzyme: Viele Bakterien (Prokaryoten und Archaeen) und alle höheren Organismen verfügen über verschiedene Enzyme, die Superoxidradikale und Wasserstoffperoxid abbauen (Abb. 3). Der Abbau von Superoxidradikalen erfolgt hauptsächlich durch Enzyme, die als Superoxid-Dismutasen (SOD) bezeichnet werden. Das Funktionsprinzip ist dabei die Beschleunigung des Zerfalls von Superoxidradikalen zu Sauerstoff (O2) und Wasserstoffperoxid (H2O2) (s. Reaktionsgleichung 3). Zudem weisen viele Organismen Katalasen auf, die Wasserstoffperoxid zu Sauerstoff und Wasser zersetzen. Diese Enzyme sind ein sehr effektiver Schutz gegen ROS, da sie diese giftigen (weil sehr reaktiven) Moleküle mit der physikalisch nahezu maximal möglichen Reaktionsgeschwindigkeit von 106-107 Reaktionen pro Sekunde abbauen (Herbert & Pinsent 1948; Milo & Phillips 2016). Diese Reaktionsgeschwindigkeiten gehören zu den schnellsten überhaupt. Sie sind um das 105-Fache höher als durchschnittliche Enzymreaktionen und stellen eher Ausnahmen dar (Milo & Phillips 2016).
Figure 3. Abb. 3 Enzymatischer Abbau von Superoxidradikalen durch SOD (A) und von Wasserstoffperoxid durch Katalasen (B).
Molekulare Regler (Regulons) der Synthese von SOD und Katalasen: Entscheidend für die Wirkung der oben angeführten Enzyme ist ihre Konzentration im zellulären Milieu, die wiederum davon abhängig ist, in welcher Rate sie in der Zelle synthetisiert werden. Hierfür gibt es in bakteriellen Zellen Sensoren, die dafür sorgen, dass die Synthese dieser Enzyme hoch- bzw. herunterfahren wird, je nachdem wie hoch die Belastung durch oxidativen Stress ist (Imlay 2013).
Bei einigen Bakterien fungieren als OxyR bezeichnete Proteine als Regler der Konzentration von Katalasen und SOD. OxyR werden durch Reaktion mit Wasserstoffperoxid oder Superoxidradikalen in eine aktive Form überführt, die durch Aktivieren entsprechender Gene die Synthese von SOD und Katalasen ankurbelt (Pedre et al. 2018). Bei E. coli-Bakterien erfolgt diese Reaktion innerhalb von 1-2 Minuten, nachdem die Zellen mit Wasserstoffperoxid in Kontakt kommen, und ist damit extrem schnell (Storz 2016). Ebbt der oxidative Stress wieder ab, wird OxyR durch Reaktion mit Glutaredoxin, einem kleinen Protein, aus der aktiven wieder in eine inaktive Form überführt. Interessanterweise gibt es bei vielen grampositiven Bakterien ein Detektionssystem für ROS, das in umgekehrter Weise funktioniert: Ein Protein mit der Bezeichnung PerR hemmt in seiner aktiven Form die Synthese von SOD und Katalasen. Durch Reaktion mit H2O2 wird PerR inaktiviert und löst sich von der DNA, sodass die Synthese von ROS-abbauenden Enzymen in Fahrt kommt.
Wie schon zuvor erwähnt, gibt es organische Moleküle, die die Entstehung von Superoxiden durch Elektronentransfer auf Sauerstoff fördern (z. B. Phenazine, Chinole). Solche Moleküle können leicht Zellmembranen durchdringen, da sie selbst fettliebend sind. Im Inneren der Zelle entziehen diese Moleküle bestimmten Komponenten der Atmungskette Elektronen (vor allem von Flavinen) und übertragen sie dann auf Sauerstoff, sodass Superoxidradikale gebildet werden. Es konnte gezeigt werden, dass die Gegenwart von Phenazinen die Superoxid-Konzentration in Bakterienzellen auf das ca. 100-Fache erhöht (Imlay 2013). Daher verfügen Bakterien über ein weiteres regulatorisches Protein (SoxR), das weder auf H2O2 noch auf Superoxidradikale anspricht, sondern auf organische Moleküle, die als Elektronenüberträger fungieren. Auch SoxR fördert in seiner durch ROS aktivierten Form die Synthese von SOD.
Bakterien weisen also ein Schutzsystem auf, das die Zelle auf zweifache Weise gegen oxidativen Stress absichert. Es detektiert sowohl die Moleküle, die die Schäden verursachen (Superoxidradikale, Wasserstoffperoxid), als auch organische Verbindungen, die ihre Entstehung fördern. In beiden Fällen folgt auf die Detektion eine schnelle Reaktion, indem Enzyme hergestellt werden, die die ROS abbauen.
Vitamine und andere kleine Moleküle: Abgesehen von den komplexen Schutzmechanismen durch aufwändige Nanomaschinen gibt es in Organismen eine Reihe von kleinen Molekülen, die in relativ hoher Konzentration im Zellmilieu vorliegen und zum Abfangen der ROS dienen. Besondere Wichtigkeit haben hierbei schwefelhaltige kleine Peptide wie Glutathion oder einige Vitamine. Bei höheren Lebewesen spielen Vitamine im Hinblick auf oxidativen Stress eine wichtigere Rolle als bei Bakterien, da vor allem die Zellmembran höherer Organismen wegen ihrer mehrfach ungesättigten Fettsäure-Bausteine recht empfindlich gegenüber Schäden durch ROS ist. Verhindert werden solche Schäden vor allem durch die gemeinsame Wirkung von Vitamin E (a-Tocopherol) und Vitamin C (Ascorbinsäure). Vitamin E ist ein ausgesprochen fettliebendes Molekül, das deshalb in die Zellwand aufgenommen wird. Es neutralisiert ROS unter Bildung sehr langlebiger Radikale, die für Zellbestandteile sehr viel weniger schädlich sind. An der Grenzfläche von Zellwand und Zellinnenraum werden Vitamin-E-Moleküle durch Reaktion mit Vitamin C wieder regeneriert (Walsh & Tang 2019).
Figure 4. Abb. 4 Abbau von ROS durch chemische Reaktion mit Vitamin E/Vitamin C. Innerhalb der Zellmembran erfolgt der Abbau von ROS durch Reaktion mit Vitamin E (Vit E), wobei es zur Bildung des Semichinons des Vitamin E (Vit E SemiQ) kommt. Vitamin E wird durch Reaktion mit Vitamin C regeneriert, wobei es nach zwei Zyklen zur Bildung des Chinons des Vitamin C kommt. Dieses Molekül wird durch Reaktion mit zwei Molekülen Glutathion (GSH) wieder ins Vitamin C überführt.
Kasten 2 | Funktionsweise der molekularen Regler OxyR und SoxR
OxyR-Proteine weisen an einer bestimmten Stelle exponierte Thiol-(-SH)-Gruppen* auf, die infolge einer Oxidation durch H2O2 eine Disulfidbrücke (-S-S-) bilden (Pedre et al. 2018). Dieser Vorgang zieht eine Veränderung der dreidimensionalen Struktur nach sich, sodass OxyR dann mit einer erhöhten Affinität an bestimmte Genregionen bindet und so die Synthese von SOD und Katalasen fördert. Als Proteine, die durch Binden an die DNA die Transkription bestimmter Gene fördern, zählen die OxyR zu den Transkriptionsfaktoren. Auch das Protein PerR funktioniert nach dem gleichen Prinzip, nur in umgekehrter Weise: Bei geknüpfter Disulfidbrücke weist es eine sehr geringe Affinität zu einer bestimmten DNA-Region auf, während die Spaltung der Brücke eine sehr hohe Affinität bewirkt. Da PerR die Transkription einer DNA-Region verhindert, solange es daran gebunden ist, spricht man von einem Repressor.
SoxR ist ein Protein, das aus zwei Untereinheiten zusammengesetzt ist. Es beinhaltet in jeder Untereinheit jeweils ein oxidationsempfindliches Eisen-Schwefel-Zentrum, das überraschenderweise ausgesprochen selektiv mit organischen Elektronenüberträgern (Chinole, Phenazine) reagiert und nicht mit ROS, wie dies im Fall vieler anderer Fe-S-Zentren geschieht. SoxR bindet stets an die DNA, wobei nur die oxidierte Form die Synthese von SOD anregt. Wenn die giftigen organischen Verbindungen beseitigt sind, wird SoxR reduziert oder abgebaut, sodass die Synthese von SOD nicht weiter aktiviert wird.
Schutz vor den Folgen der Wirkung von ROS und Reparatur beschädigter Biomoleküle
Schutz vor der Aggregation* von Proteinen: Wie oben erwähnt führt oxidativer Stress zu einer verstärkten Fehlfaltung von Proteinen und zur Bildung schädlicher Plaques. Ein wichtiger Mechanismus der Vorbeugung der Proteinaggregation in Lebewesen ist erst in den letzten ca. 30 Jahren näher erforscht worden. Kornberg et al. fanden bereits in den 1990er Jahren heraus, dass Bakterien deutlich empfindlicher auf verschiedene Arten von Stress reagieren, wenn Polyphosphat (polyP) nicht in genügender Konzentration vorliegt (Akiyama et al. 1992). Allerdings fand man erst später heraus, warum es sich so verhält. Bei E. coli-Bakterien, die erhöhten Konzentrationen von H2O2 ausgesetzt wurden, ist eine verstärkte Bildung langer Kettenmoleküle aus Phosphateinheiten (polyP) nachgewiesen worden (Gray et al. 2014). Wie gezeigt werden konnte, verhindern polyP-Moleküle selbst bei hohen Konzentrationen von ROS nahezu komplett die Aggregation von Proteinen. Auch bei Fehlfaltungen von Proteinen in Folge von erhöhten Temperaturen erwiesen sich polyP-Makromoleküle als sehr wirksam, wobei längere polyP-Ketten (>100 Phosphat-Einheiten) effektiver waren als kurze (< 50 Phosphat-Einheiten) (Gray & Jakob 2015). Die Wirkungsweise von polyP-Ketten ist relativ simpel: Sie umwickeln fehlgefaltete Proteine und sorgen aufgrund ihrer vielfachen negativen Ladung für gegenseitige Abstoßung. PolyP-Kettenmoleküle sind chemisch relativ robust und unempfindlich gegenüber Reaktionen mit ROS. Ihre Synthese in E. coli erfolgt durch das Enzym polyP-Kinase (PPK) aus Adenosintriphosphat (ATP) und der Abbau durch Exopolyphosphatasen (PPX). Im Fall von oxidativem Stress werden Exopolyphosphatasen von ROS inhibiert, d. h. unfähig gemacht, ihre Funktion auszuüben. Folglich kommt es zu einer Anhäufung von polyP, sodass die gefährliche Proteinaggregation verhindert wird. Nimmt die Belastung durch ROS wieder ab, sorgen die erneut aktivierten PPX für einen schnellen Abbau von polyP, da es in erhöhter Konzentration ebenfalls giftig ist (Desfougères et al. 2020).
PolyP ist in allen bisher untersuchten Organismen nachgewiesen worden und scheint vor allem in Säugetieren an einer ganzen Reihe von wichtigen Prozessen wie Proteinhomöostase*, Energiehaushalt und programmiertem Zelltod beteiligt zu sein (McIntyre & Solesio 2021). Im Unterschied zu Bakterien sind allerdings viele Details bezüglich der Synthese von polyP und seiner Funktionen in höheren Organismen noch unbekannt (Desfougères et al. 2020). Es kann jedoch festgehalten werden, dass alle Lebewesen, die mit Sauerstoff in Kontakt kommen, ohne polyP und dessen wichtiger Schutzfunktion nicht leben könnten.
Reparatur entfalteter Proteine: Der Schutz durch polyP beschränkt sich auf das Verhindern der Aggregation der Proteine. Schäden an den Proteinen werden dadurch nicht behoben. Wenn also die Stresssituation vorbei ist und das polyP wieder abgebaut wird, ist eine Reparatur der Proteine erforderlich, da sie anderenfalls aggregieren können. Hierfür besitzen wiederum alle Typen von Zellen Proteine, die der Fehlfaltung vorbeugen bzw. fehlerhaft gefaltete Proteine wieder in die richtige Form bringen. Solche Proteine werden allgemein als Chaperone bezeichnet. Während im Fall erhöhter Temperaturen in vielen Organismen die Synthese ATP-abhängiger Hitzeschockproteine aktiviert wird (z. B. Hsp 60 in E. coli), sieht die Strategie bei oxidativem Stress anders aus. Zunächst wird die Synthese von Proteinen hochreguliert, die entfaltete Proteine binden und so die Aggregation verhindern (Holdasen). Holdasen lösen sich erst dann von ihrem Bindungspartner, wenn die ROS abgebaut sind und zusätzlich ein ATP-abhängiges Protein bereitsteht, das entfaltete Protein zu reparieren. Solche Systeme liegen sowohl bei Bakterien vor (E. coli: Hsp33) als auch bei Eukaryoten (Hefe: Get3). Es handelt sich dabei um exakt getaktetes Protein-Teamwork, wie es auch von Reichmann et al. beschrieben wird (Reichmann et al. 2018): „Die Inaktivierung von oxidiertem Hsp33 und die Freisetzung von betroffenen Proteinen werden ebenfalls sorgfältig orchestriert und erfordern nicht nur reduzierende Bedingungen, sondern auch die Anwesenheit von faltenden Chaperonen und ATP, die die Rückfaltung der gebundenen Proteine unterstützen.“
DNA-Reparatur: Schäden an Proteinen zu verhindern und zu beheben ist jedoch bei Weitem nicht ausreichend für die Stabilität einer Zelle unter aeroben Bedingungen, da Auswirkungen von Schäden an der DNA erheblich schwerere Konsequenzen nach sich ziehen. Die Reparatur von DNA-Molekülen ist jedoch nicht weniger aufwändig als diejenige von Proteinen. Das Reparaturprinzip besteht im Ausschneiden beschädigter Teile und anschließendem Ersetzen durch intakte Entsprechungen, wobei es verschiedene Typen von Enzymen für die Reparatur von verschiedenen Schäden an der DNA gibt. Für das Erkennen und Ausschneiden beschädigter Nukleobasen* sind DNA-Glykosylasen zuständig, wobei es je nach Art des Schadens unterschiedliche Enzyme gibt (Steven et al. 2016). Ist die Nukleobase Cystein nicht intakt, wird sie von der Uracil-DNA-Glykosylase ausgeschnitten, während oxidierte Guanin-Basen (8-Oxoguanin) durch 8-Oxoguanin-Glykosylasen entfernt werden. Bei Menschen treten pro Tag pro Zelle ca. 10.000 solcher Schäden auf (Steven et al. 2016). Die Ersetzung von Nukleobasen erfolgt durch das Zusammenspiel zweier Enzyme: Endonukleasen fügen die richtige Base wieder ein und Ligasen verknüpfen erneut den Strang. So sind also allein für die Reparatur von Nukleobasen drei verschiedene Enzymklassen zuständig. Noch komplizierter verhält es sich, wenn das DNA-Rückgrat beschädigt wird (die Zuckereinheiten). Hier sind in Bakterien drei verschiedene Enzymklassen zuständig, während in Eukaryoten hierfür ganze 18 Enzyme zum Einsatz kommen (Steven et al. 2016).
Ist eine Entstehung des Schutzes gegen oxidativen Stress durch Evolution plausibel?
Herausforderungen für die Evolutionslehre
Vor dem Hintergrund der dargestellten Schutz- und Reparaturmechanismen gilt es, die Plausibilität eines Übergangs von strikt anaeroben Organismen hin zu aeroben durch evolutive Vorgänge zu beurteilen. Es ist insgesamt deutlich geworden, dass der Anspruch an einen solchen evolutiven Übergang gewaltig ist. Angesichts einer sehr schnellen Zerstörungsrate sehr vieler zellulärer Bestandteile schon durch sehr geringe Mengen von ROS ist die rasche und zeitgleiche Entstehung einer nahezu unüberschaubaren Fülle von hochkomplexen Mechanismen zur Vorbeugung und Reparatur von mannigfaltigen Schäden unverzichtbar. Es ist auffällig, dass praktisch alle aeroben Lebewesen über diese Vielfalt von Schutzvorrichtungen verfügen, von denen keine verzichtbar zu sein scheint. Selbst ein allmählich oder in wiederholten schwachen Schüben eintretender „Great Oxygen Event“ (GOE) erfordert also eine explosionsartige Bildung hochkomplexer, fein abgestimmter und hochgradig effizienter Schutzmechanismen gegen die Wirkung der giftigen Sauerstoffderivate.
Erschwerend kommt hinzu, dass gegenwärtig sogar strikt anaerobe Organismen über einige Schutzmechanismen gegen oxidativen Stress verfügen und davon ausgegangen wird, dass die Organismen vor dem GOE noch wesentlich empfindlicher gegenüber Schäden durch ROS waren (Sheng et al. 2014). Es erscheint in keiner Weise plausibel, dass solche Lebewesen auch nur einen geringen Hauch Sauerstoff hätten überleben können, geschweige denn eine „große Sauerstoffkatastrophe“. Die wiederholt in der wissenschaftlichen Literatur vorgebrachte Annahme von Rückzugsmöglichkeiten für Organismen in sehr sauerstoffarme Nischen erklärt in keiner Weise, durch welche konkreten Schritte Organismen zu dieser Fülle von Schutzmechanismen gegen ROS gelangt sind.
Alle angeführten Systeme zur Abwehr von oxidativem Stress sind nichtreduzierbar komplex und notwendigerweise hochgradig effizient. Sie bestehen stets aus mehreren aufeinander abgestimmten Komponenten und können nur als Gesamtheit funktionsfähig sein. Als Beispiel sei hier noch einmal das noch relativ simple polyP-Schutzsystem angeführt. Für die Funktion dieses „urtümlichen“ Systems (Gray et al. 2014) bedarf es des Vorhandenseins eines konstant aufrecht erhaltenen ATP-Spiegels in der Zelle, wofür wiederum eine ATP-Synthase notwendig ist – ebenfalls ein reichlich komplexes Protein. Zudem müssen zugleich polyP-auf- und abbauende Enzyme vorliegen (PPK und PPX), wobei es erforderlich ist, dass PPK gegen ROS resistent ist, während bei PPX eine Art Schalter vorliegen muss, damit es bei Vorliegen von ROS deaktiviert werden kann. Bei der Betrachtung solcher Systeme drängt sich teleologisches Denken besonders hartnäckig auf.
Noch weit mehr Schwierigkeiten bereitet allerdings die Tatsache, dass die Entstehung von ROS an zentrale Prozesse des Energiehaushalts gekoppelt ist. So hätten die ersten Mikroorganismen, die Sauerstoff-generierende Photosynthese betrieben, sofort auch über alle Schutzsysteme vor Schäden durch ROS verfügen müssen. Gleiches gilt für die ersten aerob lebenden Organismen: Sobald die erste Atmungskette operativ war, mussten es auch alle ROS-Schutzsysteme sein. Und schließlich müsste erklärt werden, wie die schädlichen ROS auch noch zu unverzichtbaren Botenstoffen geworden sind.
Diese Sachverhalte zeigen auf, dass für Evolution kein nennenswerter Spielraum gegeben ist.
Evolutionstheoretische Hypothesen
Als Argumente für eine evolutive Entstehung solcher Schutzmechanismen und auch aerober Organismen werden meistens vergleichende Analysen heute lebender Lebewesen angeführt. Ähnlichkeiten in der Ausstattung zum Schutz vor ROS werden dann durch Unterstellung einer gemeinsamen Abstammung erklärt. Ein Beispiel dafür ist das Vorliegen von SOD in nahezu allen Organismen (Miller 2012).
In Lebewesen gibt es vier Typen von SOD, die recht unterschiedlich gebaut sind und in ihrem Reaktionszentrum (RZ) verschiedene Metallionen aufnehmen: FeSOD (Eisen im RZ), MnSOD (Mangan im RZ), NiSOD (Nickel im RZ), CuZnSOD (Kupfer und Zink im RZ). SOD sind mittelgroße Enzyme, die aus weit über 200 Aminosäuren bestehen und aus zwei Untereinheiten zusammengesetzt sind. Während in der Domäne der Bakterien alle Typen von SOD vorkommen, weisen Archaea nur solche mit Eisen oder Mangan auf. Protisten* enthalten nur eisenhaltige SOD, während bei Tieren und Pilzen nur CuZnSOD und MnSOD vorkommen (Miller 2012). Darüber hinaus sind die verschiedenen SOD hinsichtlich ihrer Aminosäuresequenz und der dreidimensionalen Struktur recht unterschiedlich. Insgesamt kann also festgehalten werden, dass die Verteilung der verschiedenen SOD sich nicht sinnvoll in allgemein angenommene Abstammungsschemata fügen lässt (Abb. 5). Dies spricht nicht für Evolution, sondern eher für spezifische Schöpfung, die vermutlich den Bedingungen für den jeweiligen Lebensraum und der Kompatibilität mit den jeweiligen Stoffwechselsystemen der Organismen Rechnung trägt.
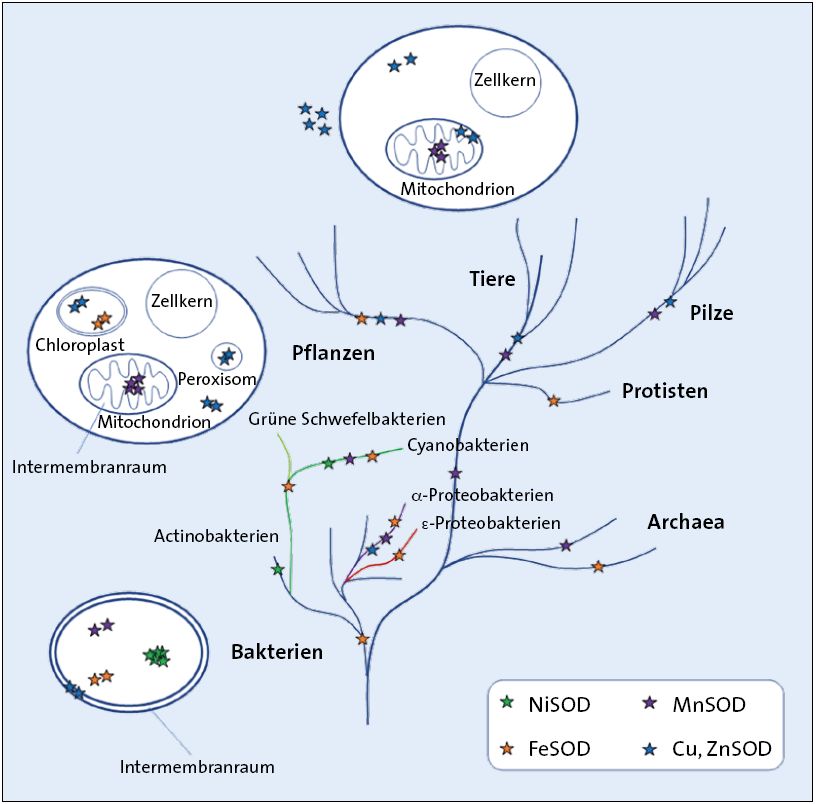
Figure 5. Abb. 5 Verteilung von SOD (Superoxid-Dismutase) in den Domänen des Lebens – angeordnet gemäß dem allgemein angenommenen evolutionstheoretischen Stammbaum (nach Miller 2012). Das Vorliegen von SOD ist durch Sterne verschiedener Farbe dargestellt (blau: CuZnSOD; lila: MnSOD; orange: FeSOD; grün: NiSOD). Bei Annahme einer evolutiven Entstehung aller Organismen erfordert die Verteilung der SOD eine vielfache unabhängige Entstehung der gleichen Typen von Enzymen in verschiedenen Domänen des Lebens (Konvergenzen).
Als weitere Hypothese wird angeführt, dass es schon vor dem GOE reaktive Moleküle gab, mit denen die noch anaerob lebenden Organismen zurechtkommen mussten. So behaupten Neubeck & Freund (2020), dass durch reaktive Schwefelspezies (RSS) eine Art vorbereitender Schwefel-Stress gegeben war, der die Evolution hin zu ROS-Schutzsystemen ermöglichte. Allerdings erweist sich diese Argumentation angesichts der z. T. deutlich anderen chemischen Eigenschaften von ROS im Vergleich zu RSS als komplett unhaltbar. Denn gerade Schwefelverbindungen in Organismen stellen die empfindlichsten Reaktionspartner für ROS dar.
Fazit
Die dargelegten Befunde zeigen deutlich auf, dass die Umstellung auf einen Stoffwechsel mit Sauerstoff (infolge eines GOE) derart hohe Anforderungen an eine Umrüstung von Organismen stellt, dass die Annahme, solche Vorgänge könnten durch Darwin‘sche Evolution verwirklicht werden, in hohem Maße unplausibel erscheint. Nichts spricht dafür, dass dies möglich ist, jedoch sehr vieles dagegen. Demgegenüber sind die unübersehbar teleologischen und biochemisch außerordentlich anspruchsvollen Schutzeinrichtungen gegen oxidativen Stress in Organismen ein eindrucksvolles Indiz für intelligente Schöpfung.
Glossar
aerob: unter Verwendung von Sauerstoff lebend
anaerob: ohne Sauerstoff lebend
Derivat: abgeleitete chemische Verbindung
GOE: great oxygenation event
Homöostase: Wahren eines bestimmten Zustandes physiologischer Parameter (pH-Wert, Konzentrationen etc.)
Protisten: einzellige oder wenigzellige Eukaryoten
ROS: reactive oxygen species (Sauerstoffderivate mit erhöhter chemischer Reaktivität)
SOD: superoxide dismutase (Enzyme, die Superoxid-Moleküle abbauen)
Thermodynamische Triebkraft: aus Energiebilanzen chemischer Prozesse resultierende Richtung bestimmter Vorgänge.
Thiol-Gruppe: funktionelle chemische Gruppe, die aus den Elementen Schwefel und Wasserstoff zusammengesetzt ist: -SH.
Literatur
Akiyama M, Crooke E & Kornberg A (1992) The Polyphosphate Kinase Gene of Escherichia coli. J. Biol. Chem. 267, 22556–22561.
D’Autréaux B & Toledano MB (2007) ROS as signalling molecules: mechanisms that generate specificity in ROS homeostasis. Mol. Cell Biol. 8, 813–824.
Desfougères Y, Saiardi A & Azevedo C (2020) Inorganic polyphosphate in mammals: Where’s Wally? Biochem. Soc. Trans. 48, 95–101.
Galaris D, Barbouti A & Pantopoulos K (2019) Iron homeostasis and oxidative stress: An intimate relationship. Biochim. Biophys. Acta - Mol. Cell Res. 1866, 118535.
Go Y-M, Chandler JD & Jones DP (2015) The cysteine proteome. Free Radic. Biol. Med. 84, 227–245.
Gray MJ & Jakob U (2015) Oxidative Stress protection by polyphosphate - new roles for an old player. Curr. Opin. Microbiol. 24, 1–6.
Gray MJ, Wholey W-J et al. (2014) Polyphosphate is a primordial Chaperone. Molecular Cell 53, 689–699.
Herbert D & Pinsent J (1948) Crystalline Bacterial Catalase. Biochemistry 43, 193–202.
Imlay JA (2013) The molecular mechanisms and physiological consequences of oxidative stress: lessons from a model bacterium. Nat. Rev. Microbiol. 11, 443–454.
Knoll AH & Nowak MA (2017) The timetable of evolution. Sci. Adv. 3, e1603076.
Koppenol WH & Hider RH (2019) Iron and redox cycling. Do’s and don’ts. Free Radic. Biol. Med. 133, 3–10.
Krumova K & Cosa G (2016) Overview of Reactive Oxygen Species. In: Singlet Oxygen: Applications in Biosciences and Nanosciences (Bd. 1, S. 1–21). Royal Society of Chemistry.
McIntyre B & Solesio ME (2021) Mitochondrial inorganic polyphosphate (polyP): the missing link of mammalian bioenergetics. Neural Regeneration Res. 16, 2227–2228.
Miller A-F (2012) Superoxide dismutases: Ancient enzymes and new insights. Febs Letters 586, 585–595.
Milo R & Phillips R (2016) Cell biology by the numbers. Taylor & Francis, Oxfordshire.
Neubeck A & Freund F (2020) Sulfur Chemistry May Have Paved the Way for Evolution of Antioxidants. Astrobiology 20, 670–675.
Pedre B, Young D et al. (2018) Structural snapshots of OxyR reveal the peroxidatic mechanism of H2O2 sensing. Proc. Natl. Acad. Sci. 115, E11623.
Reichmann D, Voth W & Jakob U (2018) Maintaining a Healthy Proteome during Oxidative Stress. Molecular Cell 69, 203–213.
Schmidtgall B (2021) Die „Sauerstoffkatastrophe“. 1. Extreme Krise als Auslöser genialer „Neuerfindungen“ des Lebens? Stud. Integr. J. 28, 13–21.
Sheng Y, Abreu IA et al. (2014) Superoxide dismutases and superoxide reductases. Chem. Rev. 114, 3854–3918.
Sies H & Jones DP (2020) Reactive oxygen species (ROS) as pleiotropic physiological signalling agents. Mol. Cell Biol. 21, 364–383.
Steven AC, Baumeister W et al. (2016) Molecular biology of assemblies and machines (1. Aufl.). Garland Science, New York.
Storz G (2016) New perspectives: Insights into oxidative stress from bacterial studies. Archives of Biochemistry and Biophysics 595, 25–27.
Walsh CT & Tang Y (2019) The Chemical Biology of Human Vitamins. CPI Group, London.
Sauerstoff ist für den Energiehaushalt vieler Lebewesen unverzichtbar. Zugleich sind viele Reaktionsprodukte des Sauerstoffs für Organismen in hohem Maße schädlich. Sie verursachen sogenannten „oxidativen Stress“. Daher sind vielfältige hochkomplexe molekulare Schutzvorrichtungen gegen oxidativen Stress lebensnotwendig. Die Entstehung solcher Vorrichtungen in Lebewesen im Zuge der postulierten großen Sauerstoffkatastrophe durch evolutive Vorgänge erscheint in hohem Maße unplausibel. Aus schöpfungstheoretischer Perspektive bieten sich hier weit bessere Erklärungsmöglichkeiten.
Die „Sauerstoffkatastrophe“
3. Biologische Schutzvorrichtungen gegen oxidativen Stress
Sauerstoff ist für den Energiehaushalt vieler Lebewesen unverzichtbar. Zugleich sind viele Reaktionsprodukte des Sauerstoffs für Organismen in hohem Maße schädlich. Sie verursachen sogenannten „oxidativen Stress“. Daher sind vielfältige hochkomplexe molekulare Schutzvorrichtungen gegen oxidativen Stress lebensnotwendig. Die Entstehung solcher Vorrichtungen in Lebewesen im Zuge der postulierten großen Sauerstoffkatastrophe durch evolutive Vorgänge erscheint in hohem Maße unplausibel. Aus schöpfungstheoretischer Perspektive bieten sich hier weit bessere Erklärungsmöglichkeiten.
Kompakt
Im Rahmen der Evolutionslehre wird angenommen, dass der auf Sauerstoff beruhende (aerobe) Energiestoffwechsel in den Zellen im Zuge der „großen Sauerstoffkatastrophe“ durch Evolution aus strikt anaeroben* Organismen entstand. Während der aerobe* Stoffwechsel hinsichtlich der Effektivität gegenüber dem anaeroben vorteilhaft ist, stellt der Umgang mit giftigen Reaktionsprodukten des Sauerstoffs, den „reactive oxygen species“ (ROS), eine besondere Herausforderung dar. Schäden durch ROS treten sehr schnell und bei sehr vielen Arten von Biomolekülen ein. Proteine werden durch Reaktionen mit ROS zur Entfaltung (Denaturierung) veranlasst und verlieren ihre Funktion, bei der DNA kommt es zu Mutationen oder der Blockade von Ableseprozessen, mehrfach ungesättigte Fettsäurebausteine aus Membranen von Eukaryoten* sind ebenfalls für Schäden durch ROS anfällig. Daher verfügen alle aeroben Organismen über eine große Vielfalt an Einrichtungen zum Schutz und zur Reparatur von Biomolekülen. Untersuchungen solcher Vorrichtungen haben wiederholt gezeigt, dass es sich dabei in der Regel um anspruchsvolle und nichtreduzierbar komplexe Systeme handelt, die offenkundig teleologischer (zielgerichteter) Natur sind. Zudem können Organismen ohne solche Systeme nicht in einer mit Sauerstoff angereicherten Atmosphäre überleben.
Evolutionäre Hypothesen beschränken sich auf das Herausgreifen von Einzelaspekten wie etwa der vergleichenden Analyse von ROS-abbauenden Enzymen in allen Lebewesen oder rein hypothetischen Annahmen wie der Vorbereitung von Organismen auf ROS durch „reactive sulfur species“ (RSS). Insgesamt wird jedoch deutlich, dass schrittweise verlaufende Darwin’sche Vorgänge als Erklärung für eine sehr schnelle und äußerst anspruchsvolle Umrüstung von anaeroben Organismen zu aeroben nicht einmal ansatzweise taugen. Vielmehr weisen die raffiniert eingerichteten und sich gegenseitig ergänzenden Schutzfunktionen auf intelligente Schöpfung hin.
Mit einem Stern* versehene Begriffe werden im Glossar erklärt.
Einleitung
Wann immer ein Antrieb konstruiert wird, stellt sich unmittelbar die Frage nach einer möglichst effizienten Energieverwertung. Nicht weniger wichtig sind jedoch sicherheitstechnische Überlegungen. Treibstoffe von Automobilen sind hochentzündlich, diejenigen von Raketen explosiv. Darüber hinaus sollte die Konstruktion möglichst wenig störanfällig funktionieren. Dies ist wegen einer kaum überschaubaren Zahl an möglichen Ursachen für Funktionsausfälle eine besondere Herausforderung. Dementsprechend heißt es auf der Internetseite eines Expertenteams im Bereich Maschinenbau: „Für Maschinenbauer gehört die Sicherheitstechnik wohl zu den komplexesten und unbeliebtesten Themen.“1 Es müssen viele Eventualitäten im Voraus bedacht und schwierige Entscheidungen getroffen werden, da eingerichtete Sicherheitsfunktionen auch unter unterschiedlichen Bedingungen ihren Zweck erfüllen müssen. Zudem muss gewährleistet sein, dass die Sicherheitsfunktionen die eigentliche Funktion der Maschine nicht nennenswert beeinträchtigen.
Auch in Organismen gibt es eine Vielzahl von Einrichtungen, die Schäden verhindern sollen. Bekannte Beispiele sind das Immunsystem und zelluläre Mechanismen, die Mutationen vorbeugen. Eine weitere Klasse sehr wichtiger Schutzfunktionen bei Lebewesen ist ausgerechnet auf denjenigen chemischen Stoff ausgerichtet, den sehr viele Organismen für ihren Energiehaushalt brauchen: molekularen Sauerstoff (O2). Der Grund dafür ist die Entstehung schädlicher Reaktionsprodukte als Folge verschiedener chemischer Reaktionen von Sauerstoff in Organismen. Für die Evolutionslehre ist dieser Sachverhalt problematisch, da erklärt werden muss, wie Organismen durch einen schrittweisen Vorgang gleichzeitig sowohl einen sauerstoffabhängigen Energiehaushalt als auch eine Reihe von Sicherheitsfunktionen gegen Schäden durch Sauerstoffderivate* erlangt haben können.
Wie in den beiden ersten Folgen zum Thema „Sauerstoffkatastrophe“ ausgeführt, gehen viele Forscher gegenwärtig davon aus, dass die ersten Organismen vor ca. 4 Milliarden Jahren in einer nahezu sauerstofffreien Erdatmosphäre entstanden sein sollen (Knoll & Nowak 2017). Demnach müssten die ersten Organismen Anaerobier* gewesen sein, was unter Kennern des Themas derzeit Konsens ist (Neubeck & Freund 2020). Vor etwa 3 Milliarden Jahren seien dann Sauerstoff-generierende Mikroorganismen evolviert, die für die Anreicherung der Atmosphäre mit Sauerstoff vor ca. 2,4 Milliarden Jahren (Great Oxygenation Event, GOE) verantwortlich sein sollen. Hierbei gehen die Auffassungen bezüglich der Ursachen und des genauen Verlaufs dieses Vorgangs jedoch recht weit auseinander (Schmidtgall 2021). Darüber hinaus wird allgemein angenommen, dass der GOE die Entstehung höherer Organismen überhaupt erst ermöglicht hat – und das trotz der oben erwähnten Schädlichkeit von Sauerstoff. Im Folgenden soll die Frage erörtert werden, ob die Entstehung von Schutzvorrichtungen gegen Schäden durch Sauerstoff durch evolutive Vorgänge im Zuge des GOE plausibel ist.
Schäden durch Sauerstoff in der Zelle
Für den Energiehaushalt vieler Organismen ist molekularer Sauerstoff unverzichtbar. Seine Umwandlung in Wasser in dem als „Zellatmung“ bezeichneten biochemischen Prozess macht den wesentlichen Teil der thermodynamischen* Triebkraft aus, die zur Bildung von ATP, der Energiewährung der Zelle, genutzt wird.
(1) Glucose + 6 O2 ➝ 6 H2O + 6 CO2
∆G = –2870 kJ/Mol Glucose
(Gesamtreaktion der Zellatmung)
Die Nutzung dieser „kontrollierten Verbrennung“ von Kohlenhydraten ermöglicht aeroben* Organismen eine effektivere Art der Energiegewinnung als den Anaerobiern. Der „Treibstoff“ der Aerobier weist eine deutlich höhere Energiedichte auf als derjenige von anaerob lebenden Organismen. Man könnte dies mit der Überlegenheit des Dieseltreibstoffs gegenüber einem Akku elektrisch getriebener Fahrzeuge vergleichen – der erste hat eine ca. 50-fach höhere Energiedichte.
Die Kehrseite der Verwendung von Sauerstoff ist jedoch die Schädlichkeit seiner Reaktionsprodukte. Während das Sauerstoffmolekül selbst praktisch unschädlich ist, wird es bei vielen chemischen und physikalischen Vorgängen in der Zelle in reaktivere Moleküle umgewandelt, die gravierende Schäden verursachen können. Für solche Moleküle hat sich in der Literatur die Sammelbezeichnung „reactive oxygen species“ (ROS) etabliert (Krumova & Cosa 2016). In vielen chemischen Reaktionen des Sauerstoffs in der Zelle entstehen zunächst Superoxidradikale, die anschließend häufig in Wasserstoffperoxid umgesetzt werden (Abb. 1). In weiteren Reaktionen können das besonders reaktive Hydroxylradikal bzw. Radikale verschiedener organischer Verbindungen gebildet werden.
Figure 1. Abb. 1 Die wichtigsten ROS („reactive oxygen species“) und ihre Entstehung aus Sauerstoff durch Aufnahme von Elektronen (e-).
Die jeweiligen ROS gehen je nach ihren Eigenschaften in unterschiedlichem Ausmaß und an verschiedenen molekularen Komponenten der Zelle chemische Reaktionen ein (D’Autréaux & Toledano 2007). Superoxidradikale weisen eine moderate chemische Reaktivität auf und reagieren bevorzugt mit Eisen-Schwefel-Clustern, die in allen Organismen wichtige Funktionen im Energiehaushalt und der Synthese molekularer Bausteine ausführen. Solche Reaktionen können daher zentrale Stoffwechselwege wie die Glykolyse, den Zitratzyklus oder die Synthese bestimmter Aminosäuren beeinträchtigen bzw. zum Erliegen bringen. Wasserstoffperoxid reagiert bevorzugt mit dem Schwefelatom des Cysteins, einer Aminosäure, die in einer Vielzahl von Proteinen aller Organismen vorhanden ist. Durch solche Reaktionen kann es zur Veränderung der dreidimensionalen Struktur der Proteine kommen, sodass sie funktionsunfähig werden. Zudem führen solche Verformungen (Entfaltungen) von Proteinen dazu, dass sie aneinander haften (Aggregation), wodurch sich schwer lösliche und für die Zelle sehr schädliche Plaques bilden.
Aufgrund ihrer Reaktivität unterliegen ROS einer genauen Kontrolle innerhalb der Zelle. Die Konzentration des etwas stabileren Wasserstoffperoxids liegt etwa im nanomolaren* Bereich und ist ungefähr um den Faktor Tausend höher als diejenige des labileren Superoxidradikals (Sies & Jones 2020). Zu Schäden durch ROS kommt es vor allem dann, wenn die hochreaktiven Hydroxylradikale entstehen. Von besonderer Wichtigkeit ist hierbei ein chemischer Prozess, der als Fenton-Reaktion bezeichnet wird (Koppenol & Hider 2019).
(2)2 O2•– + 2 H+ ➝ H2O2 + O2
(Katalysator: Superoxid-Dismutase)
Fenton-Reaktion:
(3)Fe2+ + H2O2 ➝ Fe3+ + OH• + OH–
Superoxidradikale werden schnell durch das Enzym Superoxid-Dismutase (SOD) in Wasserstoffperoxid umgewandelt, das bei Vorhandensein von Fe2+ gespalten wird, sodass sich Hydroxylradikale bilden. Diese Radikale reagieren wahllos mit allen molekularen Komponenten der Zelle. Ob Nukleinsäuren (DNA und RNA), Proteine oder Bestandteile der Zellwand – durch Reaktion mit Hydroxylradikalen entstehen gravierende Schäden in allen Typen biochemischer Funktionseinheiten.
Durch Reaktionen von Hydroxylradikalen mit DNA kommt es zu Mutationen oder zur vollständigen Blockade des Ablesevorgangs der RNA-Polymerase. Vor allem letztere Schäden können für Organismen tödlich sein, wenn sie nicht rechtzeitig repariert werden. In diesem Zusammenhang ist auch zu berücksichtigen, dass die Bildung von ROS in hohem Maße gefördert wird, wenn Moleküle vorhanden sind, die Elektronen auf den Sauerstoff übertragen (s. Kasten „Entstehung von ROS“). Daher muss in Zellen auch die Konzentration freier Metallionen wie Fe2+/3+ und organischer Elektronenüberträger streng kontrolliert werden (Galaris et al. 2019; Imlay 2013). Erhöhte Konzentrationen von ROS und damit einhergehender oxidativer Stress führen relativ schnell zum programmierten Zelltod.
Die Geschwindigkeit, mit der die beschriebenen Schäden durch ROS eintreten, ist unter heutigen Bedingungen sehr hoch. Beispielsweise liegt die Halbwertszeit für beschädigte Eisen-Schwefel-Cluster im Darmbakterium E. coli selbst bei Vorhandensein von ausreichend SOD und einer niedrigen Konzentration von 0,1 nM Superoxidionen im zellulären Milieu bei nur 20 Minuten (Imlay 2013). Das daraus resultierende Problem beschreibt Imlay wie folgt: „Dieser Zeitrahmen ist im Vergleich zu der Zellteilungsrate sehr kurz, weswegen diese Situation nur tolerabel ist, weil Zellen beständig die beschädigten Cluster durch chemische Reduktion und Remetallierung reparieren.“
Es wäre jedoch zu kurz gegriffen, nur im Überschuss an ROS eine Gefahr für die reibungslose Funktion der Zellbiochemie zu sehen. Inzwischen ist auch bekannt, dass eine zu niedrige Konzentration an ROS ebenfalls schädlich ist, da diese Moleküle in allen aeroben Organismen als Botenstoffe fungieren (Go et al. 2015; Sies & Jones 2020). Dementsprechend ist für diese Moleküle auch das Wahren einer definierten Konzentration (Homöostase) notwendig.
Kasten 1 | Entstehung und Nutzung von ROS in der Zelle
ROS können durch chemische Reaktionen des Sauerstoffs mit Biomolekülen der Zelle (endogene* Quellen) oder mit von außen stammenden chemischen Verbindungen (exogene* Quellen) gebildet werden. Bei den Reaktionspartnern, die zur Entstehung von ROS führen, handelt es sich im Allgemeinen um Moleküle, die leicht ein einzelnes Elektron auf Sauerstoffmoleküle übertragen, sodass Superoxidionen entstehen. Zu solchen Quellen von ROS gehören vor allem ungebundene Metallionen (Fe2+, Cu1+) oder organische Elektronenüberträger wie Chinole oder Phenazine (Abb. 2). Aber auch Eisenspeicherproteine und bestimmte eisenhaltige Enzyme können zur Entstehung von ROS beitragen. Bei höheren Lebewesen kommen solche Vorgänge vor allem in Phagozyten (weißen Blutkörperchen) vor. Phagozyten enthalten Transmembran-Enzyme mit der Bezeichnung NADPH-Oxidasen (NOXs), die zur Abtötung von Krankheitserregern Superoxidionen erzeugen und darüber hinaus unverzichtbare Funktionen in der Zelldifferenzierung und dem programmierten Zelltod ausüben (Magnani et al. 2017).
Eine andere bedeutende Quelle von ROS sind Mitochondrien – die „Kraftwerke“ der Zelle. Dort sind vor allem die NADH-Dehydrogenasen (Komplex I) und die Chinole des Q-Pools für einen hohen Eintrag von Superoxidionen ursächlich (Krumova & Cosa 2016). Insgesamt gibt es in menschlichen Zellen über 40 Enzyme, die Superoxidradikale bzw. Wasserstoffperoxid generieren (Go et al. 2015). Darüber hinaus gibt es noch eine Reihe an Enzymen, bei deren normaler Funktion als Nebenprodukt ROS anfallen. Hier sind insbesondere eisenhaltige Cytochrome und Fettsäure-oxidierende Lipoxygenasen zu nennen.
Neben chemischen Reaktionen kann energiereiche Strahlung durch Spaltung chemischer Bindungen (z. B. bei Wasserstoffperoxid) Sauerstoffradikale erzeugen oder das Sauerstoffmolekül in einen angeregten Zustand versetzen (Singulett-Sauerstoff). Solche Vorgänge sind vor allem in Organismen und Geweben relevant, die in erhöhtem Ausmaß dem Licht ausgesetzt sind (Sies & Jones 2020). Es kann also durchaus davon gesprochen werden, dass die Bildung von ROS ein ständiger und weit verbreiteter Vorgang in Zellen ist.
Figure 2. Abb. 2 Strukturformeln und Kalottenmodelle der organischen Elektronenüberträger Chinol und Phenazin (Atomsymbole: grau: Kohlenstoff, rot: Sauerstoff, blau: Stickstoff, weiß: Wasserstoff).
Zelluläre Vorrichtungen zum Schutz gegen oxidativen Stress
Kontrolle der Konzentration an ROS in der Zelle
Da ROS im zellulären Geschehen bei vielen Vorgängen und in vielen Kompartimenten anfallen, bedarf es einer großen Vielfalt von Mechanismen, die für einen Abbau der ROS sorgen. Die Notwendigkeit solcher Schutzvorrichtungen ist bei allen Lebewesen gegeben, die mit Sauerstoff in Kontakt kommen. Bei höheren Lebewesen gelangt der Sauerstoff über Transportmechanismen in die Zellen, während er bei Mikroorganismen einfach durch die Zellwand diffundiert.
Bakterielle Zellwände sind im Unterschied zu denjenigen von höheren Organismen deutlich weniger für Schäden durch ROS anfällig, da sie überwiegend aus gesättigten bzw. einfach ungesättigten Fettsäure-Bausteinen bestehen. Dagegen müssen alle anderen molekularen Komponenten von Zellen stets vor den schädlichen Wirkungen der ROS geschützt werden, und angesichts sehr schnell eintretender Schäden müssen rasche Reparaturprozesse erfolgen. So besitzen selbst kleine Bakterien ausgefeilte mehrstufige Systeme zur Abwehr von oxidativem Stress.
Enzyme: Viele Bakterien (Prokaryoten und Archaeen) und alle höheren Organismen verfügen über verschiedene Enzyme, die Superoxidradikale und Wasserstoffperoxid abbauen (Abb. 3). Der Abbau von Superoxidradikalen erfolgt hauptsächlich durch Enzyme, die als Superoxid-Dismutasen (SOD) bezeichnet werden. Das Funktionsprinzip ist dabei die Beschleunigung des Zerfalls von Superoxidradikalen zu Sauerstoff (O2) und Wasserstoffperoxid (H2O2) (s. Reaktionsgleichung 3). Zudem weisen viele Organismen Katalasen auf, die Wasserstoffperoxid zu Sauerstoff und Wasser zersetzen. Diese Enzyme sind ein sehr effektiver Schutz gegen ROS, da sie diese giftigen (weil sehr reaktiven) Moleküle mit der physikalisch nahezu maximal möglichen Reaktionsgeschwindigkeit von 106-107 Reaktionen pro Sekunde abbauen (Herbert & Pinsent 1948; Milo & Phillips 2016). Diese Reaktionsgeschwindigkeiten gehören zu den schnellsten überhaupt. Sie sind um das 105-Fache höher als durchschnittliche Enzymreaktionen und stellen eher Ausnahmen dar (Milo & Phillips 2016).
Figure 3. Abb. 3 Enzymatischer Abbau von Superoxidradikalen durch SOD (A) und von Wasserstoffperoxid durch Katalasen (B).
Molekulare Regler (Regulons) der Synthese von SOD und Katalasen: Entscheidend für die Wirkung der oben angeführten Enzyme ist ihre Konzentration im zellulären Milieu, die wiederum davon abhängig ist, in welcher Rate sie in der Zelle synthetisiert werden. Hierfür gibt es in bakteriellen Zellen Sensoren, die dafür sorgen, dass die Synthese dieser Enzyme hoch- bzw. herunterfahren wird, je nachdem wie hoch die Belastung durch oxidativen Stress ist (Imlay 2013).
Bei einigen Bakterien fungieren als OxyR bezeichnete Proteine als Regler der Konzentration von Katalasen und SOD. OxyR werden durch Reaktion mit Wasserstoffperoxid oder Superoxidradikalen in eine aktive Form überführt, die durch Aktivieren entsprechender Gene die Synthese von SOD und Katalasen ankurbelt (Pedre et al. 2018). Bei E. coli-Bakterien erfolgt diese Reaktion innerhalb von 1-2 Minuten, nachdem die Zellen mit Wasserstoffperoxid in Kontakt kommen, und ist damit extrem schnell (Storz 2016). Ebbt der oxidative Stress wieder ab, wird OxyR durch Reaktion mit Glutaredoxin, einem kleinen Protein, aus der aktiven wieder in eine inaktive Form überführt. Interessanterweise gibt es bei vielen grampositiven Bakterien ein Detektionssystem für ROS, das in umgekehrter Weise funktioniert: Ein Protein mit der Bezeichnung PerR hemmt in seiner aktiven Form die Synthese von SOD und Katalasen. Durch Reaktion mit H2O2 wird PerR inaktiviert und löst sich von der DNA, sodass die Synthese von ROS-abbauenden Enzymen in Fahrt kommt.
Wie schon zuvor erwähnt, gibt es organische Moleküle, die die Entstehung von Superoxiden durch Elektronentransfer auf Sauerstoff fördern (z. B. Phenazine, Chinole). Solche Moleküle können leicht Zellmembranen durchdringen, da sie selbst fettliebend sind. Im Inneren der Zelle entziehen diese Moleküle bestimmten Komponenten der Atmungskette Elektronen (vor allem von Flavinen) und übertragen sie dann auf Sauerstoff, sodass Superoxidradikale gebildet werden. Es konnte gezeigt werden, dass die Gegenwart von Phenazinen die Superoxid-Konzentration in Bakterienzellen auf das ca. 100-Fache erhöht (Imlay 2013). Daher verfügen Bakterien über ein weiteres regulatorisches Protein (SoxR), das weder auf H2O2 noch auf Superoxidradikale anspricht, sondern auf organische Moleküle, die als Elektronenüberträger fungieren. Auch SoxR fördert in seiner durch ROS aktivierten Form die Synthese von SOD.
Bakterien weisen also ein Schutzsystem auf, das die Zelle auf zweifache Weise gegen oxidativen Stress absichert. Es detektiert sowohl die Moleküle, die die Schäden verursachen (Superoxidradikale, Wasserstoffperoxid), als auch organische Verbindungen, die ihre Entstehung fördern. In beiden Fällen folgt auf die Detektion eine schnelle Reaktion, indem Enzyme hergestellt werden, die die ROS abbauen.
Vitamine und andere kleine Moleküle: Abgesehen von den komplexen Schutzmechanismen durch aufwändige Nanomaschinen gibt es in Organismen eine Reihe von kleinen Molekülen, die in relativ hoher Konzentration im Zellmilieu vorliegen und zum Abfangen der ROS dienen. Besondere Wichtigkeit haben hierbei schwefelhaltige kleine Peptide wie Glutathion oder einige Vitamine. Bei höheren Lebewesen spielen Vitamine im Hinblick auf oxidativen Stress eine wichtigere Rolle als bei Bakterien, da vor allem die Zellmembran höherer Organismen wegen ihrer mehrfach ungesättigten Fettsäure-Bausteine recht empfindlich gegenüber Schäden durch ROS ist. Verhindert werden solche Schäden vor allem durch die gemeinsame Wirkung von Vitamin E (a-Tocopherol) und Vitamin C (Ascorbinsäure). Vitamin E ist ein ausgesprochen fettliebendes Molekül, das deshalb in die Zellwand aufgenommen wird. Es neutralisiert ROS unter Bildung sehr langlebiger Radikale, die für Zellbestandteile sehr viel weniger schädlich sind. An der Grenzfläche von Zellwand und Zellinnenraum werden Vitamin-E-Moleküle durch Reaktion mit Vitamin C wieder regeneriert (Walsh & Tang 2019).
Figure 4. Abb. 4 Abbau von ROS durch chemische Reaktion mit Vitamin E/Vitamin C. Innerhalb der Zellmembran erfolgt der Abbau von ROS durch Reaktion mit Vitamin E (Vit E), wobei es zur Bildung des Semichinons des Vitamin E (Vit E SemiQ) kommt. Vitamin E wird durch Reaktion mit Vitamin C regeneriert, wobei es nach zwei Zyklen zur Bildung des Chinons des Vitamin C kommt. Dieses Molekül wird durch Reaktion mit zwei Molekülen Glutathion (GSH) wieder ins Vitamin C überführt.
Kasten 2 | Funktionsweise der molekularen Regler OxyR und SoxR
OxyR-Proteine weisen an einer bestimmten Stelle exponierte Thiol-(-SH)-Gruppen* auf, die infolge einer Oxidation durch H2O2 eine Disulfidbrücke (-S-S-) bilden (Pedre et al. 2018). Dieser Vorgang zieht eine Veränderung der dreidimensionalen Struktur nach sich, sodass OxyR dann mit einer erhöhten Affinität an bestimmte Genregionen bindet und so die Synthese von SOD und Katalasen fördert. Als Proteine, die durch Binden an die DNA die Transkription bestimmter Gene fördern, zählen die OxyR zu den Transkriptionsfaktoren. Auch das Protein PerR funktioniert nach dem gleichen Prinzip, nur in umgekehrter Weise: Bei geknüpfter Disulfidbrücke weist es eine sehr geringe Affinität zu einer bestimmten DNA-Region auf, während die Spaltung der Brücke eine sehr hohe Affinität bewirkt. Da PerR die Transkription einer DNA-Region verhindert, solange es daran gebunden ist, spricht man von einem Repressor.
SoxR ist ein Protein, das aus zwei Untereinheiten zusammengesetzt ist. Es beinhaltet in jeder Untereinheit jeweils ein oxidationsempfindliches Eisen-Schwefel-Zentrum, das überraschenderweise ausgesprochen selektiv mit organischen Elektronenüberträgern (Chinole, Phenazine) reagiert und nicht mit ROS, wie dies im Fall vieler anderer Fe-S-Zentren geschieht. SoxR bindet stets an die DNA, wobei nur die oxidierte Form die Synthese von SOD anregt. Wenn die giftigen organischen Verbindungen beseitigt sind, wird SoxR reduziert oder abgebaut, sodass die Synthese von SOD nicht weiter aktiviert wird.
Schutz vor den Folgen der Wirkung von ROS und Reparatur beschädigter Biomoleküle
Schutz vor der Aggregation* von Proteinen: Wie oben erwähnt führt oxidativer Stress zu einer verstärkten Fehlfaltung von Proteinen und zur Bildung schädlicher Plaques. Ein wichtiger Mechanismus der Vorbeugung der Proteinaggregation in Lebewesen ist erst in den letzten ca. 30 Jahren näher erforscht worden. Kornberg et al. fanden bereits in den 1990er Jahren heraus, dass Bakterien deutlich empfindlicher auf verschiedene Arten von Stress reagieren, wenn Polyphosphat (polyP) nicht in genügender Konzentration vorliegt (Akiyama et al. 1992). Allerdings fand man erst später heraus, warum es sich so verhält. Bei E. coli-Bakterien, die erhöhten Konzentrationen von H2O2 ausgesetzt wurden, ist eine verstärkte Bildung langer Kettenmoleküle aus Phosphateinheiten (polyP) nachgewiesen worden (Gray et al. 2014). Wie gezeigt werden konnte, verhindern polyP-Moleküle selbst bei hohen Konzentrationen von ROS nahezu komplett die Aggregation von Proteinen. Auch bei Fehlfaltungen von Proteinen in Folge von erhöhten Temperaturen erwiesen sich polyP-Makromoleküle als sehr wirksam, wobei längere polyP-Ketten (>100 Phosphat-Einheiten) effektiver waren als kurze (< 50 Phosphat-Einheiten) (Gray & Jakob 2015). Die Wirkungsweise von polyP-Ketten ist relativ simpel: Sie umwickeln fehlgefaltete Proteine und sorgen aufgrund ihrer vielfachen negativen Ladung für gegenseitige Abstoßung. PolyP-Kettenmoleküle sind chemisch relativ robust und unempfindlich gegenüber Reaktionen mit ROS. Ihre Synthese in E. coli erfolgt durch das Enzym polyP-Kinase (PPK) aus Adenosintriphosphat (ATP) und der Abbau durch Exopolyphosphatasen (PPX). Im Fall von oxidativem Stress werden Exopolyphosphatasen von ROS inhibiert, d. h. unfähig gemacht, ihre Funktion auszuüben. Folglich kommt es zu einer Anhäufung von polyP, sodass die gefährliche Proteinaggregation verhindert wird. Nimmt die Belastung durch ROS wieder ab, sorgen die erneut aktivierten PPX für einen schnellen Abbau von polyP, da es in erhöhter Konzentration ebenfalls giftig ist (Desfougères et al. 2020).
PolyP ist in allen bisher untersuchten Organismen nachgewiesen worden und scheint vor allem in Säugetieren an einer ganzen Reihe von wichtigen Prozessen wie Proteinhomöostase*, Energiehaushalt und programmiertem Zelltod beteiligt zu sein (McIntyre & Solesio 2021). Im Unterschied zu Bakterien sind allerdings viele Details bezüglich der Synthese von polyP und seiner Funktionen in höheren Organismen noch unbekannt (Desfougères et al. 2020). Es kann jedoch festgehalten werden, dass alle Lebewesen, die mit Sauerstoff in Kontakt kommen, ohne polyP und dessen wichtiger Schutzfunktion nicht leben könnten.
Reparatur entfalteter Proteine: Der Schutz durch polyP beschränkt sich auf das Verhindern der Aggregation der Proteine. Schäden an den Proteinen werden dadurch nicht behoben. Wenn also die Stresssituation vorbei ist und das polyP wieder abgebaut wird, ist eine Reparatur der Proteine erforderlich, da sie anderenfalls aggregieren können. Hierfür besitzen wiederum alle Typen von Zellen Proteine, die der Fehlfaltung vorbeugen bzw. fehlerhaft gefaltete Proteine wieder in die richtige Form bringen. Solche Proteine werden allgemein als Chaperone bezeichnet. Während im Fall erhöhter Temperaturen in vielen Organismen die Synthese ATP-abhängiger Hitzeschockproteine aktiviert wird (z. B. Hsp 60 in E. coli), sieht die Strategie bei oxidativem Stress anders aus. Zunächst wird die Synthese von Proteinen hochreguliert, die entfaltete Proteine binden und so die Aggregation verhindern (Holdasen). Holdasen lösen sich erst dann von ihrem Bindungspartner, wenn die ROS abgebaut sind und zusätzlich ein ATP-abhängiges Protein bereitsteht, das entfaltete Protein zu reparieren. Solche Systeme liegen sowohl bei Bakterien vor (E. coli: Hsp33) als auch bei Eukaryoten (Hefe: Get3). Es handelt sich dabei um exakt getaktetes Protein-Teamwork, wie es auch von Reichmann et al. beschrieben wird (Reichmann et al. 2018): „Die Inaktivierung von oxidiertem Hsp33 und die Freisetzung von betroffenen Proteinen werden ebenfalls sorgfältig orchestriert und erfordern nicht nur reduzierende Bedingungen, sondern auch die Anwesenheit von faltenden Chaperonen und ATP, die die Rückfaltung der gebundenen Proteine unterstützen.“
DNA-Reparatur: Schäden an Proteinen zu verhindern und zu beheben ist jedoch bei Weitem nicht ausreichend für die Stabilität einer Zelle unter aeroben Bedingungen, da Auswirkungen von Schäden an der DNA erheblich schwerere Konsequenzen nach sich ziehen. Die Reparatur von DNA-Molekülen ist jedoch nicht weniger aufwändig als diejenige von Proteinen. Das Reparaturprinzip besteht im Ausschneiden beschädigter Teile und anschließendem Ersetzen durch intakte Entsprechungen, wobei es verschiedene Typen von Enzymen für die Reparatur von verschiedenen Schäden an der DNA gibt. Für das Erkennen und Ausschneiden beschädigter Nukleobasen* sind DNA-Glykosylasen zuständig, wobei es je nach Art des Schadens unterschiedliche Enzyme gibt (Steven et al. 2016). Ist die Nukleobase Cystein nicht intakt, wird sie von der Uracil-DNA-Glykosylase ausgeschnitten, während oxidierte Guanin-Basen (8-Oxoguanin) durch 8-Oxoguanin-Glykosylasen entfernt werden. Bei Menschen treten pro Tag pro Zelle ca. 10.000 solcher Schäden auf (Steven et al. 2016). Die Ersetzung von Nukleobasen erfolgt durch das Zusammenspiel zweier Enzyme: Endonukleasen fügen die richtige Base wieder ein und Ligasen verknüpfen erneut den Strang. So sind also allein für die Reparatur von Nukleobasen drei verschiedene Enzymklassen zuständig. Noch komplizierter verhält es sich, wenn das DNA-Rückgrat beschädigt wird (die Zuckereinheiten). Hier sind in Bakterien drei verschiedene Enzymklassen zuständig, während in Eukaryoten hierfür ganze 18 Enzyme zum Einsatz kommen (Steven et al. 2016).
Ist eine Entstehung des Schutzes gegen oxidativen Stress durch Evolution plausibel?
Herausforderungen für die Evolutionslehre
Vor dem Hintergrund der dargestellten Schutz- und Reparaturmechanismen gilt es, die Plausibilität eines Übergangs von strikt anaeroben Organismen hin zu aeroben durch evolutive Vorgänge zu beurteilen. Es ist insgesamt deutlich geworden, dass der Anspruch an einen solchen evolutiven Übergang gewaltig ist. Angesichts einer sehr schnellen Zerstörungsrate sehr vieler zellulärer Bestandteile schon durch sehr geringe Mengen von ROS ist die rasche und zeitgleiche Entstehung einer nahezu unüberschaubaren Fülle von hochkomplexen Mechanismen zur Vorbeugung und Reparatur von mannigfaltigen Schäden unverzichtbar. Es ist auffällig, dass praktisch alle aeroben Lebewesen über diese Vielfalt von Schutzvorrichtungen verfügen, von denen keine verzichtbar zu sein scheint. Selbst ein allmählich oder in wiederholten schwachen Schüben eintretender „Great Oxygen Event“ (GOE) erfordert also eine explosionsartige Bildung hochkomplexer, fein abgestimmter und hochgradig effizienter Schutzmechanismen gegen die Wirkung der giftigen Sauerstoffderivate.
Erschwerend kommt hinzu, dass gegenwärtig sogar strikt anaerobe Organismen über einige Schutzmechanismen gegen oxidativen Stress verfügen und davon ausgegangen wird, dass die Organismen vor dem GOE noch wesentlich empfindlicher gegenüber Schäden durch ROS waren (Sheng et al. 2014). Es erscheint in keiner Weise plausibel, dass solche Lebewesen auch nur einen geringen Hauch Sauerstoff hätten überleben können, geschweige denn eine „große Sauerstoffkatastrophe“. Die wiederholt in der wissenschaftlichen Literatur vorgebrachte Annahme von Rückzugsmöglichkeiten für Organismen in sehr sauerstoffarme Nischen erklärt in keiner Weise, durch welche konkreten Schritte Organismen zu dieser Fülle von Schutzmechanismen gegen ROS gelangt sind.
Alle angeführten Systeme zur Abwehr von oxidativem Stress sind nichtreduzierbar komplex und notwendigerweise hochgradig effizient. Sie bestehen stets aus mehreren aufeinander abgestimmten Komponenten und können nur als Gesamtheit funktionsfähig sein. Als Beispiel sei hier noch einmal das noch relativ simple polyP-Schutzsystem angeführt. Für die Funktion dieses „urtümlichen“ Systems (Gray et al. 2014) bedarf es des Vorhandenseins eines konstant aufrecht erhaltenen ATP-Spiegels in der Zelle, wofür wiederum eine ATP-Synthase notwendig ist – ebenfalls ein reichlich komplexes Protein. Zudem müssen zugleich polyP-auf- und abbauende Enzyme vorliegen (PPK und PPX), wobei es erforderlich ist, dass PPK gegen ROS resistent ist, während bei PPX eine Art Schalter vorliegen muss, damit es bei Vorliegen von ROS deaktiviert werden kann. Bei der Betrachtung solcher Systeme drängt sich teleologisches Denken besonders hartnäckig auf.
Noch weit mehr Schwierigkeiten bereitet allerdings die Tatsache, dass die Entstehung von ROS an zentrale Prozesse des Energiehaushalts gekoppelt ist. So hätten die ersten Mikroorganismen, die Sauerstoff-generierende Photosynthese betrieben, sofort auch über alle Schutzsysteme vor Schäden durch ROS verfügen müssen. Gleiches gilt für die ersten aerob lebenden Organismen: Sobald die erste Atmungskette operativ war, mussten es auch alle ROS-Schutzsysteme sein. Und schließlich müsste erklärt werden, wie die schädlichen ROS auch noch zu unverzichtbaren Botenstoffen geworden sind.
Diese Sachverhalte zeigen auf, dass für Evolution kein nennenswerter Spielraum gegeben ist.
Evolutionstheoretische Hypothesen
Als Argumente für eine evolutive Entstehung solcher Schutzmechanismen und auch aerober Organismen werden meistens vergleichende Analysen heute lebender Lebewesen angeführt. Ähnlichkeiten in der Ausstattung zum Schutz vor ROS werden dann durch Unterstellung einer gemeinsamen Abstammung erklärt. Ein Beispiel dafür ist das Vorliegen von SOD in nahezu allen Organismen (Miller 2012).
In Lebewesen gibt es vier Typen von SOD, die recht unterschiedlich gebaut sind und in ihrem Reaktionszentrum (RZ) verschiedene Metallionen aufnehmen: FeSOD (Eisen im RZ), MnSOD (Mangan im RZ), NiSOD (Nickel im RZ), CuZnSOD (Kupfer und Zink im RZ). SOD sind mittelgroße Enzyme, die aus weit über 200 Aminosäuren bestehen und aus zwei Untereinheiten zusammengesetzt sind. Während in der Domäne der Bakterien alle Typen von SOD vorkommen, weisen Archaea nur solche mit Eisen oder Mangan auf. Protisten* enthalten nur eisenhaltige SOD, während bei Tieren und Pilzen nur CuZnSOD und MnSOD vorkommen (Miller 2012). Darüber hinaus sind die verschiedenen SOD hinsichtlich ihrer Aminosäuresequenz und der dreidimensionalen Struktur recht unterschiedlich. Insgesamt kann also festgehalten werden, dass die Verteilung der verschiedenen SOD sich nicht sinnvoll in allgemein angenommene Abstammungsschemata fügen lässt (Abb. 5). Dies spricht nicht für Evolution, sondern eher für spezifische Schöpfung, die vermutlich den Bedingungen für den jeweiligen Lebensraum und der Kompatibilität mit den jeweiligen Stoffwechselsystemen der Organismen Rechnung trägt.
Figure 5. Abb. 5 Verteilung von SOD (Superoxid-Dismutase) in den Domänen des Lebens – angeordnet gemäß dem allgemein angenommenen evolutionstheoretischen Stammbaum (nach Miller 2012). Das Vorliegen von SOD ist durch Sterne verschiedener Farbe dargestellt (blau: CuZnSOD; lila: MnSOD; orange: FeSOD; grün: NiSOD). Bei Annahme einer evolutiven Entstehung aller Organismen erfordert die Verteilung der SOD eine vielfache unabhängige Entstehung der gleichen Typen von Enzymen in verschiedenen Domänen des Lebens (Konvergenzen).
Als weitere Hypothese wird angeführt, dass es schon vor dem GOE reaktive Moleküle gab, mit denen die noch anaerob lebenden Organismen zurechtkommen mussten. So behaupten Neubeck & Freund (2020), dass durch reaktive Schwefelspezies (RSS) eine Art vorbereitender Schwefel-Stress gegeben war, der die Evolution hin zu ROS-Schutzsystemen ermöglichte. Allerdings erweist sich diese Argumentation angesichts der z. T. deutlich anderen chemischen Eigenschaften von ROS im Vergleich zu RSS als komplett unhaltbar. Denn gerade Schwefelverbindungen in Organismen stellen die empfindlichsten Reaktionspartner für ROS dar.
Fazit
Die dargelegten Befunde zeigen deutlich auf, dass die Umstellung auf einen Stoffwechsel mit Sauerstoff (infolge eines GOE) derart hohe Anforderungen an eine Umrüstung von Organismen stellt, dass die Annahme, solche Vorgänge könnten durch Darwin‘sche Evolution verwirklicht werden, in hohem Maße unplausibel erscheint. Nichts spricht dafür, dass dies möglich ist, jedoch sehr vieles dagegen. Demgegenüber sind die unübersehbar teleologischen und biochemisch außerordentlich anspruchsvollen Schutzeinrichtungen gegen oxidativen Stress in Organismen ein eindrucksvolles Indiz für intelligente Schöpfung.
Glossar
aerob: unter Verwendung von Sauerstoff lebend
anaerob: ohne Sauerstoff lebend
Derivat: abgeleitete chemische Verbindung
GOE: great oxygenation event
Homöostase: Wahren eines bestimmten Zustandes physiologischer Parameter (pH-Wert, Konzentrationen etc.)
Protisten: einzellige oder wenigzellige Eukaryoten
ROS: reactive oxygen species (Sauerstoffderivate mit erhöhter chemischer Reaktivität)
SOD: superoxide dismutase (Enzyme, die Superoxid-Moleküle abbauen)
Thermodynamische Triebkraft: aus Energiebilanzen chemischer Prozesse resultierende Richtung bestimmter Vorgänge.
Thiol-Gruppe: funktionelle chemische Gruppe, die aus den Elementen Schwefel und Wasserstoff zusammengesetzt ist: -SH.
Literatur
Akiyama M, Crooke E & Kornberg A (1992) The Polyphosphate Kinase Gene of Escherichia coli. J. Biol. Chem. 267, 22556–22561.
D’Autréaux B & Toledano MB (2007) ROS as signalling molecules: mechanisms that generate specificity in ROS homeostasis. Mol. Cell Biol. 8, 813–824.
Desfougères Y, Saiardi A & Azevedo C (2020) Inorganic polyphosphate in mammals: Where’s Wally? Biochem. Soc. Trans. 48, 95–101.
Galaris D, Barbouti A & Pantopoulos K (2019) Iron homeostasis and oxidative stress: An intimate relationship. Biochim. Biophys. Acta - Mol. Cell Res. 1866, 118535.
Go Y-M, Chandler JD & Jones DP (2015) The cysteine proteome. Free Radic. Biol. Med. 84, 227–245.
Gray MJ & Jakob U (2015) Oxidative Stress protection by polyphosphate - new roles for an old player. Curr. Opin. Microbiol. 24, 1–6.
Gray MJ, Wholey W-J et al. (2014) Polyphosphate is a primordial Chaperone. Molecular Cell 53, 689–699.
Herbert D & Pinsent J (1948) Crystalline Bacterial Catalase. Biochemistry 43, 193–202.
Imlay JA (2013) The molecular mechanisms and physiological consequences of oxidative stress: lessons from a model bacterium. Nat. Rev. Microbiol. 11, 443–454.
Knoll AH & Nowak MA (2017) The timetable of evolution. Sci. Adv. 3, e1603076.
Koppenol WH & Hider RH (2019) Iron and redox cycling. Do’s and don’ts. Free Radic. Biol. Med. 133, 3–10.
Krumova K & Cosa G (2016) Overview of Reactive Oxygen Species. In: Singlet Oxygen: Applications in Biosciences and Nanosciences (Bd. 1, S. 1–21). Royal Society of Chemistry.
McIntyre B & Solesio ME (2021) Mitochondrial inorganic polyphosphate (polyP): the missing link of mammalian bioenergetics. Neural Regeneration Res. 16, 2227–2228.
Miller A-F (2012) Superoxide dismutases: Ancient enzymes and new insights. Febs Letters 586, 585–595.
Milo R & Phillips R (2016) Cell biology by the numbers. Taylor & Francis, Oxfordshire.
Neubeck A & Freund F (2020) Sulfur Chemistry May Have Paved the Way for Evolution of Antioxidants. Astrobiology 20, 670–675.
Pedre B, Young D et al. (2018) Structural snapshots of OxyR reveal the peroxidatic mechanism of H2O2 sensing. Proc. Natl. Acad. Sci. 115, E11623.
Reichmann D, Voth W & Jakob U (2018) Maintaining a Healthy Proteome during Oxidative Stress. Molecular Cell 69, 203–213.
Schmidtgall B (2021) Die „Sauerstoffkatastrophe“. 1. Extreme Krise als Auslöser genialer „Neuerfindungen“ des Lebens? Stud. Integr. J. 28, 13–21.
Sheng Y, Abreu IA et al. (2014) Superoxide dismutases and superoxide reductases. Chem. Rev. 114, 3854–3918.
Sies H & Jones DP (2020) Reactive oxygen species (ROS) as pleiotropic physiological signalling agents. Mol. Cell Biol. 21, 364–383.
Steven AC, Baumeister W et al. (2016) Molecular biology of assemblies and machines (1. Aufl.). Garland Science, New York.
Storz G (2016) New perspectives: Insights into oxidative stress from bacterial studies. Archives of Biochemistry and Biophysics 595, 25–27.
Walsh CT & Tang Y (2019) The Chemical Biology of Human Vitamins. CPI Group, London.
